
题目列表(包括答案和解析)
3.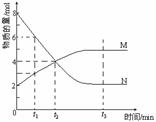 (2001年全国高考题)在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
(2001年全国高考题)在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
A.反应的化学方程式:2M  N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时N的浓度是M浓度的2倍
(本题以化学反应速率与化学平衡为素材,考查观察图象及其信息加工的能力。答题时要仔细地识图和析图,对速率与平衡的规律加以运用。)
2.(2000年广东高考题)用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )
A.加热 B.不用稀硫酸,改用98%浓硫酸 C.滴加少量硫酸铜溶液 D.不用铁片,改用铁粉
(该题旨在考查学生对影响化学反应速率因素的掌握情况。答题时要综合考虑多方面的因素,注意反应的本质。)
1.反应4A(s)+3B(g) 2C(g)+ D(g),经2min,B的浓度减少0.6mol/L。对此反应速率的表示正确的是( )
2C(g)+ D(g),经2min,B的浓度减少0.6mol/L。对此反应速率的表示正确的是( )
A.用A表示的反应速率是0.4 mol·(L·min)-1
B.分别用B、C、D表示的反应速率其比值是3:2:1
C.在2min末的反应速率,用B表示是0.3 mol·(L·min)-1
D.在这2min内用B和C表示的反应速率的值都是逐渐减小的
(本题考查学生对反应速率的理解及表示方法。答题时注意是用何种物质表示反应速率的,指的是平均速率还是瞬时速率。)
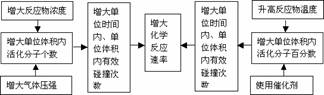
3.外界条件对反应速率的影响,可以概括为“加加、减减”四个字,即增加浓度、增加(升高)温度、增加压强、增加(使用正)催化剂,均可以增大化学反应速率;减小浓度、减小(降低)温度、减小压强、减小(使用负)催化剂,均可以减小化学反应速率。
典型题点击
2.影响化学反应速率的因素
(1)内因(主要因素):参加反应物质的性质。
 (2)同一化学反应的速率大小与外界条件(外因)有关。具体规律如下:
(2)同一化学反应的速率大小与外界条件(外因)有关。具体规律如下:
1.化学反应速率表示法
(1)意义:研究化学反应进行的快慢问题。
(2)表示方法:常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。单位:mol·(L·min)-1或mol·(L·s)-1。
(3)注意问题
①随着反应的进行,物质浓度不断变化,反应速率也不断变化,因此某一段时间的反应速率实际是平均速率,而不是瞬时速率。
②同一反应里,用不同物质表示的化学反应速率之比,等于它们在化学方程式中的化学计量数之比,也等于同一时间内各物质的浓度变化之比。表示化学反应速率时,应注明是用哪种物质表示的化学反应速率。
③化学反应速率在不同的时间间隔内不一定相等。
④对于没有达到化学平衡状态的可逆反应:v(正)≠v(逆)
14.在一个盛有催化剂、容积可变的密闭容器中,保持一定温度和压强,进行以下反应:N2+3H2 2NH3。已知加入1mol N2和4 molH2时,达到平衡后生成a mol NH3(见下表“已知”项)。在相同温度、压强下,保持平衡时各组分的体积分数不变。对下列编号①-③的状态,填写表中的空白。
2NH3。已知加入1mol N2和4 molH2时,达到平衡后生成a mol NH3(见下表“已知”项)。在相同温度、压强下,保持平衡时各组分的体积分数不变。对下列编号①-③的状态,填写表中的空白。
|
已知 编号 |
起始状态物质的量n/mol |
平衡时NH3的物质的量n/mol |
||
|
N2 |
H2 |
NH3 |
||
|
1 |
4 |
0 |
a |
|
|
① |
1.5 |
6 |
0 |
|
|
② |
|
|
1 |
0.5a |
|
③ |
m |
g(g≥4m) |
|
|
13.在10 ℃和2×105 Pa条件下,反应aA(g) dD(g)+eE(g)建立平衡后,再逐步增加体系的压强(保持温度不变)。下表列出不同压强 下反应建立平衡时物质D的浓度:
dD(g)+eE(g)建立平衡后,再逐步增加体系的压强(保持温度不变)。下表列出不同压强 下反应建立平衡时物质D的浓度:
|
压强/Pa |
2×105 |
5×105 |
1×106 |
|
D的浓度/mol·L-1 |
0.085 |
0.20 |
0.44 |
根据表中数据回答下列问题:
(1)压强2×105 Pa增加到5×105 Pa时,平衡向反应方向 移动(填“正”或“逆”),其理由是 。
(2)压强从5×105 Pa增加到1×106 Pa时,平衡向
反应方向移动(填“正”或“逆”),其理由是 。
11.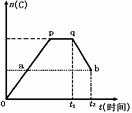 在一定温度下,对于反应2A(g)+B(g)
在一定温度下,对于反应2A(g)+B(g)  2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。试回答下列问题:
2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。试回答下列问题:
(1)p点反应的v正
v逆(填“>”、“<”或“=”)
(2)此反应的正反应为 热反应(填“放”或“吸”);
(3)a、b两点的正反应速率;va vb(填“>”、“<”或“=”)。
$
10.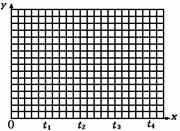
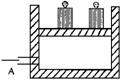 如图所示为一恒压容器。在恒定温度下,将1molN2和3molH2混合后由A口快速充入容器,封闭A,反应N2+3H2
如图所示为一恒压容器。在恒定温度下,将1molN2和3molH2混合后由A口快速充入容器,封闭A,反应N2+3H2 2NH3在t1时刻达到平衡,t2时刻再从A口快速充入一定量NH3,封闭A,t3重新达平衡至t4。请在图中画出0→t4时间内混合气中NH3的体积分数(y坐标)随时间(x坐标)变化的曲线。
2NH3在t1时刻达到平衡,t2时刻再从A口快速充入一定量NH3,封闭A,t3重新达平衡至t4。请在图中画出0→t4时间内混合气中NH3的体积分数(y坐标)随时间(x坐标)变化的曲线。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com