
题目列表(包括答案和解析)
10.a、b、c、d均为短周期元素,a的原子结构示意图为 ,元素b形成的
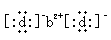
单质可以与CO2发生置换反应,原子序数b < c < a,b与d形成的化合物的电子式为 。下列比较中正确的是
A.原子半径c < d
B.四种元素在同一周期
C.气态氢化物的稳定性a < d
D.最高价氧化物对应的水化物的碱性b < c
9.下列说法不正确的是
A.等物质的量的 -CH3与-OH所含电子数相等
B.7.80 g Na2O2与5.85 g NaCl所含阴离子数相等
C.等质量的C2H4和C3H6中所含C-H键数目相等
D.等体积、等密度下的12C18O和14N2所含质子数相等
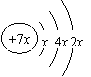
8.丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如下图所示,下列说法不正确的是
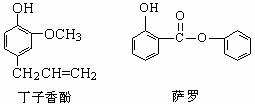
A.萨罗的分子式为C13H10O3
B.丁子香酚与浓溴水只发生取代反应
C.萨罗和丁子香酚均能发生氧化反应
D.丁子香酚和萨罗均能与氯化铁溶液发生显色反应
7.下列说法正确的是
A.35Cl2和37Cl2互为同位素
B.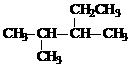 的名称为2,3-二甲基戊烷
的名称为2,3-二甲基戊烷
C.酸与碱发生中和反应而生成1 mol H2O的反应热叫做中和热
D.向鸡蛋白溶液中加入CuSO4溶液,有浑浊现象,该过程为盐析,属于物理变化
6.根据实验目的判断下列实验操作或装置正确的是
|
目的 |
实验室制O2 |
配制稀硫酸溶液 |
在铁制品上镀铜 |
净化、精制淀粉胶体 |
|
装置 或操作 |
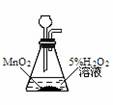 |
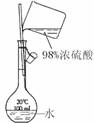 |
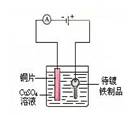 |
 |
|
选项 |
A |
B |
C |
D |
5.氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是
A.工业合成氨的过程是固氮的过程
B.自然界中,氨是动物体特别是蛋白质腐败后的产物
C.为防止粮食、罐头、水果等食品腐烂,常用氮气做保护气
D.在电闪雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收
25.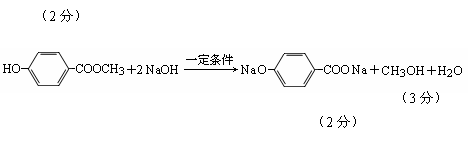 (15分)(其他合理答案参照本标准给分)
(15分)(其他合理答案参照本标准给分)
(1) ① cd
②
水解反应(取代反应)、中和反应(复分解反应)
 (2)
(2)
|
|||
|
|||
(3) ① 加成反应
 ②
②
|
|
|
 (1)N≡N
(1)N≡N
(2) ∶Cl∶P∶Cl∶ P(s)+3/2Cl2(g)=PCl3(l);△H= –306 kJ/mol
|
|
|
|
(4)Cl2、NH3
|
|
|
|
(2)NaOH和Na2CO3
|
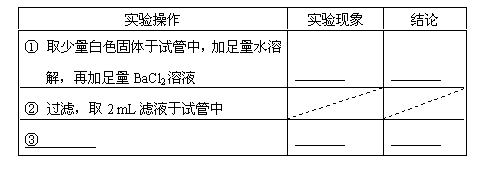
实验操作 |
实验现象 |
结论 |
|
① -- ③ 滴加酚酞 |
产生白色沉淀 溶液变红 |
有CO32-
有OH- |
|
|
|
|
HCO3–+NH3=NH4++CO32–
|
|
|
|
|
|
(3)洗涤 m(Fe2O3):m(Cu):m(SiO2)=3.2:2.88:3.0
5.A 6.B 7.C 8.B 9.D 10.A 11.C 12.D
28.(13分)某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验。

试回答:
(1)经I得到蓝色溶液,该过程中一定发生的化学反应是(用离子方程式表示)
、 。
(2)X中一定含有的物质是 。反应II的化学方程式是 。
(3)为进一步确定上述混合物X的成分,另取9.08 g X进行如下实验。
① 加入足量的NaOH溶液,过滤,将滤渣在氮气气流中干燥得固体m g。
② 向滤渣中加入过量盐酸,过滤,将滤渣在氮气气流中干燥得固体n g。
由于缺少某步操作,使得测定的质量m、n均偏高。
③ 按正确步骤重新进行实验后得到m=6.08 g,n=1.6 g。
则所缺少的步骤是______。原混合物中各成分的质量之比是 。(不必化简)
27.(17分)纯碱、烧碱等是重要的化工原料。
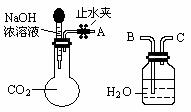 (1)利用如图所示装置可间接证明二氧化碳与烧碱
溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 ,反应的离子方程式是________。若其它操作不变,将A与C连接,可观察到的现象是 。
(1)利用如图所示装置可间接证明二氧化碳与烧碱
溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 ,反应的离子方程式是________。若其它操作不变,将A与C连接,可观察到的现象是 。
(2)向100 mL2 mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3 g白色固体,该白色固体的组成是 (写化学式)。
设计实验确认该白色固体中存在的阴离子,试完成下列方案。
(3)现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
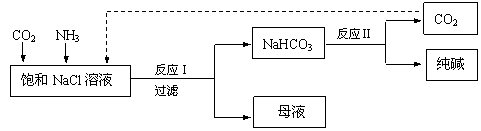
|
NaCl+CO2+NH3+H2O====NaHCO3↓+NH4Cl,处理母液的两种方法如下。
① 向母液中加入石灰乳,可将其中 循环利用,同时得到融雪剂 。
② 向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。
试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com