
题目列表(包括答案和解析)
7.通过复习总结,你认为下列对化学知识概括合理的一组是( )
①能与酸反应的氧化物,一定是碱性氧化物
②一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
③原子晶体、离子品体、金属晶体、分子晶体中都一定存在化学键
④原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低
⑤在熔化状态和水溶液中均不能导电的物质称为非电解质
⑥NF3的沸点比NH3的沸点低是因为N-F比N-H键单键键能大
A.只有①② B.只有③④ C.只有④ D.只有⑤⑥
6.2008年北京奥运会开幕式的焰火:“脚印”、“笑脸”、“五环”,给世界各国留下深刻印象。其主要原料是黑火药,还有草酸钠、碳酸铜(发出绿色的光)等发色剂和氯酸钾、
镁铝金属粉末等添加剂。据此判断下列说法正确的是 ( )
A.碳酸铜因为受热分解才发出绿色的光
B.氯酸钾的主要用途是产生紫色的焰火
C.焰火的产生与原子核外电子发生跃迁释放能量有关
D.黑火药的主要成分是木炭、硫磺
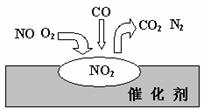
5.在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法错误的是( )
A.NO2是该过程的中间产物
B.NO和O2必须在催化剂表面才能反应
C.汽车尾气的主要污染成分包括CO和NO
D.催化转化总反应为:2NO+O2+4CO  4CO2+N2
4CO2+N2
4. 短周期元素A、B、C原子序数依次增大,A3-与B2-、
短周期元素A、B、C原子序数依次增大,A3-与B2-、
C+电子层结构相同。则下列说法中不正确的是( )
A.三种元素可组成CAB2和CAB3型化合物 B.原子半径:A>B>C
C.H2B在同主族元素气态氢化物中最稳定 D.B的某种单质可用于杀菌消毒
3.阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定错误的是( )
A.16.9 g 过氧化钡(BaO2)固体中阴、阳离子总数约为0.2×6.02×1023
B.2.3 g 钠被O2完全氧化时,失去电子数约为0.1×6.02×1023
C.0.5 mol超重水(T2O)的质子总数约为5×6.02×1023
D.8.96 LNH3中N-H键的物质的量为1.2×6.02×1023
2.乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,通过乙醇制取氢气具有良好的应用前景。已知通过乙醇制取氢气有如下两条路线:
a. 水蒸气催化重整:CH3CH2OH(g) + H2O(g) ® 4H2(g) + 2CO(g) △H=+255.58 kJ·mol-1
b. 部分催化氧化:CH3CH2OH(g)
+ 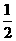 O2(g) ®
3H2(g) + 2CO(g) △H=+13.76 kJ·mol-1
O2(g) ®
3H2(g) + 2CO(g) △H=+13.76 kJ·mol-1
则下列说法错误的是( )
A.从原料消耗的角度来看,a路线制氢更有价值
B.从能量消耗的角度来看,b路线制氢更加有利
C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大.
D.降低温度,可提高b路线中乙醇的转化率
1.下列叙述正确的是( )
A.合成氨工业、硫酸工业中均用到吸收塔这一设备
B.玻璃、水泥的工业生产中均用到纯碱和石灰石作为原料
C.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅
D.绿色化学的核心思想是利用绿色植物治理环境污染
20.设NA表示阿伏加德罗常数,下列说法中不正确的是b
A.一定量的Fe与含1mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA
B.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
C.0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA
D.10mL5mol/L(NH4)2SO4溶液中含有NH4+数目小于0.1NA个

19.NA表示阿伏加德罗常数,下列说法中正确的是( c )
A.3.6 g重氧水(H218O)中所含质子数为2NA
B.4.48 L N2所含分子数为0.2 NA
C.12g金刚石中含有C-C键的个数为2NA
D.1 mol氧气与足量钠点燃反应,转移4NA个电子
18.设NA表示阿伏加德罗常数,下列说法正确的是 ( B )
A.1mol氯气参加氧化还原反应,转移的电子数一定为2 NA
B.标准状况下,以任意比混和的氢气和一氧化碳气体共8.96L,在足量氧气中充分燃烧
时消耗氧气的分子数为0.2 NA
C.1mol/LCuCl2溶液中含有的Cl-的个数为2NA
D.25℃,1.01×105Pa时,1mol氧气所含的原子数为NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com