
题目列表(包括答案和解析)
5.(浙江09届海宁市高三9月模拟)分子式为C12H14O2的F有机物广泛用于香精的调香剂。
 已知:
已知:
① R-CH2X + NaOH R-CH2OH + NaCl (X代表卤素原子)
②
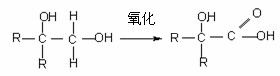
为了合成该物,某实验室的科技人员设计了下列合成路线:
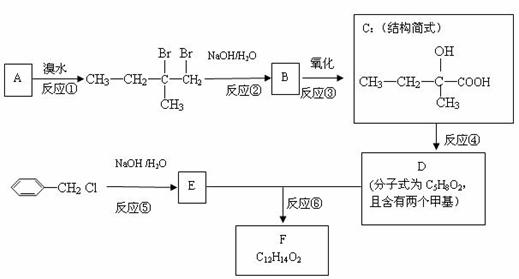
试回答下列问题:
(1)A物质在核磁共振氢谱中能呈现 种峰;
C物质的官能团名称_______________;E物质的结构简式________________;
(2)上述合成路线中属于取代反应的是 (填编号);
(3)反应④的化学方程式为 ;
(4)写出E属于芳香族化合物所有的同分异构体 。
4. (河南平顶山市09届高三第一次质量检测) 已知:
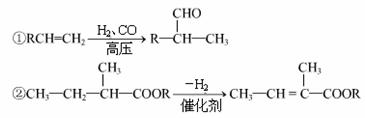
有机物A-F中,A 是链烃,A 与 H2 加成得到烷烃,经测定,该烷烃分子中只有两个-CH3, 其一卤代物有两种同分异构体,C 与X 反应生成D。各物质之间的转化关系如下图所示:
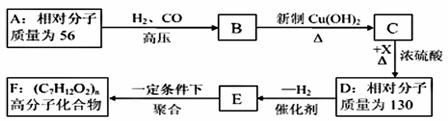
(1)写出 X的结构简式: 。
(2)写出化合物 A、E 的结构简式:A ,E 。
(3)指出下列反应的类型:C→D ,E→F 。
(4)写出 B与足量新制氢氧化铜悬浊液共热时发生反应的化学方程式: 。
 (5)有机物G是有机物C不同类型的同分异构体,并且G能与金属钠发生反应放出无色气体, 又能发生银镜反应;又知G的同一类型的同分异构体共有多种,则其中只含有一个甲基的同分异构体的结构简式有
(5)有机物G是有机物C不同类型的同分异构体,并且G能与金属钠发生反应放出无色气体, 又能发生银镜反应;又知G的同一类型的同分异构体共有多种,则其中只含有一个甲基的同分异构体的结构简式有
、 、 。
3.(09福建卷31)  有机物A是最常用的食用油氧化剂,分子式为C10H12O5,可发生如下转化:
有机物A是最常用的食用油氧化剂,分子式为C10H12O5,可发生如下转化:

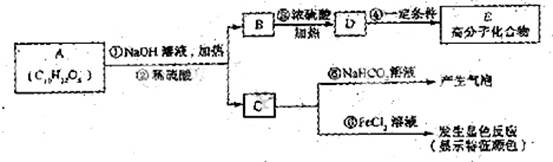


 已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为:
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为:


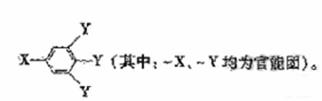
 请回答下列问题:
请回答下列问题:
 (1)根据系统命名法,B的名称为
。
(1)根据系统命名法,B的名称为
。
 (2)官能团-X的名称为
,高聚物E的链节为
。
(2)官能团-X的名称为
,高聚物E的链节为
。
 (3)A的结构简式为
。
(3)A的结构简式为
。
 (4)反应⑤的化学方程式为
。
(4)反应⑤的化学方程式为
。
 (5)C有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式
。
(5)C有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式
。
 i.含有苯环
ii.能发生银镜反应 iii.不能发生水解反应
i.含有苯环
ii.能发生银镜反应 iii.不能发生水解反应
 (6)从分子结构上看,A具有抗氧化作用的主要原因是
(填序号)。
(6)从分子结构上看,A具有抗氧化作用的主要原因是
(填序号)。
 a.含有苯环
b.含有羰基
c.含有酚羟基
a.含有苯环
b.含有羰基
c.含有酚羟基
2. (河北唐山市2008-2009学年度高三年级摸底考试)有机化合物A为一元溴代有机酸,仅含C、H、O、Br元素,与A相关的反应框图如下:
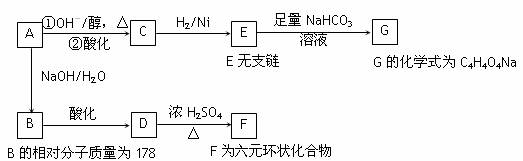
⑴写出下列反应的有机反应类型:
A→C中是_______反应,C→E是_________反应。
⑵写出F的结构简式:_______________________________________。
⑶写出与C具有相同官能团的同分异构体的结构简式__________________________。
⑷写出下列反应的化学方程式A→B:_______________________________________________。
17.(2008佛山)某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
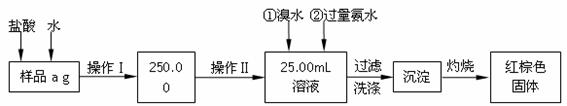
请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 ,(填仪器名称)
操作II必须用到的仪器是 。(填编号)
A.50mL烧杯 B.50mL量筒 C.100mL量筒 D.25mL滴定管
(2)请写出加入溴水发生的离子反应方程式 ,
加入氨水要过量的原因是 。
(3)检验沉淀是否已经洗涤干净的操作是 。
 (4)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3g,则接下来还应进行的操作是
(4)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3g,则接下来还应进行的操作是
。
(5)若蒸发皿质量是W1 g,蒸发皿与加热后固体总质量是W2 g,则样品中铁元素的质量分数是 (列出原始算式,不需化简);若称量准确,最终测量的结果偏大,则造成误差的原因可能是 (写出一种原因即可)。

16.(山东诸城一中2009届高三年级阶段性评估)某兴趣小组同学共同设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质。请回答下列问题:
 (1)利用装置I制取某些气体,制取气体的反应所具有的特点是___________________。
(1)利用装置I制取某些气体,制取气体的反应所具有的特点是___________________。
(2)利用装置Ⅰ、II制取气体(K2关闭,K1打开)。甲同学认为:利用装置Ⅱ可以收集H2、NH3等气体,但不能收集O2和NO,理由是
。
乙同学认为:利用装置II作简易改进(不改变仪器装置),可收集NO、O2,改进的方法是__________________ 。
丙学认为:利用装置II作简易改进(改变仪器装置),可收集NO2气体,改进的方法是_______________________ 。
(3)利用装置I、Ⅲ
验证物质的性质(K2打开,K1关闭)。如设计实验证明氧化性:KMnO4>Cl2>Br2,则在A中加浓盐酸,B中加________ __,C中加______________ ,观察到C中的现象是___________________ 
15. (福建省漳州市芗城中学2009届高三一轮复习单元测试)实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液。 应量取盐酸体积_______mL ,应选用容量瓶的规格_________mL。 除容量瓶外还需要的其它仪器_________________________________。
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)____________________
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(3) 操作A中,将洗涤液都移入容量瓶,其目的是
。溶液注入容量瓶前需恢复到室温,这是因为
。
(4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响)?
 a.没有进行A操作__________ ;b.加蒸馏水时不慎超过了刻度________ ;c.定容时俯视____________。
a.没有进行A操作__________ ;b.加蒸馏水时不慎超过了刻度________ ;c.定容时俯视____________。
(5)若实验过程中出现如下情况如何处理?
加蒸馏水时不慎超过了刻度 ? __________________。
向容量瓶中转移溶液时(实验步骤B) 不慎有液滴掉在容量瓶外? _______ _______。
14. (江苏省江安中学2009届高三年级第三次月考)奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是:食品与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
操作步骤:
(1)样品处理:准确称取一定量的固体样品奶粉,移入干燥的凯氏烧瓶中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
(2)NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸氨,再经过再经过碱化蒸馏后,氨即成为游离状态,游离氨经硼酸吸收。
 (3)氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,从消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
(3)氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,从消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水?
。
 (2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
A.凯氏烧瓶中溶液转移移到容量瓶中时,未洗涤凯氏烧瓶
B.定容时,俯视刻度线
C.定容时,仰视刻度线
D.移液时,有少量液体溅出
(3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3。
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。则三聚氰胺中氮的含量为

13.(山东济宁市2008-2009学年度第一学期高三质量检测)化学是一门以实验为基础的自然科学,进行化学实验时要采取正确的实验操作,注意实验安全:
(1)在盛放浓硫酸的试剂瓶的标签上印有如图所示警示标志,说明浓硫酸是一种 。
(2)下列有关实验操作和安全事故处理错误的有 。
a.使用水银温度计测量烧杯中水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的瓶中,残破的温度计插入装有硫粉的广口瓶中
b.用试管夹从试管底由下往上夹住距管口约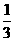 处,手持试管夹长柄进行加热
处,手持试管夹长柄进行加热
c.把用氯酸钾制氧气后的残渣倒入垃圾桶
d.给盛有液体的烧瓶加热时,需加碎瓷片或沸石
e.配制硫酸溶液时,在量筒中加入一定体积的水,再边搅拌边慢慢加入浓硫酸
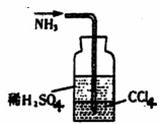
f.用图所示装置吸收氨气
12. (肇庆市中小学教学目标管理2007届高中毕业班第二次统检测)某同学用Na2CO3配制0.10mol·L-1Na2CO3(aq)的过程如下图所示。你认为该同学的错误有
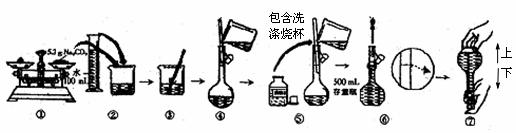
A.①⑤⑥ B.②④⑦ C.①⑥⑦ D.⑤⑥⑦
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com