
题目列表(包括答案和解析)
8.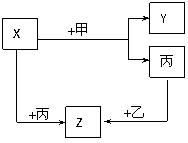 (07年娄、邵八校联考)甲、乙、丙是三种常见的单质,X、Y、Z是它们的化合物,它们之间有如右图所示的转化关系:
(07年娄、邵八校联考)甲、乙、丙是三种常见的单质,X、Y、Z是它们的化合物,它们之间有如右图所示的转化关系:
(1)若甲是具有还原性的金属单质,X、Y、Z中
有一种是离子晶体,试推断:
①X、Y、Z中含有丙元素的是 ;
②写出Y的电子式 ;
③写出X与甲反应的化学方程式,并标出电子
 转移的方向和数目:
转移的方向和数目:
。 (2)若甲是具有氧化性的黄绿色气体单质,丙通常是暗红色的液体,Y和Z具有相同的阳
离子,X与Z含有相同的离子。
①写出乙物质的化学试 ;
 ②写出X与足量的甲在溶液中完全反应的离子方程式:
。
②写出X与足量的甲在溶液中完全反应的离子方程式:
。
7.(07年常州模拟) A、B、C、D、E、F六种中学常见的物质,皆由短周期元素组成,有转化关系:
 (1)若A、C、E皆为氧化物,且常温下A为无色液体,E为有毒气。B、D、F皆为非金属单质,且D为气体。则A的结构式为
, 1molC中含有
个共价键。
(1)若A、C、E皆为氧化物,且常温下A为无色液体,E为有毒气。B、D、F皆为非金属单质,且D为气体。则A的结构式为
, 1molC中含有
个共价键。
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中C的相对分子质量最小;D、E、F皆为氧化物, 其中D、F为有毒气体。则
①A、C、E沸点由高到低的顺序为 (填化学式)。
②A跟D常温下反应可生成一种单质,化学方程式为 。
6.下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体其余均为气体。根据图中关系推断:
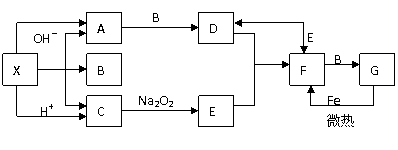
(1)化学式X ;A ;B ;
(2)写出C→E的化学反应方程式 ;
(3)实验室收集气体D和F的方法依次是 法和 法。
5.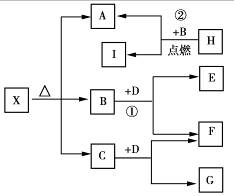 已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有右图所示的关系。
已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有右图所示的关系。
试回答下列问题:
 (1)G的化学式为:_______________。
(1)G的化学式为:_______________。
(2)写出下列反应的化学方程式
①__________________________________
②_________________________________。
 (3)X在医药上用作解酸剂,与盐酸作用时,生
(3)X在医药上用作解酸剂,与盐酸作用时,生
成B的物质的量与消耗盐酸的物质的量之比
为3∶8,则X的化学式为:_____________;
X与盐酸反应的化学方程式为:_____________________________________。
4.(07年重庆高考理综)a、b、c、d、e是短周期元素,周期表中a与b、b与c相邻;a与c的最外层电子数之比为2:3,b的最外层电子数比c的最外层电子数少1个;常见化合物d2c2与水反应生成c的单质,且溶液使酚酞试液变红。
(1)e的元素符号是
(2)a、b、c的氢化物稳定性顺序为(用分子式表示) ;b的氢化物和b的最高价氧化物的水化物反应生成Z,则Z中的化学键类型为 ,Z的晶体类型为 ;ab- 离子的电子式为
(3)由a、c、d形成的化合物的水溶液显碱性,其原因是(用离子方程式表示)
(4)一定量的d2c2与ac2反应后的固体物质,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol 气体。则用物质的量表示该固体物质的组成为 、 .
3.(08年永州模拟)一部分。表中所列的字母分别代表某一元素。

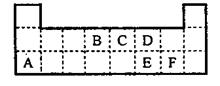
(1)1molA与D的氢化物完全反应产生的气体在标准状况下的体积为 。
(2)写出B的最高价氧化物的电子式 。
(3)表中的另一种金属元素(未标出)的单质G,可以发生如下图所示转化
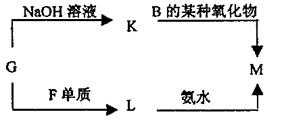
其中化合物M是一种白色胶状沉淀,则M的化学式为 ;
K的溶液与B的某种氧化物反应的化学方程式为 ;L与氨水反应的离子方程式为 ; 一种新型无机非金属材料由G元素和C元素组成,其化学式为 。
2.(08年北京高考)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。

请回答:
(1)W的电子式是 。
(2)X与Y在溶液中反应的离子方程式是 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
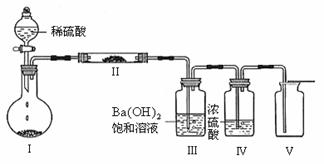
①装置Ⅰ中反应的化学方程式是
,
装置Ⅱ中物质的化学式是 。
②用X含有的四种元素中的两种
 组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 (从上图中选择必要装置,填写编号)。
组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 (从上图中选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是 。
1.(09年岳阳模拟)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种.现利用另一种溶液X,用如下图所示的方法,即可将它们一一确定.试确定A、B、C、D、X各代表何种溶液.



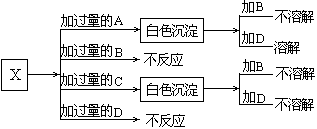 A: B: C: D: X:
A: B: C: D: X:
19.(每空2分,共8分)
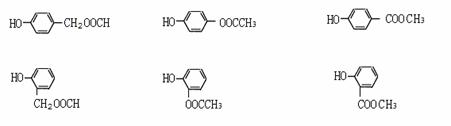
(1)C8H8O3

(2)
(3)(写出两种即可,答案合理均给分)
 20(1)空气或氧气(2分)
(2)甲醇(1分) 铜粉(铜网)(1分) 水(1分)(3)A B(2分)
20(1)空气或氧气(2分)
(2)甲醇(1分) 铜粉(铜网)(1分) 水(1分)(3)A B(2分)
(4)③②①⑨⑥⑤⑧或③①②⑨⑥⑤⑧(2分)
(5)甲醇自身分子间可形成氢键,形成缔合分子,因此甲醇的沸点较高(2分) 甲醇和甲醛均可以和水形成氢键,故两者在水中的溶解度较大(2分)
18. (10分)
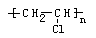 (1)(2分)
(1)(2分)
(2) 羧基 (2分)
(3) 酯化(或取代)反应 (2分)
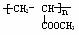
 (4) n CH2==CH-COOCH3
(4) n CH2==CH-COOCH3
(5) 216g (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com