
题目列表(包括答案和解析)
20.⑴Cl O ⑵KClO3
讲析:据化合价可知X为第IA族元素,Y为第VIIA族元素;
 再根据Z元素原子核内质子数比Y元素原子核内质子数少9个,推测Y为Cl,Z为O;最后以ClO3-的电子总数为42验证此答案符合题意。
再根据Z元素原子核内质子数比Y元素原子核内质子数少9个,推测Y为Cl,Z为O;最后以ClO3-的电子总数为42验证此答案符合题意。
19.⑴I Na Cl ⑵Na2O Na2O2 Na2O+H2O==2NaOH
2Na2O2+2H2O==4NaOH+O2↑ ⑶置换 Cl2+2I-==2Cl-+I2
讲析:X为第VA族元素推知为I;据Y的氧化物的特性大胆假设A为Na,再根据计算验证之;Z为第VIIA族元素,根据性质推知为Cl。
18. A原子中存在原子核,它占原子中极小体积
B 原子核带正电荷,且电荷数远大于α-粒子
C金的原子核质量远大于α-粒子
17.⑴N2H4 ⑵ ⑶22 ⑷CO2、N2O、BeF2
讲析:⑴N2H4+ +OH- = N2H4 + H2O ⑵电子式的书写模仿NH4+ ⑶
N3-的电子总数=7╳3+1=22⑷以N原子为中心分析讨论。
16. ⑴ ⑵ 六 ⅢA
(3)-1,+1,+2,+3。
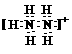 讲析:⑴由题给信息推知最外层最多容纳的电子数为4个,次外层最多容纳的电子数为9个,倒数第三层最多不超过16个电子。
讲析:⑴由题给信息推知最外层最多容纳的电子数为4个,次外层最多容纳的电子数为9个,倒数第三层最多不超过16个电子。
12.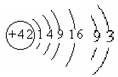 本题计算得到的相对原子质量是同位素的相对原子质量,另外本题表达时要考虑单位。 13.据化学方程式推知生成的氯气中n(35Cl):n(37Cl)=5:1,经计算选项C符合题意。 14.讨论得:H与Be、H与Al、He与C、He与S共四组。 15.由 2个u夸克和1个d夸克组成的微粒所带电量为e,即与质子的电量相同;由1个u夸克和2个d夸克组成的微粒不带电,即与中子吻合。
本题计算得到的相对原子质量是同位素的相对原子质量,另外本题表达时要考虑单位。 13.据化学方程式推知生成的氯气中n(35Cl):n(37Cl)=5:1,经计算选项C符合题意。 14.讨论得:H与Be、H与Al、He与C、He与S共四组。 15.由 2个u夸克和1个d夸克组成的微粒所带电量为e,即与质子的电量相同;由1个u夸克和2个d夸克组成的微粒不带电,即与中子吻合。
13.C 14.D 15.B
讲析:4.X1和X2可能是同位素原子,也可能是同一元素不同原子形成的离子。 6.如果BxHyz-中x=12,y=12时,z一定为2才能满足题目要求,所以选项D符合题意。 7.据R的原子结构特征讨论推知为Si。 10.X为N,Y为Mg。
1.B 2.B 3.B 4.AC 5.D 6.D 7.A 8.BC 9.B 10.AC 11.B 12.BD
4.⑴Ar ⑵S2- ⑶K+ ⑷Cl- 讲析:本题以符合题意的原子Ar为中心,再根据微粒的化学性质和结构特点选择微粒。
检测提高
1.A 2.BD 3.A
讲析:1.R2+离子的质子数为(A-N),氧化物的化学式为RO,摩尔质量为(A+16)g/mol,所以选项A符合题意。 2.若某元素有两种核素aX、bX,则构成的双原子单质分子有
三种。若a〈b,则2a=158,2b=162,求得两种核素的质量数分别为79、81。 3.据电子层结构特征推知X为第IA族元素,Y为P,Z为O,再据化合价法则分析选项得出结论。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com