
题目列表(包括答案和解析)
1.C 2.D 3.A 4.A 5.D 6.C 7.BD
4.当m:n=4.5时,溶质为Fe(NO3)3。
当m:n=3时,溶质为Fe(NO3)2。
当3<m:n<4.5时,溶质为Fe(NO3)3和Fe(NO3)2
新活题网站
3.⑴x=3;⑵3BrF3 +5H2O=HBrO3+9HF+Br2+O2↑, ⑶氧化剂是BrF3,还原剂是H2O和BrF3。
讲析:由于HBrO3、O2和Br2前的系数已定,根据的氢元素守恒可知3x=(5×2-1)=9,x=3。因此:⑴x=3;⑵3BrF3 +5H2O=HBrO3+9HF+Br2+O2↑, ⑶氧化剂是BrF3,还原剂是H2O和BrF3。
2.(1)被氧化的是C元素;
 (2)
(2)
(3)设至少需要液氯质量为x。
 根据⑴⑵两个方程式,可得总关系式:
根据⑴⑵两个方程式,可得总关系式:
2KCN ~ 5Cl2
2×65 5×71
20×0.65g x
x=35.5g
即至少需要液氯35.5g。
1.B
23.将10g铁粉置于40mL HNO3溶液中,微热,反应过程中随着硝酸浓度的降低,生成气体的颜色由红棕色逐渐变为无色,充分反应后共收集到1.792L标准状况下的混合气体(NO2、NO),溶液里还残留4.4g固体。
(1)求该反应中被还原的硝酸与未被还原的硝酸的质量比。
(2)求理论上原硝酸的物质的量浓度。
(3)求混合气体中NO2、NO的体积比。
(4)写出上述反应的总的化学方程式。

第3课时 (A卷)
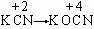 典型题点击
典型题点击
22.将铝放入烧碱溶液中,若反应过程中有0.5mol电子转移,求:(1)参加反应的水的物质的量为多少?
(2)生成水的物质的量为多少?
(3)反应总耗水的物质的量为多少?
21.在一定条件下,NO跟NH3可以发生反应生成N2和H2O。现有NO和NH3的混合物1mol,充分反应后所得产物中,若经还原得到的N2比经氧化得到N2多1.4g。
(1)写出反应的化学方程式并标出电子转移的方向和数目。
(2)若以上反应进行完全,试计算原反应混合物中NO与NH3的物质的量可能各是多少。
20.亚硫酸钠和碘酸钾在酸性溶液里反应的化学方程式是 Na2SO3+KIO3+H2SO4→Na2SO4+K2SO4+I2+H2O(未配平)
(1)其中氧化剂是 ,若反应中有5 mol电子转移,则生成的碘的物质的量为 mol。
(2) 该反应过程和机理复杂,一般认为分以下几步:
①IO3-+SO32-→ IO2-+SO42-(反应慢)
②IO2-+2SO32-→ I-+2SO42-(反应快)
③5I -+6H++IO3-→ 3I2+3H2O(反应快)
 ④I2+SO32-+H2O→
2I-+SO42-+2H+(反应快)
④I2+SO32-+H2O→
2I-+SO42-+2H+(反应快)
根据上述条件推测,此反应速率由 步反应决定。(填序号)
(3)若预先加入淀粉溶液,由反应过程看,必在 离子消耗完时才会有使淀粉变蓝的现象产生,原因是
。
19.已知几种离子的还原能力强弱顺序为I->Fe2+>Br-,现有200mL混合溶液中含FeI2、FeBr2各0.10mol,向其中逐滴滴入氯水(假定Cl2分子只与溶质离子反应,不考虑其它反应)
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是 ,剩余Fe2+的物质的量为 。
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为 ,若最终所得溶液为400mL,其中主要阳离子及其物质的量浓度为 。
(3)通过对上述反应的分析,试判断Cl2、I2、Fe3+、Br2四种氧化剂的氧化能力由强到弱的顺序是 。
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式 ,
上述所有反应共消耗Cl2 mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com