
题目列表(包括答案和解析)
9. 在固定容积的密闭容器中,可逆反应2X+Y(g)
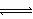 Z(s)已达到平衡,此时升高温度则气体混合物的密度增大。下列叙述正确的是( )
Z(s)已达到平衡,此时升高温度则气体混合物的密度增大。下列叙述正确的是( )
A.若X为非气态,则正反应为吸热反应
B.正反应为放热反应,X一定为气态
C.正反应为放热反应,X可能是气态、液态或固态
D.若加入少量的Z,该平衡向左移动
8. 在一定条件下,将3 molA和1
molB两种气体混合于固定容积为2 L的密闭容器中,发生如下反应: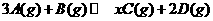 。
2 min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol·L
。
2 min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol·L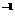 下列判断正确的是( )
下列判断正确的是( )
A.平衡常数约为0.3
B.B的转化率为60%
C.A的平均反应速率为0.3mol·(L·min)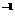

D.若混合气体的密度不变则表明该反应达到平衡状态
7. 对于反应2A(g)+B(g)
对于反应2A(g)+B(g) 2C(g),△H =- a kJ/mol ,(a>0)下列判断正确的是
2C(g),△H =- a kJ/mol ,(a>0)下列判断正确的是
A.2体积A和足量B反应,必定生成2体积C,放出a KJ热量
B.若反应容器的容积和温度不变,增大压强,平衡必定向右移动
C.平衡时,A消耗速度必定等于B生成速度的两倍
 D.平衡时,A浓度必定等于B浓度的两倍
D.平衡时,A浓度必定等于B浓度的两倍
6. 高温下,某反应达平衡,平街常数
高温下,某反应达平衡,平街常数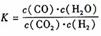 恒容时,温度升高.H2浓度减小。下列说法正确的是
恒容时,温度升高.H2浓度减小。下列说法正确的是
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应化学方程式为
5. 某可逆反应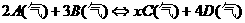 ,若按下列两种配比
,若按下列两种配比
(1)0.8molA 1.2molB 1.2molC 2.4molD
(2)1.4molA 2.1molB 0.6molC 1.2molD
将它们放入一容积不变的密闭容器中,保持温度不变,达平衡后C的质量分数仍相等,则化学反应方程式中x的值为( )
A、2 B、3 C、4 D、1
4. 在一定温度下,将CO和水蒸汽各1mol放在密闭容器中反应:
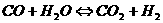 ,达平衡后测得
,达平衡后测得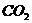 为0.6mol,再通入4mol水蒸汽,达新的平衡后,
为0.6mol,再通入4mol水蒸汽,达新的平衡后,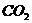 物质的量( )
物质的量( )
A等于0.6mol B等于1mol
C大于0.6mol,小于1mol D大于1mol
3.
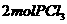 和
和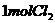 充入一容积不变的密闭容器中,在一定条件下反应
充入一容积不变的密闭容器中,在一定条件下反应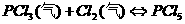 (气)达平衡时,
(气)达平衡时, 为0.4mol,此时若移走
为0.4mol,此时若移走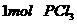 和
和 在相同温度下达平衡时
在相同温度下达平衡时 的物质的量是( )
的物质的量是( )
A 0.4mol B0.2mol
C小于0.2mol D大于0.2mol而小于0.4mol
2. 将气体A、B置于容积为2L的密闭容器中,发生如下反应:4A(g)+B(g)=2C(g),反应进行到4s末,测得A为0.5mol,B为0.4mol,C为0.2mol,用反应物浓度的减少来表示该反应的速率可能为( )
将气体A、B置于容积为2L的密闭容器中,发生如下反应:4A(g)+B(g)=2C(g),反应进行到4s末,测得A为0.5mol,B为0.4mol,C为0.2mol,用反应物浓度的减少来表示该反应的速率可能为( )
A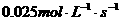
B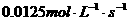
C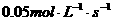
D
1. 已知 若反应速率分别用
若反应速率分别用 、
、
 表示,则正确的关系是( )
表示,则正确的关系是( )


25. 某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)

(1)装置B中发生反应的化学方程式是 。
(2)装置E中的现象是 。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法:
(4)该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
滤液→FeCl3溶液→FeCl3·6H2O晶体
①步骤I中通入Cl2的作用是 。
②步骤II从FeCl3稀溶液中得到FeCl3·6H2O晶体的主要操作包括: 。
③该流程中需保持盐酸过量,主要原因是(结合离子方程式简要说明) 。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com