
题目列表(包括答案和解析)
9.一定量的Cu粉与浓硫酸共热产生二氧化硫气体的体积为2.24L(标准状况),则下列情况不可能的是 ( )
A.加入铜的质量为6.4g B.加入浓硫酸中溶质0.2mol
C.加入铜的质量大于6.4g D.加入浓硫酸中含溶质多于0.2mol
lO.单质钛的机械强度高,抗蚀能力强,有“未来金属”之称。工业上常用硫酸分解钛铁矿(FeTiO3)的方法制取二氧化钛,再由二氧化钛制金属钛, 主要反应有: ( )
①FeTi03+3H2SO4=Ti(SO4)2+FeSO4+3H2O ②Ti(SO4)2+3H2O=H2TiO3↓+2H2SO4
 ③H2TiO3
③H2TiO3  TiO2+H2O ④TiO2+2C+2Cl2
TiO2+H2O ④TiO2+2C+2Cl2  TiCl4↑+CO↑
TiCl4↑+CO↑
⑤TiCl4+2Mg  2MgCl2+Ti
2MgCl2+Ti
下列叙述错误的是 ( )
A.反应①属于非氧化还原反应 B.反应②是水解反应
C.反应④中二氧化钛是氧化剂 D.反应⑤表现了金属镁还原性比金属钛强
8.制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应2FeC13+Cu=2FeCl2+CuCl2向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A.烧杯中有铜无铁 B.烧杯中有铁无铜
C.烧杯中铁、铜都有 D.烧杯中铁、铜都无
7.我国古代制得的“药金”外观和金相似,常被误认为是金子。冶炼方法是:将炉甘石(ZnCO3)和赤铜矿(Cu2O)与木炭按一定比例混合,加热至800℃左右,即炼出闪着似金子般光泽的“药金”。有关叙述正确的是
①“药金”是铜锌合金 ②冶炼过程中炉甘石直接被碳还原而有锌生成 ③用火焰灼烧可区分黄金与“药金”④用王水可以区分黄金与“药金”⑤表面有黑色氧化物的“药金”,用稀硫酸洗涤后可去掉黑色膜,但可能发出铜红色
A.①② B.①②③④ C.①③④⑤ D.①②③④⑤
6.重金属离子有毒性。实验室有甲、乙两种废液,均有一定毒性。甲废液经化验呈碱性,主要有毒离子为Ba2+,如将甲、乙两废液按一定比例混合,毒性明显降低。乙废液中可能含有的离子是 ( )
A.Cu2+和SO42- B.Cu2+和Cl- C.K+和SO42- D.Ag+和NO3-
5.已知铍(Be)的原子序数为4。下列对铍及其化合物的叙述中,正确的是
A.铍的原子半径小于硼的原子半径 B.氯化铍分子中铍原子的最外层电子数是8
C.氢氧化铍的碱性比氢氧化钙弱 D.单质铍跟冷水反应产生氢气
4.制备卤磷酸钙荧光粉所用的高纯氯化钙中混有镁杂质,除去的方法是把氯化钙的水溶液加热到90-95℃,在不断搅拌下加入适当的沉淀剂,使镁生成沉淀过滤除去。此沉淀剂最好选用 ( )
A.氢氧化钙乳浆 B.碳酸钠溶液 C.碳酸氢钠溶液 D.氢氧化钠溶液
3.定向爆破建筑物时,应同时定向切断钢筋和炸碎水泥,除要用适宜的猛烈炸药外,还需用 ( )
A.氧炔焰 B.铝热剂 C.液氧 D.电弧
2.下列灭火剂能用于扑灭金属钠着火的是
A.干冰灭火剂 B.黄沙 C.干粉灭火剂(含NaHC03) D.泡沫灭火剂
1.微量元素是指在人体内总含量不到万分之一,重量总和不到人体重量的千分之一的20多种元素,这些元素对人体正常代谢和健康起着重要作用,下列各组元素全部属于微量元素的是 ( )
A.Na,K,Cl,S,O B.F,I,Fe,Zn,Cu
C.N,H,0,P,C D.Ge,Se,Ca,Mg,C
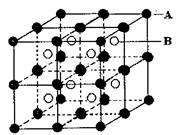
14.(山东省淄博市09届高三检测题)(1)由A、B两元素组成的离子晶体结构(甲)如图所示,则该晶体的化学式是: 。
 (2)C原子的最外层电子排布为nsnnpm,其某一激发态可使这两个亚层的每一个轨道都处于充满状态,1个C原子与2个D原子结合,使双方都达到8电子稳定结构。则在C与D形成的分子中,C原
(2)C原子的最外层电子排布为nsnnpm,其某一激发态可使这两个亚层的每一个轨道都处于充满状态,1个C原子与2个D原子结合,使双方都达到8电子稳定结构。则在C与D形成的分子中,C原
子发生轨道的杂化方式是 ,分子构型是 ,从成键方式看,该分子中含有的共价键的类型和数目分别是 。
 (3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙 甲,其原因是
(3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙 甲,其原因是
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com