
题目列表(包括答案和解析)
13、X、Y、Z、W四种短周期主族元素的最外层电子数之和为20。在周期表中X与Y、Z、W紧密相邻,X、Y两元素的原子序数之和等于Z元素的原子序数。下列说法正确的是( )
A.原子序数:Z>Y>X>W
B.X、Y、Z、W形成的单质最多有6种
C.X元素最高价氧化物对应水化物的化学式为:H3XO4
D.四种元素的气态氢化物中,W的气态氢化物最稳定
12.市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li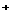 的高分子材料。这种锂离子电池的电池反应为:
的高分子材料。这种锂离子电池的电池反应为:
Li+2Li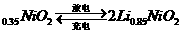
下列说法不正确的是
A.放电时,负极的电极反应式:Li-e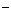 =Li
=Li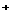
B.充电时,Li 既发生氧化反应又发生还原反应
既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li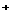 向负极移动
向负极移动
11. 下列装置所示的实验中,能达到实验目的的是




10.已知氧元素有16O、18O两种核素,按中学化学知识要求,下列说法正确的是 ( )
A.Na2O2与H218O反应时生成产生18O2气体
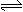 B.向2SO2(g)+O2(g) 2SO3(g)的平衡体系中加入18O2,结果18O2只出现在产物中
B.向2SO2(g)+O2(g) 2SO3(g)的平衡体系中加入18O2,结果18O2只出现在产物中
C.CH3COOH和CH3CH218OH发生酯化反应时,产物中分子式为H218O
D.用惰性电极电解含有H218O的普通水时,阳极可能产生三种相对分子质量不同的氧分子
9.下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的是
A.Mg2+、Na+、SO42-、Cl- B.K+、CO32-、Cl-、NO3-
C.Na+、K+、NO3-、SO32- D.NH4+、Na+、SO42-、NO3-
7、下列操作会导致实验结果偏高的是 ( )
A、中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,所测中和热的数值
B、配置一定物质的量浓度溶液时,定容后反复摇匀发现液面低于刻度,没有再加水,所得溶液的浓度
C、配制一定物质的量浓度溶液时,用量筒量取浓溶液的体积时仰视读数,所得溶液的浓度
D、用天平称量20.5g某物质,砝码和药品的位置放反,所得药品的质量
8下列指定微粒的数目相等的是
A.物质的量相等的水与重水含有的中子数
B.等质量的乙烯和丙烯中含有的共用电子对数
C.同温、同压、同体积的一氧化碳和乙烯含有的质子数
D.等物质的量的铁和铜分别与足量氯气完全反应,转移的电子数
3.下列化学实验事实及其解释都正确的是
A.升高温度化学反应速率加快,是因为单位体积内活化分子百分数增加
B.将SO2通入BaCl2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸
C.鸡蛋清溶液中加入饱和CuSO4溶液析出沉淀,说明蛋白质发生了盐析
D.滴有酚酞的Na2CO3溶液中滴加BaCl2溶液后红色变浅,说明BaCl2溶液有酸性
4在一定温度下,恒容密闭容器中,充入一定量的NO和O2,发生2NO+ O2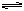 2NO2,
2NO2,
反应达到平衡的标志是( )
①. NO、O2、NO2分子数目比是2:1:2 . ②反应混合物中各组分物质的浓度相等
③. 混合气体的颜色不再变化 ④. 混合气体的密度不再改变
⑤混合气体的平均相对分子质量不再变化 ⑥ 2 v O2(正)= V NO2(逆)
A ② B ①② C ②③④ D ③ ⑤⑥
5一定条件下,充分燃烧一定量的丁烷放出热量161.9 kJ,经测定完全吸收生成的二氧化碳需消耗5mol/L的KOH溶液100mL,恰好生成正盐。则此条件下热化学方程式: 的ΔH为
A.+2590.4KJ/mol B. -2590.4KJ/mol
的ΔH为
A.+2590.4KJ/mol B. -2590.4KJ/mol
C. +1295.2KJ/mol D. -1295.2KJ/mol
6设阿伏加德罗常数的值为NA。则下列说法正确的是
A.常温常压下,18.0 g NH4+中所含的质子数为10 NA
B.室温下,8g甲烷含有共价键数为2NA
C、111gCaCl2晶体中所含共用电子对的数目为2NA
D.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA
2.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是
 A.CO2的电子式:
A.CO2的电子式: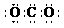
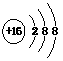
B.S2-的结构示意图:
C.乙烯的结构简式:C2H4
D.质量数为37的氯原子:
1.下列叙述错误的是
A.合金材料中可能含有非金属元素
B.人造纤维,合成纤维和光导纤维都是有机高分子化合物
C.加热能杀死甲流感病毒是因为病毒的蛋白质受热变性
D.在车排气管上加装“催化转化器”是为了减少有害气体的排放
8、化合物X是一种不稳定的物质,它的化学组成可用OxFy表示。10mLX气体能分解生成15mLO2和10mLF2(同温、同压下)。则X的化学式是( )
A.OF2 B.O2F2 C.O3F2 D.O3F4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com