
题目列表(包括答案和解析)
5. 分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:[MxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子晶胞结构如图示,下列说法正确的是
分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:[MxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子晶胞结构如图示,下列说法正确的是
A.该晶体是原子晶体
B.M的离子位于上述晶胞的面心,呈+2价
C.M的离子位于上述晶胞体心,呈+1价,且M+空缺率为50%(体心中没有M+的占总体心的百分比)
D.晶体的化学式可表示为MFe2(CN)6,且M为+1价
4.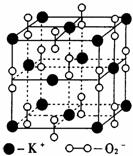 如图是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元)。晶体中氧的化合价可看作是部分为0价,部分为-2价。
如图是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元)。晶体中氧的化合价可看作是部分为0价,部分为-2价。
①该结构与 的结构相似(填选项字母,下同)。
A.NaCl B.CsCl C.干冰 D.SiO2
②钾、氧两元素所形成化合物的化学式是 。
A.K2O B.K2O2 C.K2O3 D.KO2
③下列对KO2晶体结构的描述正确的是 。
A. 晶体中与每个K+距离最近的K+有8个
B.晶体中每个K+周围有8个O2-,每个O2-周围有8个K+
C.每个 O2-周围最近且等距离的K+所围成的空间构型为正八面体
D.晶体中,0价氧原子与-2价氧原子的数目比为3:1
3..若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为
A.CH4·14H2O B.CH4·8H2O
C.CH4·7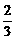 H2O D.CH4·6H2O
H2O D.CH4·6H2O
2.下列各组物质中,按熔点由低到高排列正确的是( )
A. O2 、I2、 Hg B. CO2 、KCl 、SiO2
C. Na、K、 Rb D.SiC 、 NaCl 、SO2
1.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A. SO2和SiO2 B. CO2和H2
C. NaCl和HCl D.CCl4和KCl
10.(1)Al H2 Cl2 。 (2)非金属,2H2O+4F2?4HF+O2
(3)氧化物,SiO2+2C高温si+2CO
2010年高考化学第二轮复习20分钟专题突破(23)
专题 晶体
7.HClO 8.28 9.Na2S、SO3、SO2+2H2S=3S+2H2O
1.C 2.D 3.C 4.B 5.B 6.D
10.A、B、C、是三种短周期元素的单质,甲、乙是两种常见的化合物,这些单质、化合物之间存在如下图所示关系,反应条均未注明,回答下列问题:

下列(1)-(3)中的A不在同一主族。
(1)若A为ⅢA族元素,则A是 ,B为 ,C为 。
(2)若化合物甲在常温、常压下为液态,则组成化合物甲的元素所属类别为 。
(填金属或非金属),单质A与化合物甲反应的化学方程式为: 。
参考答案
9.有X、Y、Z三种元素,已知①它们都是短周期元素,X和Z在同一周期②它们可以组成X2Z、ZY2、ZY3③ZY3与水化合生成一种强酸,此强酸与X2Z反应可生成一种气体A,A和ZY2反应可得到单质Z,则X2Z是________,ZY3是________。A和ZY2反应的方程式为___________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com