
题目列表(包括答案和解析)
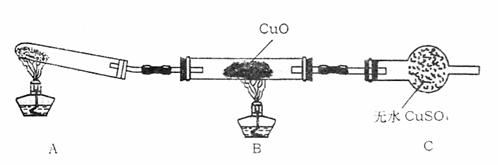
(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是
。
(2)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与CuO反应的化学方程式
。
(1)写出实验室制取氨气的化学方程式 ;
(2)在实验室中,还可以用浓氨水与 (填写一种试剂)快速制取少量氨气;
(3)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的? (填“能”或“否”),理由是
。
3.某校化学研究性学习小组的同学在学习了氨的性质持讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列研究:
2. 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象所得到的有过氧化钠跟水反应的结论是:
第一,为氧气生成,
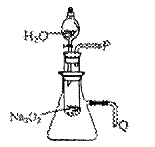 第二,
。
第二,
。
Na2O2跟水反应的化学方程式是 。
(2)某研究性学习小组拟用右图所示装置(气密
性良好)进行实验,以证明上述结论。
用以验证第一条结论的实验操作及现象是:
。
用以验证第二条结论的实验操作及现象是:
。
(3)实验(2)向试管中加水至固体完全溶解且不再有气泡生成后,取出度管,向试管中滴入酚酞试液,发现溶液先变红后退色,为探究其原因,该小组同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2,H2O2具有强氮化性的漂白性。
请设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在。(只要求写出实验所用的试剂及观察到的现象)
试剂: ;
现象: 。
 (4)该小组同学提出用定量的方法探究Na2O2跟水反应后的溶液中是否含有H2O2,其实验方法为:称取2.6gNa2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论:
(4)该小组同学提出用定量的方法探究Na2O2跟水反应后的溶液中是否含有H2O2,其实验方法为:称取2.6gNa2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论:
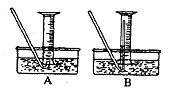
①测量气体体积时,必须持试管和量筒内的气体
都冷却至室温时进行,应选用如图装置中的
(忽略导管在量筒中所占的体积)
(填序),理由是
。
②若在标准状况下测量气体的体积,应选用的量
筒的大小规格为 (选填“100mL”、“200mL”、“500mL”或“1000mL”)
1.某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。

请回答下列问题:
(1)装置F中发生反应的离子方程式是 。
(2)装置A中的烧瓶内固体可选用 (选填以下选项的代号)。
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从右图的备选装置中选择,并将编号填入下列空格。B 、D 、E 。
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为: ;装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体就是氯化铵: 。
(5)若从装置C和G处逸出的尾气中含有N2和少量C12,应如何处理?
。
6. (1)1、5、3、3、3、3。
(2)①I2+SO32 -+H2O = 2I-+SO42 -+2H+;②在步骤b后,增加操作:将分液漏斗充分振荡后静置。
(3)①溶液由蓝色恰好变为无色。 ②20
tt2010年高考化学第二轮复习20分钟专题突破(28)
专题 实验探究
5. (1)反应前先用小火加热烧瓶,B、C、D瓶中有气泡冒出,停止加热之后,水会升到导管里形成一段水柱,证明装置不漏气.
(2)
(3)无水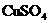 检验水蒸气 品红溶液 检验
检验水蒸气 品红溶液 检验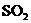 酸性
酸性
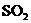 澄清石灰水 检验
澄清石灰水 检验 (4)酸性
(4)酸性 溶液颜色不褪色
溶液颜色不褪色
4. (1)500mL的容量瓶、烧杯、胶头滴管
(2)10 (3)C
(4)①搅拦,加速氢氧化钠固体的溶解 ②引流液体
1.C 2.B 3.B
6. 市场销售的某种食用精制盐包装袋上有如下说明(部分):
|
产品标准 |
 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
20-50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处):
 +
+  + H2SO4
+ H2SO4 == 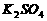 +
+  +
+ 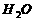
(2)上述反应生成的 可用四氯化碳检验。向碘的四氯化碳溶液中加入
可用四氯化碳检验。向碘的四氯化碳溶液中加入 稀溶液,将
稀溶液,将 还原,以回收四氯化碳。
还原,以回收四氯化碳。
① 稀溶液与
稀溶液与 反应的离子方程式是
反应的离子方程式是
②某学生设计回收四氯化碳的操作步骤为:
a、将碘的四氯化碳溶液置于分液漏斗中;
b、加入适量 稀溶液;
稀溶液;
c、分离出下层液体。
以上设计中遗漏的操作及在上述操作中的位置是
(3)已知: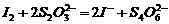
某学生测定食用精制盐的碘含量,其步骤为:
a、准确称取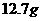 食盐,加适量蒸馏水使其完全溶解;
食盐,加适量蒸馏水使其完全溶解;
b、用稀硫酸酸化所得溶液,加入足量 溶液,使食用盐中
溶液,使食用盐中 与
与 反应完全;
反应完全;
c、以淀粉溶液为指示剂,逐滴加入物质的量浓度为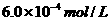 的
的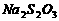 溶液
溶液 ,恰好反应完全。
,恰好反应完全。
①判断c中反应恰好完全依据的现象是
②根据以上实验和包装说明,所测精盐的碘含量是

参考答案
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com