
题目列表(包括答案和解析)
5. 解析:D项中,AgNO3溶液不能鉴别NaCl溶液、Na2SO3溶液,因两者都有白色沉淀生成。
答案:D
4. 解析:A项和B项中,NaOH溶液能够将CO2和SO2完全吸收;C项中,饱和的NaHCO3溶液和SO2反应生成CO2气体,经过浓H2SO4干燥,可以得到干燥纯净的CO2;D项中,浓硫酸不起作用,饱和的Na2CO3溶液既能够吸收SO2,也能吸收CO2。k+s-5#u
答案:C
3. 解析:A项中,苯酚和饱和NaHCO3溶液不反应;B项中,蔗糖分子结构中没有醛基,不能和Cu(OH)2悬浊液反应;C项中,PH试纸试纸变蓝,说明醋酸根离子水解显k+s-5#u碱性,即醋酸为弱酸;D项中,淀粉不能透过半透膜,所以应该取袋外液体来分析。k+s-5#u
答案:C
2. 解析:A项中,能够和BaCl2溶液生成沉淀的离子除SO42-外,还有Ag+等离子;B项中,SO42-和Ag+生成的Ag2SO4也不能溶解与稀盐酸;C项中,HCO3-或HSO3-也能够和盐酸生成CO2或SO2;D项中,氨气能够使湿润的红色石蕊试纸变蓝。k+s-5#u
答案:B
1. 解析:A项装置是铁的吸氧腐蚀,铁钉为负极,石墨为正极,氧气在正极参与反应生成OH-离子;B项中,Na+的检验不需要透过蓝色钴玻璃;C项中,胶头滴管不能伸入试管中。
答案:D k+s-5#u
21.(10分)下图所示是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。

(1)若锥形瓶中盛装锌片,分液漏斗中盛装稀硫酸,则:
①当仪器连接顺序为A→D→B→B→C时,两次使用B装置,其中所盛的药品依次是CuO、无水CuSO4粉末。此实验的目的是 。
②为了使B中CuO反应充分,在不改变现有药品的条件下,可采取的方法有(写一种) 。
③加热前必须进行的操作是 。
(2)若锥形瓶中盛装Na2SO3固体,分液漏斗中盛装H2SO4溶液,B中装过氧化钠固体,验证SO2气体与过氧化钠反应时是否有O2生成。
①SO2与过氧化钠反应生成O2的方程式可能为: ;
②根据气流方向,从图中选择适当的仪器进行实验,装置的连接顺序为(填字母);( )→( )→( )→( )→( );(可以不填满,也可以补充)
装置B中可能观察到的现象是 。
③验证有O2产生的方法是: 。
④有同学认为B装置后要接装置C或装置D或装置E,你的选择是 ,其理由为: 。k+s-5#u
答案和解析
20.(10分)某研究性学习小组在查阅资料时发现,化工厂常用氨气来检验氯气是否泄漏,于是它们设计实验来探究氯气与氨气之间的反应。该小组设计的实验装置如下图:k+s-5#u

实验可用药品有:a. 二氧化锰 b. 浓盐酸 c. 浓氨水 d. 氯化铵 e.碱石灰 f.浓硫酸 g. 饱和食盐水 h. NaOH固体 i.消石灰k+s-5#u
请回答下列问题:
(1)实验室制备氨气有多种方法。通常用加热固体混合物的方法制备氨气,反应的化学方程式是 ,本实验中装置A烧瓶内的固体可选用 (填上述给定药品的序号)。
(2)装置E的烧瓶中发生反应的化学方程式是 。
(3)装置D中盛装的药品是 (填序号),装置C的作用是 。
(4)通入B装置的两根导管左边的较长、右边的较短,其目的是 。
(5)实验中观察到装置B内出现浓厚的白烟,并在容器壁上凝结成白色固体,将该固体溶于水,所得溶液中离子浓度由大到小的顺序为 。
(6)已知,在水溶液中能发生反应3Cl2+2NH3===N2+6HCl,如果氯气过量,一种产物分子的空间构型与NH3相似,该反应的化学方程式是 。
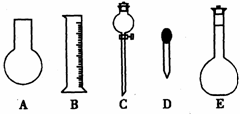
19.(12分)某种胃药片中含有CaCO3,为测定每片中CaCO3的含量(药片中的其他成分不与酸、碱反应),需要完成下列实验步骤:
 k+s-5#u
k+s-5#u
①配制0.1mol·L-1盐酸和0.1 mol·L-1 NaOH溶液;
②取一片此胃药片(药片质量均相等,每片为0.2g),磨碎后转移至锥形瓶中;
③以酚酞为指示剂,用0.1 mol·L-1NaOH溶液滴定,用去Vx mL NaOH溶液时达到滴定终点;
④加入25mL 0.1 mol·L-1盐酸。
(1)为使测定结果准确,至少需要滴定两次,得到的Vx值分别为V1和V2。写出全部实验过程中,各步操作的正确顺序(填编号): 。
(2)图中所示仪器中,配制0.1mol·L-1盐酸和0.1mol·L-1 NaOH溶液肯定不需要的仪器是 (填序号);配制上述溶液还需要用到的玻璃仪器是(量取液体的仪器除外) (填仪器名称)。
(3)写出相关化学方程式: 。
(4)每片胃药中含CaCO3的质量为 g。
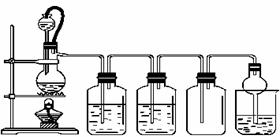
18.(10分)(1)实验室制取乙烯常因温度过高产生少量的二氧化硫,因此实验便包括了二氧化硫的尾气处理,但是图1实验却存在着严重的装备错误与不足,请一一指出:
|
A |
|
E |
|
|
B |
|
F |
|
|
C |
|
G |
|
|
D |
|
H |
|
注:以上表格可以不填满,但是不能错填。
(2)有人设计图2所示简易装置进行实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:

a.图中①、②、③、④装置可盛放的试剂是(填序号):
①________;②________;③________;④________。
A.品红溶液 B.氢氧化钠溶液 C.浓硫酸 D.高锰酸钾酸性溶液
b.能说明二氧化硫气体存在的现象是_______________________________________。
c.使用装置②的目的是____________________________________。
d.使用装置③的目的是____________________________________。k+s-5#u
e.确定含有乙烯的现象是____________________________。
17.(10分)
浓H2SO4和木炭在加热时发生反应的化学方程式是
2H2SO4(浓)+C  CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)



将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
|
选用的仪器 (填字母) |
加入的试剂 |
作用 |
|
|
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com