
题目列表(包括答案和解析)
7.(09广东化学模拟)下列物质保存方法正确的是( )
①金属钠一煤油或石蜡油; ②过氧化钠一塑料瓶密封;
③水玻璃一橡胶塞细口瓶; ④氯水一毛玻璃塞棕色细口瓶;
⑤苯一毛玻璃塞无色细口瓶; ⑥浓、稀硝酸 毛玻璃塞棕色细口瓶;
A.全部 B.⑤④⑥ C.②④⑥ D.①②③
6.(2009杭州学军中学模拟题)下列实验操作或原理不正确的是 ( )
A.纸层析法中的展开剂之所以能够展开的主要原理是毛细现象
B.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.测定溶液pH的操作:将pH试纸置于表面皿上,用洁净玻璃棒蘸取溶液,点在pH
试纸的中部,与对应的标准比色卡比较
5.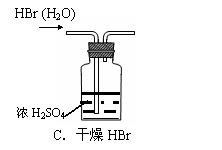
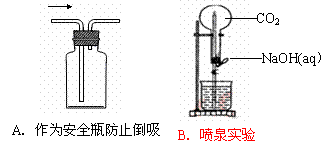
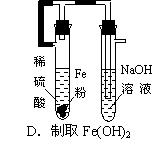 下列装置能达到实验目的的是
( )
下列装置能达到实验目的的是
( )
4.(惠州市2009届二模)假设与猜想是科学探究的先导,在下列假设(或猜想)引导下的探究活动肯定没有实际意义的是 ( )
A.探究浓硫酸与铜在一定条件下反应产生的黑色物质中可能有CuS
B.探究SO2和Na2O2反应可能有Na2SO4生成
C.探究Na与水的反应可能有O2生成
D.向滴有酚酞的NaOH溶液中通入 Cl2,探究红色褪去的原因是溶液的酸碱性变化还是HClO的漂白性所致
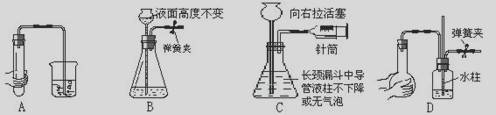
3.(山东诸城一中2009届评估题)下列各图所示装置的气密性检查中,漏气的是( )
2.(2009浙江卷13)下列说法正确的是 ( )
A.仅用AgNO3溶液便可鉴别亚硝酸钠和食盐
B.重结晶时,溶液冷却速度越慢得到的晶体颗粒越大
C.乙酸与乙醇的混合液可用分液漏斗进行分离
D.用标准盐酸滴定待测NaOH溶液时,水洗后的酸式滴定管未经标准液润洗,
则测定结果偏低
1. (新编)下列说法正确的错误的是 ( )
A. 食醋用氢氧化钠溶液滴定开始时,溶液的PH通常变化缓慢,当接近完全反应时(即
滴定终点),PH出现突变,称为滴定突跃。
B. Cu2+与足量氨水反应的离子方程式 Cu2++2NH3·H2O==Cu(OH)2↓+2NH4+
C. 抽滤装置由 布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,工作的主要原理是抽气
泵给吸滤瓶减压,导致装置内部的压强降低,使过滤的速度加快。
D. 硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出。
(二)[猜想II]:主要成分为氯化锌;
[验证(操作)过程]: ;
[实验现象]: ;
[判断猜想]:猜想Ⅱ成立;
由上述实验得出的结论是:滤液中的主次成分: 。
11.实验和探究对化学学科的发展起着非常重要的作用
⑴为了探究食盐中有没有加入碘元素,某学生选取的试剂有:食盐、食醋、碘化钾、淀粉,请问,该学生还必须的一种化学物质是 (填化学式),淀粉在其中所起的作用是
⑵某学生为了探究铝合金中是否含有铝元素,第一步的操作是将合金切成小块,然后溶解于某溶液中,试问溶解铝合金使用的试剂可以是 (填写一种常用试剂),请写出一个合理的化学方程式
⑶某学生为了探究牙膏中是否含有碳酸钙,利用的化学反应原理
是 (用离子方程式表达),而需要检验牙膏中有没有甘油,当溶液中加入 试剂后会
出现 现象。
⑷为了探究海水中是否含有Na+、Mg2+ ,检验前者通常使用的是 的方法,检验后者一般使用常用的 试剂。
12.实验室向40ml硫酸亚铁溶液(浓度约为4.0mol/L)中加入过量硫酸铵来制取摩尔盐((NH4)2SO4·FeSO4·6H2O),其流程如下:

请回答下列问题:
(1)摩尔盐的溶解度随温度变化并不大,采用冷却结晶回收率不高,有人建议直接采用蒸发结晶,你认为是否合理?____________并给出你的理由
 (2)若降温过程中未见摩尔盐晶体析出,可以
促使结晶出现。
(2)若降温过程中未见摩尔盐晶体析出,可以
促使结晶出现。
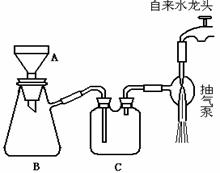
(3)下图所示为减压过滤装置,回答有关问题。
①写出图中A、B、C三种仪器的名称,A_____;B ______;C______。
②该装置图有几处错误,请指出错误。_____;______( 写出两处即可)
(4)过滤是一种常见的物质分离方法,下列实验方法也可用于物质分离的是
a.分液 b.蒸馏 c.盐析 d.滴定 e.洗气 f. 纸层析
(5)另取等量硫酸亚铁溶液,用1mol/L的酸性高锰酸钾溶液进行滴定:
①滴定终点的现象为 ,滴定原理为 (用离子反应方程式表示)
②滴定过程中可能用到下列哪些仪器?
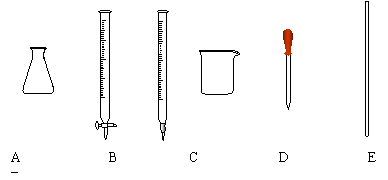
(6)滴定至终点耗用高锰酸钾溶液40ml,若实验最后得到摩尔盐晶体为58.8g,则本次实验的产率为 。
(一)[猜想I]:主要成分为氯化铵;
[验证(操作)过程]:取少量滤液加入NaOH固体,并加热;
[实验现象]:闻到有轻微的氨味;
[判断猜想]: (“填猜想I成立”或“填猜想I不成立”);
10、(浙江省萧山区2009年高考模拟题)某同学用废干电池内的黑色固体(可能含有MnO2、NH4Cl、ZnCl2等物质)进行如图所示实 验:
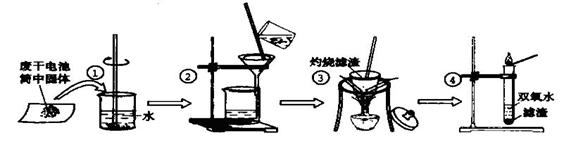
(1) 操作②中过滤时玻璃棒的作用: ;
(2) 操作④加入③中所得滤渣,试管中迅速产生能使带火星的木条复燃的气体,由此推测滤渣含有MnO2,试管中发生反应的化学方程式: ;
(3) 操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的物质为: 。
(4) 已知氯化锌与稀氨水反应先生成Zn(OH)2白色沉淀,Zn(OH)2可以溶于稀氨水生成可溶性的Zn(NH3)4(OH)2;下列是该同学对操作②的滤液主次成分进行探究的过程:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com