
题目列表(包括答案和解析)
10.化学影响着社会的发展和人们的生活质量,以下说法正确的是
A.焚烧废旧塑料可以解决“白色污染”问题
B.为了加强食品的色、香、味,可以大量使用添加剂
C.糖类和油脂在人体内经氧化放出能量,为机体活动和维持恒定体温提供能量
D.将草木灰和碳铵混合施用有利于提高肥效
9.下列说法中正确的是
A.中和反应有盐和水生成,所以有盐和水生成的化学反应一定是中和反应
B.单质只含一种元素,所以含一种元素的物质一定是单质
C.离子是带电的原子或原子团,所以带电的微粒一定是离子
D.溶液是由溶质和溶剂组成,所以溶液一定是混合物
8.下列实验操作正确的是
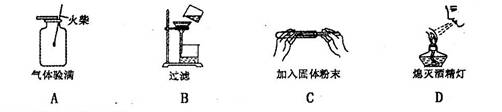
7.在化学反应MnO2+4HCl(浓)====MnCl2+2H2O+Cl2↑中,同种元素的化合价在化学反应前后变化最大的元素是
A.Mn B.Cl C.H D.O
6.下列变化过程中既有物理变化又有化学变化的是
A.活性炭吸附冰箱中的异味 B.干冰汽化
C.点燃蜡烛 D.分离液态空气制取氧气
14.(6分) 科学探究是奇妙的过程,在一次实验中,小明小心把硫酸铜溶液滴加到了盛有5%过氧化氢的溶液中,立即有大量气泡产生.硫酸铜溶液中有三种粒子(H2O,SO42-,Cu2+),小明想知道硫酸铜溶液中的哪种粒子能使双氧水分解的速率加快.请你和小明一起通过下图所示的三个实验完成这次探究活动,并填写空白.
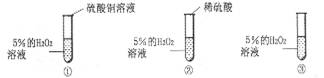
(1). 你认为最不可能的是哪一种粒子,理由是________________________________-,
(2). 检验实验产生的气体的方法是_________________________--.
(3). 要证明另外两种粒子能否加快双氧水分解的速率,还需要进行实验②和③:
在实验②中加入稀硫酸后,无明显变化,说明________不起催化作用;
在实验③中加入 ____后,会观察到大量气泡,证明起催化作用的是_____________.
(4). 小明如果要确定硫酸铜是催化剂,还需通过实验确认它在化学反应前后_______________________.
13. (4分).下图是实验室常用的实验装置,请回答下列问题.
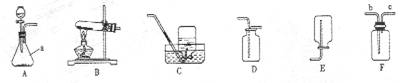
(1). 写出仪器a的名称_____--.
(2).用上述装置组装实验室制取和收集二氧化碳的一组仪器组合是___________(填装置代号字母). 若用F进行排空气法收集氢气,则气体应从___口进入.(填b或c).
(3).若某同学用C装置收集一瓶较纯净的氧气,当观察到____________时开始收集.
28.化学兴趣小组的同学取10 g某锌样品(含少量杂质,且杂质不溶于水,也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7 g时,恰好完全反应,生成气体的质量与反应时间 的关系如下图所示,试回答下列问题:
的关系如下图所示,试回答下列问题:
(提示:Zn+H2SO4=ZnSO4+H2↑)

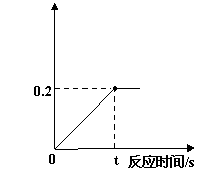 (1)从右图中可以看出,完全反应后生成氢气的
(1)从右图中可以看出,完全反应后生成氢气的
质量为 72 g。(1分)
(2)样品中锌的质量为 73 g。(1分)
(3)反应后,所得溶液中硫酸锌的质量分数
为多少?(4分) 74

27.饮酒会使人的 中枢神经系统过度兴奋或麻痹抑制,容易引发交通事故。2011年5月1日开始,《刑法修正案》和修改后的《道路交通安全法》开始实施,对醉酒驾车者一律刑事拘留。下表是国家对“饮酒驾车”和“醉酒驾车”的界定标准:
中枢神经系统过度兴奋或麻痹抑制,容易引发交通事故。2011年5月1日开始,《刑法修正案》和修改后的《道路交通安全法》开始实施,对醉酒驾车者一律刑事拘留。下表是国家对“饮酒驾车”和“醉酒驾车”的界定标准:
|
饮酒驾车 |
20毫克/100毫升 ≤ 血液中的酒精含量 <
80毫克/100毫升 |
|
醉酒驾车 |
血液中的酒精含量 ≥ 80毫克/100毫升 |
(1)某司机驾车时经交警检查每100毫升血液中酒精含量为138毫克,他属于 68 驾车;(1分)
(2)交警通常用一种“酒精检测仪”检查司机呼出气体中酒精的含量,其反应原理为:C2H5OH+4CrO3+6H2SO4=2Cr2(SO4)3+2X↑+9H2O,反应中红色的CrO3转变为绿色的Cr2(SO4)3,则X的化学式为 69 。(1分)
A.CO2 B.SO2 C.O2 D.H2
(3)乙醇(C2H5OH)俗名酒精,由 70 种元素组成,其中碳、氧两元素的质量比为:
71 。(2分)
26.化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了 以下探究:
以下探究:
[提出问题1] 该氢氧化钠溶液是否变质了呢?
[实验探究1]
|
实验操作 |
实验现象 |
实验结论 |
|
取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡。 |
有气泡冒出。 |
氢氧化钠溶液一定变质了。 |
[提出问题2] 该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想1:氢氧化钠溶液部分变质。
猜想2:氢氧化钠溶液全部变质。
[查阅资料] (1) 氯化钙溶液呈中性。
(2) 氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
[实验探究2]
|
实验步骤 |
实验现象 |
实验结论 |
(1)取少量该溶液于试管中,向 溶液中滴加过量 溶液中滴加过量 的氯化钙溶液,并不断振荡。 的氯化钙溶液,并不断振荡。 |
有 62 生成。 |
说明原溶液中一定有碳酸钠。 |
|
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 |
溶液变红色。 |
说明原溶液中一定有 63 。 |
[实验结论] 该氢氧化钠溶液 64 (填“部分”或“全部”)变质。
[反思与评价] (1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:
65 。
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,
你认为该方案 66 (填“可行”或“不可行”)。
[理解与应用] 氢氧化钠溶液容易变质,必须密封保存。实验室必须密封保存的药品还有很
多,试另举一例: 67 。
67 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com