
题目列表(包括答案和解析)
7.1999年曾报导合成和分离了含高能量的正离子N5+的化合物N5ASF6,下列叙述错误的是
A.N5+共有34个核外电子 B.N5+中N-N原子间以共用电子对结合
C.化合物N5AsF6中As化合价为+l价 D.化合物N5AsF6中F化合价为-1价
6.下列各组物质均由一种干燥气体和一种液体组成,其中可以进行喷泉实验,且液体几乎充满烧瓶的组合是 ( )
A.Cl2,饱和食盐水 B.SO2 氨水 C.NH3,稀盐酸 D.NO2 水
5.氯胺(NH2Cl)在中性或酸性条件下是一种有效的强力消毒剂,据此判断,氯胺在水溶液中因水解产生的物质是 ( )
A.HCl0和HCl B.NH4C1和HCl C.NH4Cl和HCl0 D.NH4Cl和HClO3
4.国外有人用激光将置于铁室中石墨靶上的碳原子炸松,与此同时再用射频电火花喷射N2,此时碳氮原子结合成碳氮化合物薄膜。据称,这种化合物可能比金刚石更坚硬,其原因可能是 ( )
A.碳、氮原子构成网状结构的晶体 B.碳氮键比金刚石中的碳碳键更短
C.氮原子最外层电子数比碳原子最外层电子数多 D.碳、氮的单质化学性质均不活泼
3.石墨炸弹爆炸时,能在方圆几百米范围内撤下大量石墨纤维,造成输电线、电厂设备损失,这是由于石墨 ( )
A.有放射性 B.易燃、易爆 C.能导电 D.有剧毒
2.宣传科学知识,介绍高新科技,揭露伪科学,是科学工作者的义务,下列各项中学的是)
A.高温高压下将石墨制成金刚石 B.用催化剂将水变成燃料油
C.将空气中游离的氮变成氮的化合物 D.用碘化银人工降雨
1.目前,我国城市环境污染中的大气污染物主要是 ( )
A.NH3、NO、CO2、雾 B.CO2、N2、Cl2、酸雨
C.SO2、NO2、CO、烟尘 D.HCl、SO2、N2、沙尘暴
29.某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为
(2)A与溴的四氯化碳溶液反应的化学方程式为 ,反应类型是 。
(3)已知: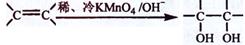 ,请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得产物的结构简式
;该产物与足量醋酸反应的化学方程式为
,请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得产物的结构简式
;该产物与足量醋酸反应的化学方程式为
;
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式 。w.w.^w.k.s.5*
(5)在一定条件下,A聚合得到高分子化合物的化学方程式为 。
28.下列图1中B是一种常见的无色无味的液体。C是一种有磁性的化合物,E是一种无色无味的有毒气体。根据下列图1、图2,回答下列问题:w.w.^w.k.s.5*
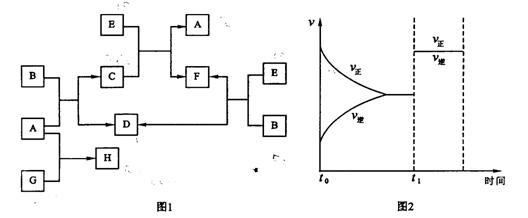
(1)写出A+B→C+D的化学方程式 ;
(2)在101kPa和150℃时,可逆反应E(g)+ B(g) F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
;
F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
;
A.升高温度 B.增大压强 C.加入催化剂
(3)若G是一种黄色固体单质,16 g G和足量的A反应放出的热量为QkJ(Q > 0),写出这个反应的热化学方程式 。
(4)若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式 ;少量H的浓溶液滴入沸水中,继续煮沸,生成了一种红褐色的液体,请用离子方程式表示该过程 。w.w.^w.k.s.5*
(5)请写出C与足量的稀盐酸反应的离子方程式__________________
答案:(1)3Fe +4H2O(g)=Fe3O4+4H2O
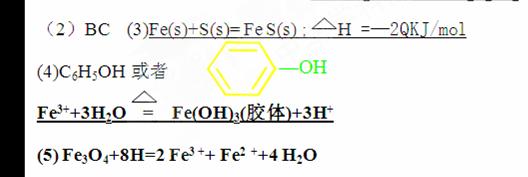
27.Ⅰ、室温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题。
(1)若由0.2mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH>7,则混合溶液中各种离子浓度由大到小的顺序是: 。
(2)若HA为弱酸,现有两组溶液
A组:由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH<7;
B组:0.1mol/L的HA溶液
① A组溶液pH<7的原因:
此时混合溶液中除水分子外的各种微粒浓度由大到小的顺序是:w.w.^w.k.s.5*
。
②两组溶液中c(A-)的大小, A组 B组(填“>”“ <”或“ =”);溶液中水的电离程度A组 B组(填“>”“ <”或“ =”)。
(3)若由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是
(填选项番号字母)。
A.若反应后溶液呈中性,则c(OH-)+c(H+)=2×10-7mol/L
B.若V1= V2,反应后溶液一定呈中性
C.若反应后溶液呈酸性,则V1一定大于 V2 D.若反应后溶液呈碱性,则V1一定小于 V2
(4)若HA为强酸,若是pH=2 HA V1mL与pH=12 Ba(OH)2 V2 mL混合后得到pH=11的溶液,则V1/V2= 此时溶液中离子浓度由大到小的顺序为:
Ⅱ、现有浓度为0.1 mol·L-1的五种电解质溶液①Na2CO3;②NaHCO3;③NaAlO2;④CH3COONa;⑤NaOH
已知:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32-
(1)这五种溶液的pH由小到大的顺序是 (填编号)。将五种溶液稀释相同的倍数时,
其pH变化最大的是 (填编号);w.w.^w.k.s.5*
(2)在上述五种溶液中分别加入AlCl3溶液,能产生大量无色无味气体的是______________(填编号);
(3)将上述①、②、③、④四种溶液两两混合时,有一对溶液相互间能发生反应,现象为:
写出该反应的离子方程式
Ⅰ(1)c(Na+) >c(A-)>c(OH-)>c(H+)
(2)①HA的电离大于A-的水解, c(A-) >c(Na+)> c(HA)>c(H+)>c(OH-)
② > >
(3)AD
(4)9:11 c(A-) >c(Ba2+)>c(OH-)>c(H+)
Ⅱ (1)④②①③⑤ ⑤ (2)①② (3)有白色沉淀产生 HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com