
题目列表(包括答案和解析)
23. I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)
 I3-(aq)
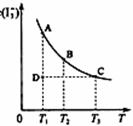
, 某 I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
I3-(aq)
, 某 I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
A.反应I2(aq)+I-(aq)  I3-(aq)的△H>0
I3-(aq)的△H>0
B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
C.若反应进行到状态D时,一定有v正>v逆
D.状态A与状态B相比,状态A的c(I2)大
22.下列化学实验事实及其解释都正确的是( )
A.向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘
B.向SO2水溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸
C.向0.1 mol·L-1FeSO4溶液中加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具氧化性
D. 向2.0 mL浓度均为0.1 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1AgNO3 溶液,振荡,沉淀呈黄色,说明AgCl的KSP比AgI的KSP大
12.已知:2H2S+SO2=3S↓+2H2O。某同学向100 mL氢硫酸溶液中通入标准状况下的二氧化硫气体,所得溶液pH变化如图所示。他据此得到的下列四条关于二氧化硫和亚硫酸的说法。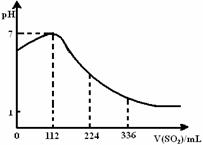 请分析其中正确的是( )
请分析其中正确的是( )
A.SO2是弱电解质
B.H2SO3不是强酸
C.亚硫酸是比氢硫酸还弱的酸
D.原氢硫酸溶液的物质的量浓度0.05 mol·L-1
11.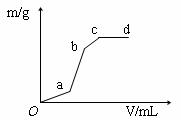 向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于下图曲线的推测正确的是( )
向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于下图曲线的推测正确的是( )
A.ab段产生的沉淀为硫酸钡
B.ab产生段的沉淀为氢氧化镁
C.bc段产生的沉淀为氢氧化镁
D.bc段产生的沉淀为硫酸钡和氢氧化镁
10.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4 +8H2O  3Zn(OH)2
+2Fe(OH)3 +4KOH。下列叙述不正确的是( )
3Zn(OH)2
+2Fe(OH)3 +4KOH。下列叙述不正确的是( )
A.放电时锌做负极 B.充电时氢氧化铁被氧化 C.放电时溶液的碱性增强 D.放电时转移3 mol e-,有2 mol FeO42-被还原
9.下列离子方程式书写正确的是( )
A.少量金属钠加到冷水中:Na+2H2O==Na++OH-+H2↑
B.往氨水中滴加氯化铝:Al3++4OH-==AlO2-+2H2O
C.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-==3Fe3++NO↑+2H2O
D.苯酚钠溶液中通入少量二氧化碳:2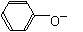 +CO2+H2O
+CO2+H2O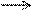 2
2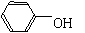 +CO32-
+CO32-
8.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.17 g氨气所含质子数目为1NA
B.2.4 g金属镁变成镁离子时失去的电子数目为0.1NA
C.在标准状况下,22.4 L氧气中所含的氧原子数目为1NA
D.在25 ℃,压强为1.01×105 Pa时,28 g氮气所含的分子数目为NA
7.有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不正确的是( )
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.自然界中存在大量单质硅 C.自然界硅的贮量丰富
D.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
25、以石墨为电极,电解400ml某二价金属的硫酸盐溶液,当溶液中的金属离子全部反应后,阴极增重1.28g,阳极产生了224ml气体(折算成标准状况下),求该金属的摩尔质量及电解后溶液的PH(电解前后溶液体积变化忽略不计)。
24、(10分)某烧碱样品含有少量不与酸作用的杂质,为了滴定其纯度,进行以下滴定操作:
A、配制250ml烧碱溶液;
B、用碱式滴定管取25.00ml烧碱溶液于锥形瓶中并滴加几滴酚酞做指示剂;
C、在天平上准确称取烧碱样品wg,在烧杯中用蒸馏水溶解;
D、将物质的量浓度为c的标准硫酸溶液装入酸式滴定管调整液面记下开始读书为V1ml;
E、在锥形瓶下垫一张白纸,滴至红色刚好消失且半分总内不再变化为止,记下读数V2ml。
就此实验完成下列填空:



 ⑴正确的操作顺序是:(用编号字母填写) D 。
⑴正确的操作顺序是:(用编号字母填写) D 。
⑵观察滴定管里液面的高度时应注意: 。
⑶D操作中液面应调节到 ,尖嘴部分应 。
⑷某学生实验时把锥形瓶用烧碱样品洗涤,使测定的浓度偏高还是偏低? 原因是
。
⑸该烧碱样品纯度的计算式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com