
题目列表(包括答案和解析)
11.(1) 第四周期第Ⅷ族(1分) 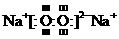 (2分) 纯碱或苏打 (1分)
(2分) 纯碱或苏打 (1分)
(2) 铝热剂(1分) 加入少量 粉末,插上镁条并点燃 (2分)
粉末,插上镁条并点燃 (2分)
(3) MgO、C (各1分)
(4) 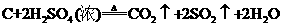 (3分)
(3分)
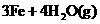
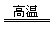
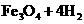 (3分)
(3分)
(5) 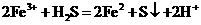 (3分)
(3分)
10.Ⅰ、(1)一氧化碳 (2)生产玻璃。制粗硅
(3)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(4)SiO32-+CO2 +H2O = H2SiO3↓+CO32-
Ⅱ、(1) Na2O2+2H2O=4Na++ 4OH-+O2↑ 0.5mol
(2) H:C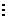
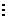 C:H 直线型
C:H 直线型
(3)CO2+OH-= HCO3-; 1:5
9.
(1)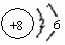
(2) F Na S Cl
(3)HF > HCl 因为HF分子间有氢键
(4) SO32- + 2H+ == SO2↑+ H2O(S2O32- + 2H+ == S↓ + SO2↑ + H2O)
(5)2SO2(g)+O2(g) 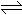 2SO3(g);△H= -196 kJ/mol
2SO3(g);△H= -196 kJ/mol
8. (1) KI 、 AgBr
(2)①2Cl- + 2H2O  H2↑ + Cl2↑ + 2OH-
H2↑ + Cl2↑ + 2OH-
②3I2 + 6OH-  5I- + IO3-
+ 3H2O
5I- + IO3-
+ 3H2O
(3) B D , 水封(放在阴暗处)
(4) I2 > Br2 > Cl2
(5) Cl2+2KOH=KCl+KClO+H2O
7.
(1)原子晶体 C+H2O CO+H2
(2)①H2O 水分子之间存在氢键
 ②2H2S+SO2 3S+2H2O
②2H2S+SO2 3S+2H2O
 ③SO
③SO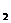 +Cl
+Cl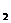 +2H2O 4H
+2H2O 4H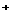 +SO
+SO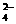 +2Cl
+2Cl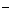
6.
(1)S2-、SO32-存在于甲溶液中,且n(S2)-:n(SO32-)=2
(2)乙 由实验可知,其他的四种阴离子均处于甲溶液中,而溶液呈电中性,故Cl-存在于乙溶液中 (3)K+、S2-、SO42-、SO32-、OH-
5.
 (1)4FeS2+11O2
2Fe2O3+8SO2
(1)4FeS2+11O2
2Fe2O3+8SO2
 (2)NaHSO4+NaHSO3
Na2SO4+ H
(2)NaHSO4+NaHSO3
Na2SO4+ H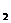 O+SO
O+SO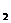 ↑
↑
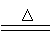
 (3)2MnO4-
+ 5H2O2
+6H+
2Mn2+
+ 8H2O
+5O2↑
(3)2MnO4-
+ 5H2O2
+6H+
2Mn2+
+ 8H2O
+5O2↑
(4)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
 (5)C
(5)C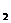 H
H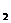 (g)+
(g)+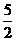 O
O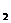 (g) 2CO
(g) 2CO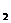 (g)+H
(g)+H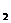 O(l);
O(l);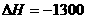 kJ/mol
kJ/mol
4.(1) ①Al3++3HCO3-=Al(OH)3↓+3CO2↑ (2分)
②生成白色胶状沉淀 (2分) AlO2-+ HCO3-+H2O=Al(OH)3↓+ CO32- (3分)
(2)① 2.6g (3分) ②130mL (3分)
3.(1)E>A>D
Br2
Cl2+2NaBr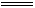 2NaCl+Br2
2NaCl+Br2
(2)2Na2O2+2H2O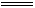 4Na++4OH-+O2↑ 2NA或1.204×1024
4Na++4OH-+O2↑ 2NA或1.204×1024
2.(1)H2+S H2S(写成可逆反应也正确)
H2S(写成可逆反应也正确)
(2)H2SO3 + 2H2S=3S + 3H2O
(3)C+2H2SO4(浓) CO2
↑+2SO2 ↑+2H2O
CO2
↑+2SO2 ↑+2H2O
(其他合理答案也给分如Cu+ 2H2SO4(浓) CuSO4
+SO2↑+ 2H2O等)
CuSO4
+SO2↑+ 2H2O等)
(4)①H2SO3 +2OH- = SO32- + 2H2O
②大于 , Na2SO3溶液中SO32-发生水解使溶液显碱性
③增大 , 升高温度促进Na2SO3溶液的水解
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com