
题目列表(包括答案和解析)
11.(13分)
(1)碳酸锂,碳酸钠,碳酸铍,碳酸镁
(2)mA/MA=mB/MB+mC/MC(或MB<MA<MC;MC<MA<MB 以及其它合理答案)
(3)2种 Li2CO3 MgCO3
(4)MgCO3,BeCO3,Na2CO3 1.05
8.2Al+6HCl==AlCl3+3H2↑2F2+2H2O==4HF+O2
2Mg+CO2===2MgO+C(其它合理答案也行)
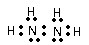 9(1)分子;干冰。
9(1)分子;干冰。
(2)正四面体;非极性;Si3N4。
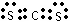 (3)三角锥;
。
(3)三角锥;
。
(4)CS2;CCl4。 ;非极性。
10(1)Al(OH)3+OH-=AlO2-+2H2O。
(2)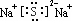
(3)酸 Al3++3H2O Al(OH)3+3H+。
Al(OH)3+3H+。
(4)SO2+Cl2+2H2O=H2SO4+ 2HCl。
(5)HCl>H2S。
(6)Cl2O7(l)+H2O(l)=2HClO4(aq);△H=-4QkJmol-1。
7.(14分)
(1)1nm-100nm
(2)Fe FeS H2SO4(稀)
(3)①  ② 2Fe2+ +H2O2 +2H+ ==2Fe3+
+2H2O
② 2Fe2+ +H2O2 +2H+ ==2Fe3+
+2H2O
(4)取少量 E于试管中,用胶头滴管入 NaOH溶液,加热试管,可观察到试管口处湿
润的红色石蕊试纸变蓝。(或其他合理答案)
(5)4Fe2+ +4Na2O2+6H2O ==4Fe (OH)3↓+O2↑+8Na +
5、(15分)
(1)A:碳(或C) C:钠(或Na)
(2)Na2CO3+2HCl==2NaCl+CO2↑+H2O
(3)2CO2+2Na2O2==2Na2CO3+O2
(4)Na2O2+S2-+2H2O==4OH-+S↓+Na
6:(1)2NH3+H2SO4==(NH4)2SO4
(2)N≡N (NH4)2SO3或NH4HSO3
(3)ClO-+SO2+2OH-==Cl-+SO42-+H2O
(4)N2H4
4.(1)四(或4);Ⅷ。 (2)1:2。 (3)③。 (4)3Fe2++NO3- +4H+ = 3Fe3++NO↑+2H2O。
(5)Fe2O3+3KNO3+4KOH 2K2FeO4+3KNO2+2H2O。
2K2FeO4+3KNO2+2H2O。
11. A、B、C是短周期ⅠA和ⅡA族元素的碳酸盐,它们的质量分别为 mA、mB、mC,
与足量盐酸完全反应,消耗盐酸的物质的量分别为nA(HCl)、nB(HCl)、nC(HCl)。
已知:。mA=mB+mC,nA(HCl)=nB(HCl)+ nC(HCl)。请填空:
(1)写出短周期ⅠA和ⅡA族元素形成的所有碳酸盐的名称:
(2)若以MA、MB和MC分别表示A、B、C的相对分子质量,试写出MA、MB和MC三者的相互关系式 。
(3)A的正确选择有 种,其化学式为: 。
(4)若A和B为ⅡA族元素的碳酸盐,C为ⅠA族元素的碳酸盐,则A、B、C的化学式依次是 ,mB︰mC=1︰ 。(保留2位小数)
无机推断题(一)
1 A:CaC2,B:H2O,D:C2H2,E:CO2,H:Ca(HCO3)2
2(1)Al (2)Al3++3AlO2-+6H2O=4Al(OH)3↓ (3)光照 过量Cl2 (4)Al4C3 12H2O=4Al(OH)3+3CH4↑
3(1)NaI NaClO AgI (2)2I-+ClO-+H2O=I2+Cl-+OH- I2+5ClO-+2OH-=2IO3-+5Cl-+H2O (3)Fe3++SO32-+2H2O=Fe2-+SO42-+4H+ (4)Cl2+2NaOH=NaClO+NaCl+H2O
10.W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生盐和水,该反应的离子方程式为____________________。
(2)W与Y 可形成化合物W2Y,该化合物的电子式为______________。
(3)X的硝酸盐水溶 液显______性,用离子方程式解释原因___________________________________________。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为____________________________。
(5)比较Y、Z气态氢化物的稳 定性_____>_______(用分子式表示)
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:_____>_____>______>______。
(7)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶 液,并放出QkJ的热量。写出该反应的热化学方程式:_______________________。
9. Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y原子序数小于Z。
(1)Q的最高价氧化物,其固体属于________晶体,俗名叫_____________。
(2)R的氢化物的分子的空间构型是_____________,属于____________分子(填“极性”或“非极性”),它与X形成的化合物可作为一种重要陶瓷材料,其化学式是___________。
(3)X的常见氢化物的空间构型是____________;它的另一种氢化物X2H4是一种火箭燃料的成分,其电子式是__________。
(4)Q分别与Y、Z形成的共价化合物的化学式是_______和_______;Q与Y形成的分子的电子式是____________,属于______________分子(填“极性”或“非极性”)。
8.(06全国理综I)27(15分)置换反应的通式可以表示为:
单质(1) + 化合物(1) ==单质(2) + 化合物(2)
请写出满足以下要求的3个置换反应的化学方程式:
①所涉及的元素的原子序数都小于20;②6种单质分属于6种不同的主族
5、 (15分)A、B、C、D是按原子序数由小到大排列的第二、三周期的元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素和金属元素的原子个数比为1 :2。在一定条件下,各物质之间的相互转化关系如右(图中部分产物未列出):
(15分)A、B、C、D是按原子序数由小到大排列的第二、三周期的元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素和金属元素的原子个数比为1 :2。在一定条件下,各物质之间的相互转化关系如右(图中部分产物未列出):
请填写下列空白:
(1)A是 ,C是 。
(2)H与盐酸反应生成E的化学方程式是 。
(3)E与F反应的化学方程式是 。
(4)F与G的水溶液反应生成I和D离子方程式是 。
6(06江苏20)(10分)下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
A.A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。
B.反应①②是化工生产中的重要反应。
C.化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。
D.化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。
E.化合物J由两种元素组成,其相对分子质量为32。
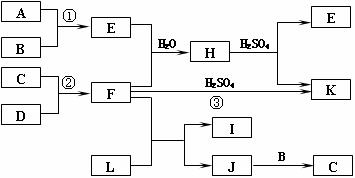
请按要求填空:
⑴反应③的化学方程式______________。
⑵C的结构式______________;H的化学式______________。
⑶L的溶液与化合物E反应的离子方程式______________。
⑷化合物J的化学式______________。
7(14分)中学化学中几种常见物质的转化关系如下:
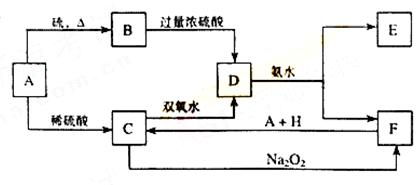
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体E粒子直径大小的范围: 。
(2)A、B、H的化学式:A ,B ,H 。
(3)①H2O2分子的电子式:
② 写出C的酸性溶液与双氧水反应的离子方程式: 。
(4)写出鉴定E中阳离子的实验方法和现象:
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com