
题目列表(包括答案和解析)
4.下列物质发生变化,因反应条件或反应物的用量不同,能够得到不同生成物的是
① Na和 O2 ②C2H5OH和浓 H2SO4 ③H2S和 O2 ④AlCl3和 NaOH ⑤Cu和HNO3
A.①③ B.①④⑤ C.除②③外 D.全部
3.用下列气体和溶液进行喷泉实验,最终液体不能充满烧瓶的是
A.CO2和NaOH溶液 B.NH3和重水
C.Cl2和饱和食盐水 D.NO2和NaOH溶液
2.已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),如下图,则下列判断错误的是
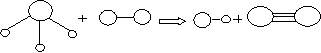
E G L M
A.G是最活泼的非金属单质 B.L是极性分子
C.E能使紫色石蕊试液变蓝色 D.M化学性质活泼
1.三聚氰酸[C3N3(OH)3]可用于消除汽车尾气中的NO2。反应原理为:C3N3(OH)3
3HNCO; 8HNCO+6NO2 7N2+8CO2+4H2O,下列说法正确的是
7N2+8CO2+4H2O,下列说法正确的是
A.C3N3(OH)3与HNCO为同一物质 B.HNCO是一种很强的氧化剂
C.1 mol NO2在反应中转移的电子为4 mol D.反应中NO2是还原剂
23.(15分)科学家对H2O2结构的认识经历了较为漫长的过程,最初,科学家提出了两种观点:①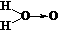 、②H-O-O-H。式中O→O表示配位键,即共用电子对由某原子单方面提供(在化学反应中氧氧键遇到还原剂时易断裂)。
、②H-O-O-H。式中O→O表示配位键,即共用电子对由某原子单方面提供(在化学反应中氧氧键遇到还原剂时易断裂)。
化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应,生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
(1)用电子式表示①、②两种结构:①_________________、②________________。
(2)如果H2O2的结构如①所示,实验c中化学反应方程式为(A写结构简式,下同)___________________________________________________________________;假如H2O2的结构如②所示,实验c中化学反应方程式为_____________________
___________________________________________________________________。
(3)为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:___________________________________________________________
___________________________________________________________________。
22.(13分)科学家发现在特殊条件下,水能表现出许多有趣的结构和性质。
(1)一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如下。

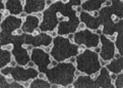

水 热冰
使水结成“热冰”采用“弱电场”的条件,说明水分子是 分子。请你展开想象,给“热冰”设计一个应用实例 。
(2)用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子。
①释放出来的电子可以被若干水分子形成的“网”捕获而形成水合电子,你认为水分子间能形成“网”的原因是 。
②由水分子释放出电子时产生的一种阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式 ;该阳离子还能与水分子作用生成羟基,经测定此时的水具有酸性,写出该过程的离子方程式 。
21.(12分)1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是:
和 ; 和 。
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与NO2-互为等电子体的分子有: 、 。
20.由短周期元素构成的某离子化合物中,一个阳离子和一个阴离子核外电子数之和为20。下列说法中正确的是
A.晶体中阳离子和阴离子个数不一定相等
B.晶体中一定有离子键,可能有共价键
C.所含元素一定不在同一周期也不在同一主族
D.晶体中阳离子半径一定大于阴离子半径
19.顺式Pt(NH3)2Cl2(相对分子质量为300)是临床广泛使用的抗肿瘤药物。下列有关该物质的说法中正确的是
A.由4种元素组成 B.含有NH3分子
C.Pt的化合价为+4 D.Pt元素的质量分数为65%
18.有放射性的同位素称之为稳定同位素,近20年来,稳定同位素分析法在植物生理学、生态学和环境科学研究中获得广泛应用,如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用做环境分析指示物。下列说法中正确的是:
A.34S原子核内的中子数为16
B.1H216O在相同条件下比1H218O更易蒸发
C.13C和15N原子核内的质子数相差2
D.2H+的酸性比1H+的酸性更强
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com