
题目列表(包括答案和解析)
8.工业上由二氧化锰制备高锰酸钾可分二步进行,第一步:二氧化锰与氢氧化钾共熔并通入氧气2MnO2+4KOH+O2 2K2MnO4+2H2O;第二步:电解锰酸钾溶液:2K2MnO4+H2O
2K2MnO4+2H2O;第二步:电解锰酸钾溶液:2K2MnO4+H2O 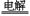 2KMnO4+H2↑+2KOH下列说法叙述正确的是
2KMnO4+H2↑+2KOH下列说法叙述正确的是
A 氧化性:KMnO4>K2MnO4>O2
B 根据上述过程,每生成1mol KMnO4共转移6mol电子
C 第二步电解时,KMnO4在阳极区生成
D 第二步电解时阴极周围pH减小
7.固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。其工作原理如右图所示:下列关于固体燃料电池的有关说法正确的是
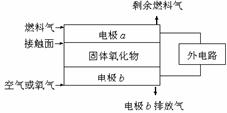 A.电极b为电池负极,电极反应式为O2+4e-=4O2-
A.电极b为电池负极,电极反应式为O2+4e-=4O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为
H2+2OH--4e-=2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为
C2H4+6O2--12e-=2CO2+2H2O
6.2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的 烯烃复分解催化剂。工业上冶炼钼的化学原理为:

则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3是金属氧化物,能溶解于稀盐酸中
C.H2MoO4是一种强酸
D.用还原剂还原等质量的MoO3,消耗H2、CO和Al的物质的量之比为3:3:2
5.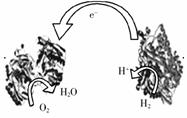 2006年,科学家们发明了一种能够给电子设备提供动力的生物燃料电池。该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中。由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示:下列说法正确的是
2006年,科学家们发明了一种能够给电子设备提供动力的生物燃料电池。该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中。由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示:下列说法正确的是
A.左边为该电池的负极
B.该电池可在高温环境下使用
C.该电池负极反应为:H2 –2e-=2H+
D.该电池正极反应为O2+4e-=2O2–
4.物质的颗粒达到纳米级时,具有特殊的性质。如将单质铜制成“纳米铜”时,“纳米铜”具有非常强的化学活性,在空气中可以燃烧。下列叙述中正确的是
A.常温下,“纳米铜”比铜片的金属性强
B.常温下,“纳米铜”比铜片更易失电子
C.常温下,“纳米铜”与铜片的还原性相同
D.常温下,“纳米铜”比铜片的氧化性强
3.
 某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
A.铅笔端作阳极,发生还原反应
B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生
D.a点是负极,b点是正极
2.物质氧化性、还原性的强弱不仅与物质的结构有关,还与物质的浓度和反应温度有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液 ;由于浓度不同而能发生不同氧化还原反应的是
A.①③ B.③④ C.① D.①③④
1.发生原电池的反应通常是放热反应,在理论上可设计成原电池的化学反应是
A.C(s)+H2O(g)=CO(g)+H2(g) ;△H>0
B.Ba(OH)2·8H2O+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(l)+8H2O(l); △H>0
C.CaC2(s)+2H2O(l)=Ca(OH)2(s)+C2H2(g) ;△H<0
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ;△H<0
15.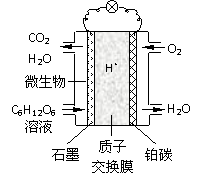 (12分)微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体,将有机物的化学能转化为电能。
(12分)微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体,将有机物的化学能转化为电能。
以葡萄糖溶液作底物为例,其工作原理如右图所示。
 已知石墨电极上反应为:
已知石墨电极上反应为:
C6H12O6+6H2O-24e- 6CO2+24H+
⑴ 电池中的质子交换膜只允许质子和水分子通过。
电池工作时,质子移向电源的 极,
铂碳上所发生的电极反应式为_____________。
⑵ 葡萄糖的燃烧热为2800kJ/mol,写出葡萄糖燃烧的
热化学方程式 。
⑶ 化学需氧量(COD)是重要的水质指标,其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量。科学家设想利用微生物燃料电池来处理某些污水,并进行发电,该设想已经在实验室中获得成功。但如果1L废水中有机物(折算成葡萄糖)氧化提供的化学能低于5.6kJ,就没有发电的必要。则下列污水中,不适合用微生物燃料电池发电的是 (填序号)。
|
序号 |
A |
B |
C |
D |
E |
|
污水类型 |
生活污水 |
印染 |
电镀 |
造纸 |
硫酸工业废水 |
|
COD值(mg/L) |
520 |
870 |
20 |
960 |
120 |
14.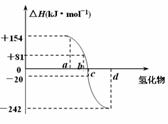 (10分)已知:在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H)。右图为氧族元素氢化物a、b、c、d的生成热数据示意图。试回答下列问题:
(10分)已知:在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H)。右图为氧族元素氢化物a、b、c、d的生成热数据示意图。试回答下列问题:
⑴ 出氧族元素中含有18e-的两种氢化物
。
⑵ 你归纳:非金属元素氢化物的稳定性
与氢化物的反应热△H的关系
。
⑶ 硒化氢在热力学标准态下,发生分解反应的热化学反应方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com