
题目列表(包括答案和解析)
13.下列离子方程式中,正确的是
A.硫酸镁溶液和氢氧化钡溶液反应:SO42-+Ba2+ ==BaSO4↓
B.碳酸氢钙溶液跟稀硝酸反应:HCO3-+H+ == H2O + CO2↑
 C.偏铝酸钠的水溶液显碱性:AlO
C.偏铝酸钠的水溶液显碱性:AlO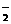 +2H2O Al(OH)3↓+OH–
+2H2O Al(OH)3↓+OH–
D.电解饱和食盐水: 2Cl-+2H+ H2↑+C12↑
H2↑+C12↑
12. 在室温下,某溶液中由H2O H++OH-这一途径产生出来的H+和OH-浓度的乘积为1×10-26,则此溶液中可能大量共存的离子组为
在室温下,某溶液中由H2O H++OH-这一途径产生出来的H+和OH-浓度的乘积为1×10-26,则此溶液中可能大量共存的离子组为
A.HCO3-、Al3+、H+、SO42- B.SiO32-、ClO-、Na+、K+
C.Cu2+、Cl-、NO3-、K+ D.I-、Fe3+、SCN-、NH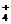
11.下列溶液中,能大量共存的离子组是
A.pH=7的溶液:Na+、Fe3+、Cl-、SO42-
B.c(H+)=1×10-2mol·L-1的溶液:Na+、NH4+、CO32-、SO42-
C.含有大量SO42-的溶液:K+、Cu2+、Cl-、NO3-
D.含有大量ClO-的溶液:H+、Mg2+、I-、SO42-
10.下列各组离子能大量共存,当溶液中c(H+)=10-1mol·L–1时,有气体产生;而当溶液中c(H+)=10–13mol·L-1时,又能生成沉淀。则该组离子可能是:
A.Na+、Cu2+、NO3-、CO32- B.Ba2+、K+、Cl-、HCO3-
C.Fe2+、Na+、SO42-、NO3- D.Mg2+、NH4+、SO42-、Cl-
9.下列离子在溶液中能大量共存,加入(NH4)2Fe(SO4)2·6H2O晶体后,仍能大量共存的是
A.Na+、H+、Cl-、NO3- B.K+、Ba2+、OH-、I-
C.Cu2+、 Fe3+、Br-、NO3- D.Na+、Mg2+、Cl-、SO42-
8.将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为
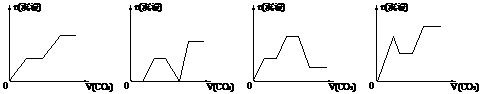
A B C D
7.Zn(OH)2是一种与A1(OH)3类似的两性氢氧化物,它与强碱反应的离子方程式为:Zn(OH)2+2OH– ==ZnO22–+2H2O。而且Zn(OH)2还能溶于过量的氨水,生成易溶于水的Zn(NH3)42+,而Al(OH)3不能。则下面四组溶液不能用相互滴加来进行鉴别的是
A.A1Cl3、NH3·H2O B.ZnCl2、NH3·H2O C.A1Cl3、NaOH D.ZnCl2、NaOH
6.某溶液含有①NO3-、②HCO3-、③SO32-、④CO32-、⑤SO42-等五种阴离子。向其中加入少量的Na2O2固体后,溶液中离子浓度基本保持不变的是(设溶液体积无变化)
A.① B.①②④ C.①③⑤ D.①③④⑤
5.下列各组离子可以大量共存,加入括号中试剂,整体可能形成无色澄清溶液的是
A.Na+、NH4+、Fe2+、NO3-(稀硫酸) B.Al3+、K+、HCO3-、NO3-(NaOH溶液)
C.NH4+、Ag+、K+、NO3-(NaOH溶液) D.Na+、K+、AlO2-、SiO32–(稀硝酸)
4.假设SiO2原子晶体中Si原子被Al原子取代,不足的价数由K原子补充。当有25%的硅原子被铝原子取代时,可形成正长石,则正长石的化学组成为
A.KAlSiO4 B.KAlSi2O6 C.KAlSi3O8 D. KAlSi4O10
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com