
题目列表(包括答案和解析)
7. 下列关于电解精炼铜的叙述中不正确的是
A. 精铜板:阴极
B. 电解时,阳极发生氧化反应,而阴极发生的反应为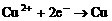
C. 粗铜中所含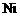 、
、 、
、 等杂质,电解后以单质形式沉积槽底,形成阳极泥
等杂质,电解后以单质形式沉积槽底,形成阳极泥
D. 电解铜的纯度可达 ~99.98%
~99.98%
6.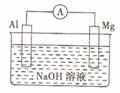 将Mg条、Al条平行插入一定浓度的NaOH溶液中,用电器连接成原电池。此电池工作时,下列叙述中正确的是
将Mg条、Al条平行插入一定浓度的NaOH溶液中,用电器连接成原电池。此电池工作时,下列叙述中正确的是
A. Mg比Al活泼,Mg失去电子被氧化成Mg2+
B. Al条表面虽有氧化膜,但可不必处理
C. 该电池的内、外电路中,电流均是由电子定向移动形成的
D. Al是电池负极,开始工作时溶液中会立即有白色沉淀析出
5. 用惰性电极电解下列溶液一段时间后,再加入一定量的另一种物质(方括号内),溶液能与原来溶液完全一样的是
A.  B.
B.  C.
C.  D.
D. 
4. 下列防腐措施中,属于电化学保护法的是
A. 用氧化剂使金属表面生成致密稳定的氧化物保护膜 B. 金属表面喷漆
C. 在金属中加入一些铬或镍制成金属合金 D. 在轮船的船壳水线以下部分,装上一锌锭
3. 关于电解NaCl水溶液,下列叙述正确的是
A. 电解时在阳极得到氯气,在阴极得到金属钠
B. 若在阳极附近的溶液中滴加KI溶液,溶液呈棕色
C. 若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D. 电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
2. 下列描述中,不符合生产实际的是
A. 电解熔融的氧化铝制取金属铝,用铁作阳极 B. 电解法精炼粗铜,用纯铜作阴极
C. 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 D. 在镀件上电镀锌,用锌作阳极
1. 用惰性电极电解下列溶液,电解一段时间后,阴极质量增加,电解液的pH下降的是
A. KI B. AgNO3 C. BaCl2 D. H2SO4
9(12分).已知反应:C(石墨) + O2(g) = CO2(g); DH = -393.13kJ×mol-1
2 CO(g) + O2(g) = 2 CO2(g);ΔH = -566 KJ·mol-1
(1)写出石墨与二氧化碳反应的热化学方程式:
_________________________________________________。
(2)若反应(1)(对应的二氧化碳为1mol)的DS = +175.3J×mol-1×K-1
①说明此反应的DS为正值的理由:____________________________。
②经计算298K时,此反应的DG=_______(填“>”、“=”、“<”)0
③此反应在____________________________℃(填计算式,不必计算出结果)以上,自发方向发生逆转。
10(20分).如图Ⅰ,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2 A(?)+B(?) x C(g);ΔH<0 平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。
x C(g);ΔH<0 平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。

⑴根据题中数据计算,x =_________、y =_________;
⑵如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol。由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
|
可能的情形 |
A、B是否为气态 |
z与y的大小关系 |
M(B)与M(C)的大小关系 (M表示摩尔质量) |
|
|
A |
B |
|||
|
① |
是 |
不是 |
z = y |
无法确定 |
|
② |
|
|
|
|
|
③ |
|
|
|
|
11(20分).在TK、300MPa时,往容积可变的密闭容器中充入 1molN2、3molH2,此时,容器的体积为200L。向容器中加入催化剂(铁触媒)并保持恒温恒压,发生反应:N2 (g)+ 3H2(g)
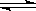 2NH3(g),达到平衡时 NH3的体积分数为1/3。
2NH3(g),达到平衡时 NH3的体积分数为1/3。
试回答下列问题:
(1)保持上述温度和压强不变,若向容器中只充入2molNH3,并加入铁触媒催化剂。则平衡时,N2的体积分数是_____________,容器的体积为_________。
(2)保持上述温度不变,在200L的定容容器中进行合成氨反应,改变起始时原料气的充入量,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应N2 (g)+ 3H2(g)
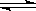 2NH3(g) V(N2)正 3V(H2)逆
2NH3(g) V(N2)正 3V(H2)逆
(填:“>”、“<”、“=”、“不能确定”)
(3)温度仍保持TK,容器体积保持200L不变(恒容)。充入amolN2,bmolH2,并加入铁触媒催化剂,反应达到平衡时,NH3的体积分数仍为1/3,体系压强为300MPa。若a:b=1:3,则a=_______________mol。
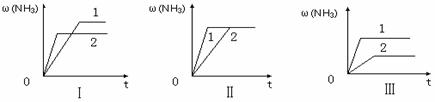
(4)在三个相同容器中各充入1 molN2和3molH2,在某一不同条件下反应并达到平衡,氨的体积分数随时间变化曲线如下图。下列说法正确的是__________
(填序号)。
A.图Ⅰ可能是不同催化剂对反应的影响,且催化剂性能 2>1
B.图Ⅱ可能是同温同压下,不同催化剂对反应的影响,且催化剂性能1>2
C.图Ⅱ可能是不同压强对反应的影响,且P1>P2
D.图Ⅲ可能是不同温度对反应的影响,且T1>T2
8.在一条件下,可逆反应2A(气)+B(气)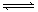 n(C)(固)+D(气)
n(C)(固)+D(气)
达到平衡。若维持温度不变,增大强压,测得混合气体的平均相对分子质量不发生改变,则下列判断正确的是 ( )
A.其它条件不变,增大压强,平衡不发生移动
B.其它条件不变,增大压强,混合气体的总质量不变
C.反应可以从正反应开始,也可以从逆反应开始,但必须满足下列条件:
其中x、y、z分别表示第一次达到平衡时, A、B、D的物质的量(mol),(其中M表示物质的摩尔质量,下同)

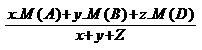 =
=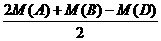
D.反应只能从正反应开始,且原混合气中A与B的物质的量之比为2:1,并有
班次________ 姓名__________ 计分_________
7.为比较 和
和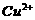 对
对 分解反应的催化效果,甲乙两组同学分别设计了如图中甲、乙所示的实验。下列叙述不正确的是 ( )
分解反应的催化效果,甲乙两组同学分别设计了如图中甲、乙所示的实验。下列叙述不正确的是 ( )
A.图甲实验可通过观察产生气泡快慢来比较反应速率的大小
B.若图甲所示实验中反应速率①>②,则一定说明 比
比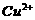 对
对 分解催化效果好
分解催化效果好
C.用图乙装置测定反应速率,可测定反应产生的气体体积及反应时间.
D.为检查图乙装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com