
题目列表(包括答案和解析)
17.锌片和铁片放在盛有稀食盐水和酚酞混合液的U型管中,如图所示,
最终可在A极观察到酚酞变红。写出电极名称反应式和总反应式。
16.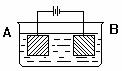 按图示装置进行实验:A极是铜锌合金,B极为纯铜,电解质中含有足量的铜离子。通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,
按图示装置进行实验:A极是铜锌合金,B极为纯铜,电解质中含有足量的铜离子。通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,
溶液质量增加0.03g,则A合金中Cu、Zn原子个数比为
A. 4∶1 B. 3∶1 C. 2∶1 D.任意比
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
15.以铁为阳极、铜为阴极,对足量的NaOH溶液进行电解,一段时间后得到2mol
Fe(OH)3沉淀,此时消耗水的物质的量共为
A. 6mol B. 3mol C. 4mol D. 5mol
14.固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,其工作原理如图所示。下列关于固体燃料电池的有关说法正确的是
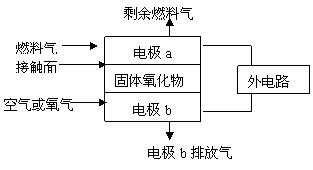
固体氧化物燃料电池的工作原理示意图
A.电极b为电池负极,电极反应式为O2+4e- ==2O2-
B.固体氧化物的作用是让电子在电池内部通过
C.若H2作为燃料气,接触面上发生的反应为: H2+2OH--2e-=2H2O
D.若C2H4作为燃料气,接触面上发生的反应为:C2H4+6O2--12e-=2CO2+2H2O
13. 1L0.1mol/LAgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极增重2.16g时。下列判断(设电解按理论进行,溶液不蒸发) 正确的是:
A. 溶液的浓度变为0.08mol/L B. 阳极上产生112mLO2(标准状况)
C. 转移的电子数是1.204×1022个 D. 反应中有0.01mol的Ag被氧化
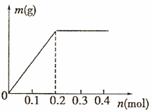
12.用Pt电极电解含有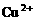 和
和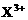 均为0.1 mol的溶液,阴极析出金属的质量m(g)与溶液中通过电子的物质的量n(mol)关系如图,则离子的氧化能力由大到小排列正确的是
均为0.1 mol的溶液,阴极析出金属的质量m(g)与溶液中通过电子的物质的量n(mol)关系如图,则离子的氧化能力由大到小排列正确的是
 A.
A.
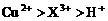
B. 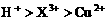
C. 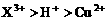
D. 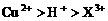
11. 将铁片和银片用导线联接插入硫酸铜溶液中,当线路中有0.2mol的电子发生转移时,负极的质量变化是
A.减少0.8g B. 增加6.4g C. 减轻5.6g D. 增加5.6g
10. 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
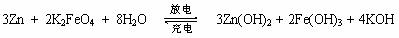
下列叙述不正确的是
A. 放电时负极反应为:Zn - 2e- + 2OH- == Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3 - 3e- + 5OH- == FeO42- + 4H2O
C. 放电时每转移3moL电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
9. 甲、乙两个电解池均以Pt为电极且互相串联。甲池盛有AgNO3溶液,乙池盛有一定量的某盐溶液,通电一段时间后,测得甲池阴极质量增加2.16g,乙池电极析出0.64g金属,则乙池中溶质可能是
A. CuSO4 B. MgSO4 C. Al(NO3)3 D. Na2SO4
8. 将两个铂电极插入500mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重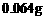 (设电解时该电极无氢气析出,且不考虑水解和溶液体积的变化)。此时溶液中氢离子浓度约为
(设电解时该电极无氢气析出,且不考虑水解和溶液体积的变化)。此时溶液中氢离子浓度约为
A. 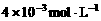 B.
B.  C.
C. 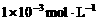 D.
D. 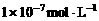
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com