
题目列表(包括答案和解析)
4.Na2O2、CaC2、CaH2、Mg3N2都能与水反应,且反应中均有气体放出。下列说法中正确的是
A.都属于氧化还原反应
B.CaC2、Mg3N2与水反应属于复分解反应
C.Na2O2、CaH2与水反应时水作氧化剂
D.CaH2与水反应时产生H2,它是氧化产物和还原产物
3.氯气跟碘在加热条件下,以等物质的量进行反应,可得到一种红棕色液体ICl。ICl有很强的氧化性,ICl跟Zn、H2O反应的化学方程式为:
2ICl+2Zn===ZnCl2+ZnI2
ICl+H2O===HCl+HIO
下列叙述中正确的是
A.ZnCl2既是氧化产物,又是还原产物
B.ICl跟H2O的反应是自身氧化还原反应
C.ZnI2既是氧化产物,又是还原产物
D.在ICl跟H2O的反应中,ICl是氧化剂,H2O是还原剂
2.在一定温度下,NH4NO3分解的化学方程式为:5NH4NO3 2HNO3+4N2+9H2O在此反应中被氧化和被还原的氮原子数之比是
2HNO3+4N2+9H2O在此反应中被氧化和被还原的氮原子数之比是
A.5∶3 B.5∶4 C.1∶1 D.3∶5
1.(2002年全国高考题)R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应;X2++Z===X+Z2+;Y+Z2+===Y2++Z。这四种离子被还原成0价时表现的氧化性大小符合
A.R2+>X2+>Z2+>Y2+
B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+
D.Z2+>X2+>R2+>Y2+
17.(10分)取两种钠的正盐A和B,溶于1 L 0.2 mol·L-1的盐酸溶液得淡黄色固体C和溶液D(溶液体积仍为1 L,下同)。过滤分离出固体C,经洗涤、干燥后在空气中燃烧,把生成的1/3量的气体E导入溶液D又得固体物C(其质量和前一次得到的相同)和溶液F。F中氢离子浓度为0.01 mol·L-1。向F中加A或B,或导入气体E,均未见有固体物生成。
(1)A、B、C、E各为何物?
(2)溶液D、F中各含哪些物质?它们的物质的量浓度各为多少?
(3)写出有关反应方程式。
16.(8分)某待测溶液(阳离子为Na+)中可能会有SO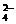 、S2-、SO
、S2-、SO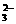 、Cl-、Br-、NO
、Cl-、Br-、NO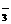 、CO
、CO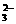 、HCO
、HCO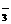 中的一种或若干种。进行下列实验(如下图所示)(每次实验所加试剂均过量):
中的一种或若干种。进行下列实验(如下图所示)(每次实验所加试剂均过量):

回答以下问题:
(1)待测液是否含有SO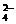 、SO
、SO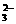 ?答:
?答:
(2)沉淀B的化学式为 。
(3)根据以上实验,待测液中肯定没有的离子是 ,肯定存在的离子是 。
15.(6分)已知硫和氧同族,性质相似,请用化学方程式解释下列实验现象:
(1)CS2和Na2S水溶液一起振荡,水溶液由无色变有色 。
(2)P2S5溶于K2S水溶液中 。
(3)Na2S2溶液中加稀HCl产生浅黄色沉淀 。
14.(8分)(1)将m g铁粉和n g硫粉均匀混合,在密闭容器中加热到红热,冷却后加入多少毫升b mol·L-1的盐酸就不再产生气体?若把已放出的气体收集起来,在标准状况下的体积共是多少升?
(2)若把0.1 mol铁粉和1.6 g硫粉均匀混合后,铺在石棉网上用酒精灯加热引燃,完全反应后将残渣全部放入过量的稀H2SO4中充分反应,结果所产生的气体体积在标准状况下明显少于2.24 L,简述其原因。
13.(4分)将a g硫粉随机分成两份,第一份与足量O2反应制得SO2,第二份先与足量铁混合加热,再将所得产物投入稀H2SO4中,得H2S。将SO2与H2S混合,结果得硫a/3 g,求第一份的质量。
12.(6分)今有五种硫的化合物①H2S ②K2S ③Al2S3 ④CuS ⑤FeS,其中(填序号):
(1)不能由两种单质化合而成,只能在溶液中由两种离子反应而生成的是 。
(2)只能由两种单质化合而成,不能在溶液中由两种离子反应生成的是 。
(3)既能由两种单质化合生成,又能在溶液中由两种离子反应生成的是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com