
题目列表(包括答案和解析)
8. 答案解析:(易)考查对物质的量、阿伏加德罗常数相关知识的理解,答案:C。物质的摩尔质量单位是“g·mol-1”,物质的质量单位是“g”,A不正确;B中转移电子数应为2NA;500mL 0.5mol·L-1Al2(SO4)3溶液中,SO42-的物质的量为3×0.5mol·L-1×0.5L=0.75mol,含SO42-数目为0.75NA,C正确。0.5NA个氧气分子为0.5mol ,在标准状况下所占的体积为0.5mol×22.4 L·mol-1 =11.2L,但常温常压下要比11.2L 略大,D不正确。
8.设NA为阿伏加德罗常数,下列说法中正确的是( )
A.Cl2的摩尔质量与NA个Cl2分子的质量在数值和单位上都相等。
B.活泼金属从盐酸中置换出1molH2,转移电子数为NA
C.500mL0.5mol·L-1Al2(SO4)3溶液中,含SO42-数目为0.75NA
D.常温常压下,0.5 NA个一氧化碳分子所占体积是11.2L
7. 答案解析:(中难)考查元素周期表(长式)的结构(周期、族)及其应用,答案:C。L层电子数为奇数的有锂、硼、氮、氟4种元素,锂是金属,硼、氮、氟是非金属。第三、四、五、六周期元素的数目分别是8、18、18、32。由左至右第8、9、10三列为Ⅷ族,是过渡元素,都是金属。最外层电子数为2的除第ⅡA族外,还有零族的He以及某些过渡元素。
7.根据中学化学教材所附元素周期表判断,下列叙述正确的是( )
A.L电子层为奇数的所有元素都是非金属
B.第三、四、五、六周期元素的数目分别是8、18、32、32
C.由左至右第8、9、10三列元素中没有非金属元素
D.只有第ⅡA族元素的原子最外层有2个电子
6. 答案解析:(易)考查物质的分类知识,答案:D。明矾[KAl(SO4) 2·12H2O]、胆矾(CuSO4·5H2O)、石膏(CaSO4·2H2O)等结晶水水合物有一定的组成,是纯净物。玻璃是多种硅酸盐的混合物;冰是水的固态,是纯净物;蔗糖有固定的组成(C12H22O11),是纯净物;天然橡胶是高分子化合物,一般来说,高分子化合物都不是纯净物,天然物质通常含有多种物质。王水是硝酸和盐酸的混合物。弱酸H2SiO3、H2CO3是弱电解质;NaHCO3是强电解质;SO2、CO2、CH3CH2OH、NH3非电解质;Cl2是单质,既不是电解质也不是非电解质。
6.下列表中对于相关物质的分类全部正确的一组是
|
编号 |
纯净物 |
混合物 |
弱电解质 |
非电解质 |
|
A |
明矾 |
蔗糖 |
NaHCO3 |
CO2 |
|
B |
天然橡胶 |
石膏 |
SO2 |
CH3CH2OH |
|
C |
冰 |
王水 |
H2SiO3 |
Cl2 |
|
D |
胆矾 |
玻璃 |
H2CO3 |
NH3 |
15.(9分)一定质量的氯酸钾与二氧化锰的混合物加热至无气体放出时,将残余的固体与足量的浓硫酸共热,并把此时生成的气体通入500 mL某浓度的亚硫酸钠溶液中,设气体被完全吸收且无SO2逸出,也无游离氯分子存在,测得溶液的pH=0(不计溶液体积变化),最后向溶液中加入足量的BaCl2溶液,生成不溶于酸的白色沉淀16.31 g。求原混合物中氯酸钾、二氧化锰的质量及亚硫酸钠溶液的物质的量浓度。
14.(5分)用纯度为92.5%(杂质不与Cl2反应)的消石灰与Cl2反应制漂白粉,消石灰的转化率为80%,要求某游泳池消毒一次需要4.26 kg Cl2,现改用上述漂白粉,假定起消毒作用的是HClO,要达到与Cl2相当的消毒效果,需向游泳池中投放这种漂白粉多少千克?
13.(10分)KClO3和浓盐酸在一定温度条件下反应会生成黄绿色的易爆物二氧化氯,其变化可表示为:
KClO3+ HCl(浓)-- KCl+ ClO2↑+ Cl2↑+
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)。
(2)浓盐酸在反应中显示出来的性质是 (填写序号)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)产生0.1 mol Cl2,则转移的电子的物质的量为 mol
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的多少倍?
12.(12分)用下图所示装置(酒精灯、铁架台等未画出)制取三氯化磷,在短颈分馏烧瓶d中放入足量白磷,将Cl2迅速而又不间断地通入d中,氯气与白磷会发生反应,产生火焰。
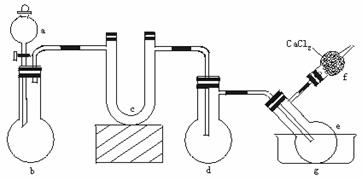
物质制备装置
三氯化磷和五氯化磷的物理常数如下表。
物质熔沸点
|
|
熔点 |
沸点 |
|
三氯化磷 |
-122℃ |
76℃ |
|
五氯化磷 |
148℃ |
200℃分解 |
图中,a,b应该装入的试剂或药品分别是浓盐酸和二氧化锰,在b仪器处加热。请据此回答下列回答:
(1)在蒸馏烧瓶e中收集生成的三氯化磷,为保证三氯化磷蒸气冷凝,应在水槽g中加入 。
(2)三氯化磷遇到水蒸气强烈反应,甚至发生爆炸,所以d,e仪器及装入其中的物质都不能含有水分。为除去Cl2中的水分,c中应装入 作干燥剂。
(3)实验室将白磷保存于水中,取出的白磷用滤纸吸干表面水分,浸入无水酒精中片刻,再浸入乙醚中片刻即可完全除去水分。已知水与酒精互溶,酒精与乙醚互溶,乙醚极易挥发,用上述方法除去水分的原因是 。
(4)为防止Cl2污染空气,装置末端导出的气体应如何净化处理,画出装置图并注明使用药品: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com