
题目列表(包括答案和解析)
26、(10分)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
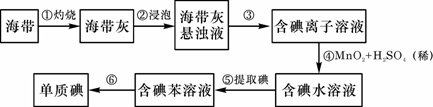
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架、酒精灯外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法: 。
25、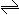 (6分)在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
(6分)在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1) 计算20s一40s内用N2O4表示的平均反应速率为 mol· L-1·S-1;
(2) 计算在80℃时该反应的平衡常数K= (请注明单位)。
(3) 反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”、“变深”
或“不变”) ;
(4) 要增大该反应的K值,可采取的措施有(填序号) :
 A.增大N2O4的起始浓度 B.向混合气体中通入NO2
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
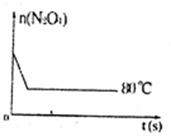
(5) 如图是80℃时容器中N204物质的量的变化曲线,请在该图中补画出该反应在60℃时N204物质的量的变化曲线。
24、(9分)CuS难溶于水,不溶于一般稀酸。在某反应体系中的物质有:H2O、NO、CuS、S、HNO3、Cu(NO3)2。
(1)请将NO之外的反应物与生成物分别填入以下空格内:

+ + + + NO
(2)反应中,被还原的元素是 ,还原剂是 。
(3)反应中1mol氧化剂 (填“得到”或“失去” ) mol电子。
(4)将氧化剂与还原剂填入下列空格中,并标出电子转移的方向和数目。
+ ……
23、(9分)元素周期表是学习化学的重要工具,它饮食许多信息和规律。下表所列是五种短周期的原子半径及主要化合价:
|
元素代号 |
A |
B |
C |
D |
E |
|
原子半径/m |
0.16 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6,-2 |
+2 |
-2 |
(1)用元素代号标出它们的周期表中对应位置
(2)在上面的元素周期表中通常寻找催化剂材料的区域,用粗线标出。
(3)五种元素中非金属性最强的是 (填元素符号),C、E形成化合物为 (填化学式)
(4)证明B元素与A元素在性质上有明显不同的离子方程式为
22、用NA表示阿伏加德罗常数,下列说法中不正确的是 ( )
A. 常温常压下,活泼金属从盐酸中置换出1 mol H2,发生转移的电子数为2NA
B. 醋酸的摩尔质量与NA个醋酸分子的质量在数值上相等
C. 在标准状况下,22.4L的HF所含分子数为NA
D. 在标准状况下,a g某气体含分子数为b,c g该气体的体积为22.4bc /aNA升
第Ⅱ卷 (非选择题,共84分)
21、将0.2mol/LNaA溶液和0.1mol/L盐酸等体积混全后,溶液pH>7,则以下关系式错误的是 ( )
|
B.c(A-)>c(HA)
C.c(Na+)+c(H+)=c(A-)+c(C1-)+c(OH-)
D.c(Na+)=c(A-)+c(HA)
20、下列离子方程式的书写正确的是 ( )
A.实验室用浓盐酸与MnO2反应制Cl2:
MnO2 +2H++2Cl- →Cl2↑+Mn2+ +H2O
B.将标准状况下1.12 L氯气通入10 mL 1 mol / L的溴化亚铁溶液中:
2Fe2++4Br-+3Cl2 →2Fe3++6Cl-+2Br2
C.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:
Ca2++ HCO3- +OH- →CaCO3↓+H2O
D.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+H++ SO42- + NH4+→BaSO4↓+ NH3·H2O +H2
19、已知反应BeCl2+Na2BeO2+2H2O→2NaCl+2Be(OH)2↓能完全进行,则下列推断中正确的是 ( )
A. BeCl2溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO
B. Na2BeO2溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO
C. Be(OH)2既能溶于盐酸又能溶于烧碱溶液
D. BeCl2水溶液的导电性强,因此BeCl2一定是离子化合物
18、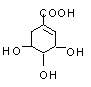 莽草酸是制取抗甲型H1N1流感药物“达菲”的中间活性物质,其结构简式如图所示。它不可能存在下列类别的同分异构体
( )
莽草酸是制取抗甲型H1N1流感药物“达菲”的中间活性物质,其结构简式如图所示。它不可能存在下列类别的同分异构体
( )
A. 酚类 B. 醛类 C. 醇类 D. 酯类
17、已知: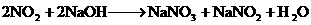 ;
;
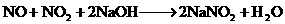 。将224 mL(SPT)NO和
。将224 mL(SPT)NO和 的混合气体溶于20 mL NaOH溶液中,恰好完全反应并无气体逸出,则NaOH溶液的物质的量浓度为 ( )
的混合气体溶于20 mL NaOH溶液中,恰好完全反应并无气体逸出,则NaOH溶液的物质的量浓度为 ( )
A. 1 mol/L B. 0.5mol/L C. 0.25mol/L D. 0.2mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com