
题目列表(包括答案和解析)
7.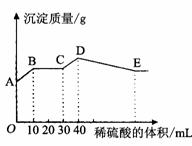 将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol·L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示。下列有关判断正确的是
将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol·L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示。下列有关判断正确的是
A.A点所表示的沉淀的化学式是: Al(OH)3、 BaSO4
B.B~C段所发生反应的离子方程式是:H+ + OH- = H2O
C.A~B段所发生反应的离子方程式是:Ba2+ + SO42- =BaSO4↓
D.E点所表示的溶液中:n (Na+) = n (Cl-)
6.某酸式盐NaHY的水溶液显碱性,下列叙述正确的是
 A.H2Y的电离方程式:H2Y 2H++Y2-
A.H2Y的电离方程式:H2Y 2H++Y2-
B.该酸式盐溶液中离子浓度关系:c(H+)+c(Na+)=c(OH-)+c(Y2-)+c(HY-)
C.该酸式盐溶液中离子浓度关系:c(H+)+ c(H2Y) =c(OH-)+c(Y2-)
D.该酸式盐溶液中离子浓度大小关系: c(Na+)> c(OH-)> c(H+)>c(HY-)
5.在加入铝粉产生氢气的溶液中,下列各组离子可能大量共存的是
A.NH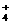 、NO
、NO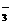 、CO
、CO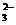 、Na+
、Na+
B.Ba2+、Mg2+、HCO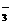 、Na+
、Na+
C.H+ 、F一、K+ 、Cl-
D.K+ 、AlO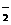 、OH一、NO
、OH一、NO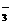
4.由两种短周期元素A和M形成的离子化合物A2M3,A3+离子比M2-离子少一个电
子层,且A3+具有与Ne原子相同的核外电子层结构,则下列说法正确的是
A.化合物A2M3是三氧化二铝
B.A3+和M2-最外电子层上的电子数都是8
C.A的最高价氧化物对应的水化物是强电解质
D.元素M是第2周期第VIA族的元素
3.下列实验操作和事故处理中,正确的是
A.银镜反应实验后附有银的试管,可用稀硫酸洗涤
B.在中学“硫酸铜晶体中结晶水含量测定”的实验中称量操作致少需要四次
C.不慎将浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
D.在250mL烧杯中,加入216mL水和24gNaOH固体,配制10%NaOH溶液
2.若NA表示阿伏加德罗常数的值,下列说法正确的是
A.2.3g Na在足量的O2中完全燃烧和与在空气中缓慢反应完全,转移的电子数均为0.1NA
B.11.2L Cl2所含的原子数为NA
C.化学上定义12g 碳中的碳原子数为NA的数值
‥
D.17g .O︰H中所含电子数为7NA
‥
1.用右图表示的一些物质或概念之间的从属或包含关系中不正确的是
|
|
X |
Y |
|
||
|
例 |
氧化物 |
化合物 |
纯净物 |
||
|
A |
苯 |
芳香烃 |
有机化合物 |
||
|
B |
溶液 |
分散系 |
混合物 |
||
|
C |
强电解质 |
电解质 |
化合物 |
||
|
D |
置换反应 |
氧化还原反应 |
离子反应 |
10.一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:
 2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
A.以X浓度变化表示的反应速率为0.001mol·L-1·s-1
B.其它条件不变,将容器体积变为20L,Z的平衡浓度变为原来的1/2
C.其它条件不变,若增大压强,则物质Y的转化率减小
D.其它条件不变,若升高温度,X的体积分数增大,则该反应的△H>0
9.一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
① CH4 (g)+4NO2 (g)=4NO (g) +CO2 (g)+2H2O (g) ;△H=―574 kJ·mol-1
② CH4 (g)+4NO (g)=2N2 (g)+CO2 (g)+2H2O (g) ;△H=―1160 kJ·mol一1。
下列选项正确的是
A.CH4 (g)+2NO2 (g)= N2 (g)+CO2 (g)+2H2O (l) ;△H=―867 kJ·mol-1
B.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ
C.CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子为3.2 mol
D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为1.6 mol
8.常温下,0.1mol·L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是
A.该溶液中由水电离出的c(H+)=1×10-3 mol·L-1
B.由pH=3的HA与pH=11的NaOH溶液等体积混合,溶液中c(Na+)>c(A-)>c(OH-)>c(H+)
C.浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,则
c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-)
D.0.1mol·L-1HA溶液与0.05mol·L-1NaOH溶液等体积混合后所得溶液中
2c(H+)+c(HA)=c(A-)+2c(OH-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com