
题目列表(包括答案和解析)
8.下列比较中,正确的是( )
A.常温下,同浓度的一元酸HA比HB易电离,则相同浓度的NaA溶液比NaB溶液的pH大
B.0.2 mol/L NH4NO3 和 0.l mol/L NaOH 溶液等体积混合后:
c(NH4+)>c(NO3-)>c(Na+)>c(OH-)>c(H+)
C.物质的量浓度相等的醋酸溶液和氢氧化钠溶液等体积混合:
c(Na+)+c(H+)=c(CH3COO-)+c(OH-)+c(CH3COOH)
D.同浓度的下列溶液:①NH4Al(SO4)2;②NH4Cl;③NH3·H2O;④CH3COONH4
其中c(NH4+) 由大到小的顺序是:①>②>④>③
7.从下列事实所得出的相应结论正确的是( )
|
|
实验事实 |
结论 |
|
① |
Cl2的水溶液可以导电 |
Cl2是电解质 |
|
② |
将燃烧的镁条放入CO2中能继续燃烧 |
还原性:Mg>C |
|
③ |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
|
④ |
某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 |
该溶液一定有NH4+ |
A.③④ B.②④ C.①② D.全部
6.下列实验操作正确的是( )
A.将10 mL饱和FeCl3溶液与10 mL沸水混合,可制得Fe(OH)3胶体
B.向2 mL浓硫酸中加入3 mL乙醇和2 mL乙酸,充分混合并加热,制备乙酸乙酯
C.配制100 mL 1 mol/L NaOH溶液的过程中,将4 g NaOH在烧杯中溶解,冷却后再转移到
100 mL容量瓶中
D.取加热至亮棕色的纤维素水解液,滴入新制Cu(OH)2悬浊液并加热,检验水解产物是否具有还原性
5.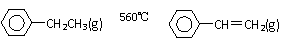 工业生产苯乙烯是利用乙苯的脱氢反应:
工业生产苯乙烯是利用乙苯的脱氢反应:
 +H2(g);△H<0
+H2(g);△H<0
针对上述反应,在其它条件不变时,下列说法正确的是( )
A.加入适当催化剂,可以提高苯乙烯的产量
B.在保持体积一定的条件下,充入较多的乙苯,可以提高乙苯的转化率
C.仅从平衡移动的角度分析,工业生产苯乙烯选择恒压条件优于恒容条件
D.加入乙苯至反应达到平衡过程中,混合气体的平均相对分子质量不断增大
4.某晶体由两种阳离子、一种阴离子和结晶水组成,取少量该晶体进行如下实验:
①将晶体置于试管中加热,试管口有无色液体生成; ②待试管冷却后加水,固体全部溶解;
③向试管中逐滴加入Ba(OH)2溶液至过量,同时加热,生成沉淀的量先增多后减少,最终仍有沉淀未溶解,此过程中有刺激性气味气体生成。
根据以上实验现象判断,该晶体是( )
A.NH4Al(SO4)2·12H2O B.KAl(SO4)2·12H2O
C.(NH4)2Fe(SO4)2·6H2O D.KCl·MgCl2·6H2O
3.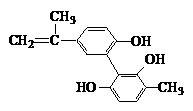 “人文奥运”是2008年北京奥运会的重要特征,其中禁止运动员使用兴奋剂是其重要举措之一。以下是两种兴奋剂的结构简式,下列说法正确的是( )
“人文奥运”是2008年北京奥运会的重要特征,其中禁止运动员使用兴奋剂是其重要举措之一。以下是两种兴奋剂的结构简式,下列说法正确的是( )

利尿酸 兴奋剂X
A.兴奋剂X的化学式为C16H15O3
B.两者均能与酸性高锰酸钾溶液和氢氧化钠溶液反应
C.两者均为芳香族化合物,均能发生消去反应
D.1 mol兴奋剂X最多可与含4 mol Br2的浓溴水和6 mol H2反应
2.阿伏加德罗常数约是6.02×1023 mol-1,下列说法正确的是( )
A.20 g D2O中含有的中子数是8×6.02×1023
B.1 mol乙醇分子中所含共价键数是7×6.02×1023
C.标准状况下22.4L氧气和二氧化碳混合气中所含的氧原子数是2×6.02×1023
D.71 g Cl2制备漂白粉[有效成分Ca(ClO)2]时转移电子数是2×6.02×1023
1.下列叙述正确的是( )
A.鸡蛋白溶胶中加入饱和硫酸铵溶液后有蛋白质析出
B.直径介于1nm ~ 100nm之间的微粒称为胶体
C.根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
D.电泳现象可证明胶体属于电解质溶液
8.常温下,下列各溶液中微粒的物质的量浓度关系正确的是( )
A.0.1 mo1·L-1的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
B.0.1 mol·L-1的NH4Cl溶液与0.05mol·L-l的NaOH溶液等体积混合后,得到的pH>7的溶液中:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
C.浓度分别为0.1 mol·L-1和0.01 mol·L-1的CH3COOH溶液中:CH3COO﹣离子浓度前者是后者的10倍
D.浓度均为0.1mol·L-1的苯酚钠溶液和CH3COONa溶液中:阴离子总浓度前者小于后者
选择题练习(6)
7.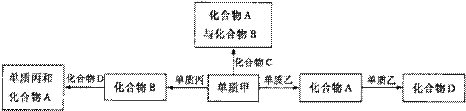 化合物A、B、C、D各由两种元素组成,甲、乙、丙是前两周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的是( )
化合物A、B、C、D各由两种元素组成,甲、乙、丙是前两周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的是( )
A.上图所示的五个转化关系中,有三个是化合反应
B.上述转化关系所涉及的化合物中有一种是电解质
C.甲、乙、丙三种单质的晶体一定是分子晶体
D.上图所示的五个转化关系中,均为氧化还原反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com