
题目列表(包括答案和解析)
4、已知25℃、101Kpa下,石墨、金刚石燃烧的热化学方程式分别为:
C(石墨)+O2(g)=CO2(g) △H= -393.51KJ/mol
C(金刚石)+O2(g)=CO2(g) △H= -395.41KJ/mol
据此判断,下列说法正确的是
①由石墨制备金刚石是吸热反应 ②由石墨制备金刚石是放热反应 ③等质量时,石墨的能量比金刚石的低 ④等质量时,石墨的能量比金刚石的高。
A、①③ B、①④ C、②③ D、②④
3、下列各组物质各自形成的晶体,均属于分子晶体的化合物的是
A.NH3、HD、C10H8 B.PCl3、CO2、H2SO4
C.SO2、SiO2、P2O5 D.CCl4、Na2S、H2O2
2、在镀锌铁皮的锌镀层厚度的测定过程中,下列操作会导致测定结果偏高的是
A.过早判断反应终点 B.在测定铁皮的面积时测得面积比铁皮的实际面积大
C.过迟判断反应终点 D.锌在酸中溶解后,铁皮未烘干就去称重
1、下列物质中不能通过置换反应生成的是 A.F2 B.CO C.Fe 3O4 D.S
74、(天津一中2010届高三上学期第三次月考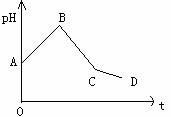 ,23)
,23)
I. 有机化合物A 一E的转化如下列反应框图所示,1molA和2molH2在一定条件下恰好反应,生成饱和一元醇X,X中碳元素的质量分数为65%。
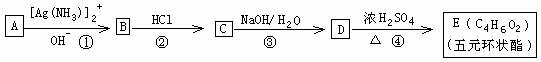
(1)X的分子式为____________________
(2)A分子中所含官能团的名称是_____________________________
(3)上述转化①一④步反应中,属于取代反应类型的是__________________
(4)C的结构简式为_________________________
(5)D→E的反应方程式为_________________________________
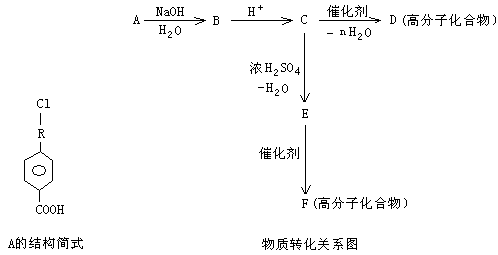 II 有机物A的相对分子质量为198.5,其结构简式如下(-R-代表某种烷基),已知在光照条件下,A分子中的一个氢原子被氯原子取代时只得到一种产物,A在一定条件下还有下图所示的反应关系:
II 有机物A的相对分子质量为198.5,其结构简式如下(-R-代表某种烷基),已知在光照条件下,A分子中的一个氢原子被氯原子取代时只得到一种产物,A在一定条件下还有下图所示的反应关系:
(1)A的分子式为______________
(2)A→B的化学方程式为________________________________________________
(3)写出E中所含官能团的名称____________________;C→D的反应类型_________________
(1) C4H10O 1分
(2)醛基 碳碳双键 各1分
(3) 3、4 2分
(4)CH2Cl CH2 CH2CH2COOH 2分
(5)HOCH2 CH2
CH2CH2COOH 
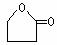 + H2O 2分
+ H2O 2分
(1)C10H11O2Cl 2分
(2)
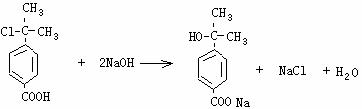
2分
(3)碳碳双键 羧基 各1分
聚合反应(缩聚反应) 1分
|

|
版权所有:()
版权所有:()
73、(哈尔滨三中、东北育才、大连育明、天津耀华2010年四校第一次联考,38)柠檬酸三丁酯(TBC)是绿色环保的增塑剂,应用极其广泛,它的结构式如左下图,
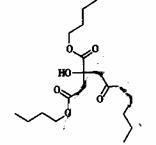
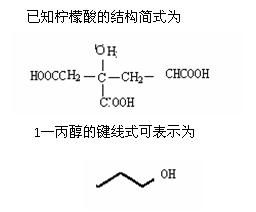
试回答:
(1)TBC的分子式为 ,在研究TBC的结构时要用到一种谱图(如下),用于推测 等信息,它是 图(填序号);
A.核磁共振氢谱 B.红外光谱 C.质谱

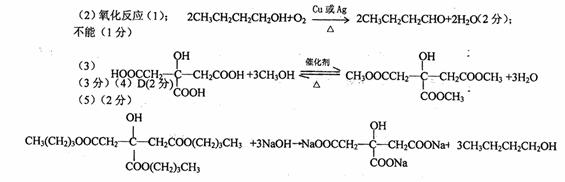
(2)1-丁醇在一定条件下可生成1-丁醇,反应类型为 ,化学方程式为 ,TBC在该条件下 (填“能”或“不能”)生成含醛基的化合物;
(3)柠檬酸与甲醇反应生成柠檬酸三甲酯的化学方程式 ;
(4)合成TBC时,不同条件对酯化学率的影响如下表:
|
n(酸):n(醇) |
1:5.0 |
1:5.5 |
1:6.0 |
1:6.5 |
1:7.0 |
|
酯化率/% |
95.1 |
96.3 |
97.0 |
97.4 |
97.2 |
|
时间/h |
0.5 |
1.0 |
2.0 |
3.0 |
5.0 |
|
酯化率/% |
40.0 |
70.2 |
94.3 |
97.4 |
97.4 |
|
温度/°C |
130 |
140 |
145 |
150 |
160 |
|
酯化率/% |
89.5 |
96.2 |
97.4 |
97.4 |
97.2 |
酯化反应时应选择的条件如下:它们分别是n(酸):(醇)、时间、温度,其中最佳的是: (填序号)。
A.1:5,1h,130° B.1:5.5,1h,140°C
C.1:7,2h,160°C D.1:6.5,3h,145°C
(5)TBC与足量NaOH溶液反应的化学方程式: 。
(1)C18H32O7(1分);化学键或官能团(2分);B(1分)
72、(2010届佛山市普通高中高三教学质量检测一,33)
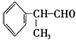
氢化阿托醛是一种重要的化工原料,其合成路线如下:
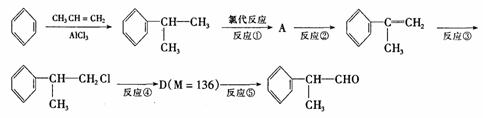
(1)氢化阿托醛被氧化后的含氧官能团的名称是 。
(2)在合成路线上②③的反应类型分别为② ③ 。
(3)反应④发生的条件是 。
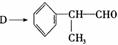
(4)由 反应的化学方程式为 。
(5)1mol氢化阿托醛最多可和______mol氢气加成,1mol氢化阿托醛发生银镜反应可生成__________molAg。
(6)D与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的结构简式为 。D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有 种。
(1)羧基…………(2分) (2)消去反应 加成反应……………(各1分共2分)
(3)NaOH溶液加热……………(2分)
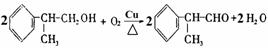
(4) ……………………………(2分)
(5)4 ; 2 (6)CH3COOH ; 6 ……………………………… (以上每空2分)
71、(江苏省江浦高级中学2010届高三模块复习,21)
 A、B、C、D、E、F是元素周期表前四周期的元素,它们在元素周期中的位置如下图所示:
A、B、C、D、E、F是元素周期表前四周期的元素,它们在元素周期中的位置如下图所示:
⑴写出F的基态原子核外电子排布式:__________________。
⑵C元素的第一电离能比同周期相邻的两种元素的第一电离能都高的原因是__________。
⑶由A、B、D三种元素形成的一种物质俗称光气,分子中A原子采取sp2杂化成键。光气分子的结构式是___________,其中碳氧原子之间共价键是_____(填序号):
 a.2个σ键 b.2个π键 c.1个σ键、1个π键
a.2个σ键 b.2个π键 c.1个σ键、1个π键
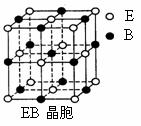
⑷EB晶胞如右下图所示,EB晶体中E2+的配位数为_____,EB晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:EB为3401kJ/mol、NaCl为786kJ/mol。导致两者晶格能差异的2点原因是____________。
⑴ 1s22s22p63s23p63d24s2(2分)
⑵ sp3(2分)
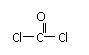 ⑶
(2分) c(2分)
⑶
(2分) c(2分)
⑷ 6 (2分) CaO晶体中离子的电荷数大于NaCl,离子间的平均距离小于NaCl(2分)
高频考点二十五 有机化学基础
70、(福建省龙岩一中2009-2010学年度高三第七次月考,30)现有部分前四周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
A |
第三周期中的半导体材科 |
|
B |
L层s电子数比p电子数少l |
|
C |
地壳中含量最高的元素 |
|
D |
第三周期主族元素中其第一电离能最大 |
|
E |
第四周期中未成对电子数最多 |
( 1)写出元素E基态原子的电子排布式: 。
(2)B单质分子中,含有
个 键和
个
键和
个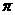 键,元素B的气态氢化的空间构型为
。
键,元素B的气态氢化的空间构型为
。
(3)A、B、C第一电离由大到小的顺序为(用元素符号表示): ;
(4)C单质的熔点 A单质的熔点(填“高于”或“低于”),其原因是:
。
(1)ls22s22p63s23p63d54s1(2)1 2 ,三角锥形
(3)N>O>Si
(4)低于 C12晶体属于分子晶体,Si晶体属于原子晶体,原子晶体中原子之间以很强的共价键结合,而分子晶体中分子间以较弱的分子间作用力结合,因而原子晶体的熔点比分子晶体的熔点高。
69、(银川一中2010届高三年级第六次月考,34)A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
(1)当n=2时,AB2属于_______分子(填“极性”或“非极性”),分子中有_____个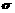 键,_____个
键,_____个 键。(6分)
键。(6分)
(2)当n=3时,A与B形成的晶体属于__________晶体。(2分)
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是________________(用元素符号表示)(2分)
 (4)已知某红紫色络合物的组成为CoCl3•5NH3•H2O。该络合物中的中心离子钴离子在基态时核外电子排布式为___________________,作为配位体之一的NH3分子的空间构型为_________________________。(4分)
(4)已知某红紫色络合物的组成为CoCl3•5NH3•H2O。该络合物中的中心离子钴离子在基态时核外电子排布式为___________________,作为配位体之一的NH3分子的空间构型为_________________________。(4分)
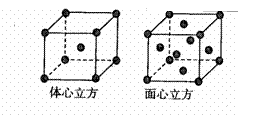
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为_______。(3分)
(1)非极性(2分),2(2分),2(2分) (2)原子(2分)
(3)P>S>Si(2分)
(4)Co3+[Ar]3d6(2分),三角锥形(或四面体)(2分)
(5)1:2(3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com