
题目列表(包括答案和解析)
5、下列有关氧化还原反应的叙述中正确的是 A.有单质参加或有单质生成的反应一定是氧化还原反应 B.氧化还原的本质是元素化合价的升降 C.失电子的反应物在反应中作还原剂,反应中被氧化 D.金属单质在化学反应中一定作还原剂
4、下列反应即属于氧化还原反应又属于置换反应的是
A.Fe2O3+3H2SO4==Fe2(SO4)3+3H2O
B.3Cu + 8 HNO3== 3Cu(NO3)2 +2 NO↑ + 4H2O
C.2Mg + CO2 ==C + 2MgO
D.C + H2O(g)== CO + H2
3、下列叙述正确的是 ( )
A 元素的单质可由氧化或还原含该元素的化合物来制得
B 得电子越多的氧化剂,其氧化性就越强
C 阳离子只能得到电子被还原,只能作氧化剂
D 含有最高价元素的化合物不一定具有强的氧化性
2、铁屑溶于过量的盐酸后,再加入下列物质,会有三价铁生成的是( )
A、 硫酸 B、氯水 C、硝酸锌 D、氯化钙
1、水在下列反应中不作还原剂的是 ( )
A、C12+H2O=HCIO+HCl B、2Na+2H2O=2NaOH+H2↑
C、3NO2+H2O=2HNO3+NO D、2F2+2H2O= 4HF+O2
3、氧化还原反应与四种基本反应类型的关系。
|
反应类型 |
表达式 |
举例 |
|
化合反应 |
A+B=AB |
|
|
分解反应 |
AB=A+B |
|
|
置换反应 |
A+BC=AC+B |
|
|
复分解反应 |
AB+CD=AD+CB |
|
肯定是氧化还原反应, 肯定不是氧化还原反应,
和 可能是氧化还原反应。
思考:下列方框代表化学反应的集合、圆圈代表某种反应类型的集合,其中,表示的关系正确的是 ( )
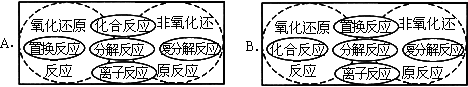
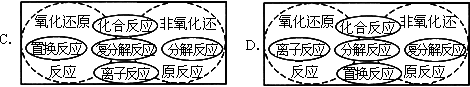
[课堂复习]
知识点1:了解氧化还原反应的本质是电子的转移
例1:下列关于氧化还原反应的叙述,正确的是 A.失去电子的反应是还原反应 B.失去电子的物质是还原剂 C.发生氧化反应的物质是氧化剂 D. 电子是从还原剂出发向氧化剂转移
例2:生产泡沫橡胶过程中,有如下一个反应:2H2O2=2H2O+O2↑。该反应中H2O2
A、既不是氧化剂,也不是不原剂 B、既是氧化剂又是还原剂
C、仅为氧化剂 D、仅为还原剂
例3:对于2NaBr + Cl2 == 2NaCl + Br2反应,下列说法不正确的是
A.该反应既是置换反应,又是氧化还原反应
B.Cl2是氧化剂,发生还原反应
C.若有1.6gBr2生成,反应过程中转移了0.04NA个电子
D.钠元素在反应中价态不变,所以NaBr既不是氧化剂,又不是还原剂
知识点2:了解常见的氧化还原反应
例4:属于氧化还原反应的离子方程式的是( )
A.CaCO3+2H+ = Ca2++CO2↑+H2O B.2Fe2++Cl2 = 2Fe3++2Cl-
C.HCO3-+H+ = CO2+H2O D.2Na+2H2O = 2Na++2OH-+H2↑
例5:苹果汁中含有Fe2+,是人们喜欢的一种补铁饮料,现榨的苹果汁在空气中会由淡绿色逐渐变为棕黄色。若榨汁时加入维生素C,可以防止这种现象发生。说明维生素C具有 A.还原性 B.氧化性 C.碱性 D.酸性
例6:下列试剂的浓溶液在空气久置都会变质。在变质过程中既发生了氧化还原反应,又发生了非氧化还原反应的是
A、双氧水 B、次氯酸钙 C、金属钠 D、硫酸亚铁
[记记背背]
常见的氧化剂:活泼非金属单质,如:F2、Cl2、Br2、I2、O2、O3,含较高价态元素的化合物如:HNO3、H2SO4、KClO3、KMnO4、MnO2、HClO。
常见的还原剂:活泼金属单质,如K、Na、Mg、Al等,非金属离子,含低价态元素的化合物和某些非金属单质,如S2-、H2S、SO2 、I-、CO、H2等,低价阳离子如Fe2+等。
即做氧化剂又做还原剂的是:Na2O2、H2O2等。
[课后练习]
多项选择题15题,每题3分,共30分,每题中至少有2个选项是正确的,全选对给3分,少选且正确给1分,错选给0分。
2、常见的氧化剂:
常见的还原剂:
一般说来,元素处于最高化合价时,它的原子只能 电子,因此,该元素只能作 剂,元素处于最低化合价时,它的原子只能 电子,因此,该元素只能作 剂,元素处于中间价态,随反应条件不同,该元素既能 电子,又能 电子,因此该元素既能作 剂,又能作 剂。
思考::从硫元素的化合价态上判断,下列物质中的硫元素不能表现氧化性的是( )
A.Na2S B. S C. SO2 D. H2SO4
1、 有关概念
在氧化还原反应中:
氧化剂 电子,化合价 ,被 ,发生 反应,得到 产物,具有 性;
还原剂 电子,化合价 ,被 ,发生 反应,得到 产物,具有 性。
氧化还原反应的特征: ,实质 。
判断一个反应是否为氧化还原反应的标志是 。

思考:下面的两个反应的氧化剂、还原剂,氧化产物和还原产物?电子转移的方向和数目?
高温
Cl2 + 2KBr = 2KCl + Br2 (2) Fe2O3 + 3CO = 2Fe + 3CO2
2、 了解常见的氧化还原反应。
[课前准备]
1、 了解氧化还原反应的本质是电子的转移。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com