
题目列表(包括答案和解析)
3、同位素 ⑴定义: ⑵性质: a. 同一元素的各种同位素虽然质量数不同,但它们的 几乎完全相同。 b. 天然存在的某种元素里,各种同位素所占的 一般是不变的。 c. 使用同一元素符号。 d. 在 中处于同一位置。 (3)核素:
如:H、D、T是氢元素的三种核素。 4、原子核外电子排布 ⑴.核外电子运动特征: a.电子质量 ,运动空间很 ,但电子运动速度 ,接近光速(3×108m/s) b.高速运动时,不能找到运动轨迹,不能准确地测量和计算出电子的确切位置。 ⑵.电子云:表示
⑶.核外电子排布规律: a.各电子层最多容纳电子数目: b.最外层电子数目不超过 个,(K层为最外层时,不超过 个)。 c.次外层电子数目不超过 个,倒数第三层电子数目不超过 个。
d.核外电子总是尽先排布在 的电子层,然后按能量高低依次排布 例:1-18号元素原子核外电子排布特点 (1)1-2号元素只有K电子层,有 个电子;3-10号元素的原子各有 个电子层,
最外层为 个电子,11-18号元素原子次外层(L层) 个电子。 练习:画原子结构示意图:
O Cl- K+
2、数量关系
⑴质量数(A)= +
⑵质子数(Z)= = = =
⑶电子层数 = ; 最外层电子数 =
1、原子组成(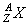 )
中子( 个):决定
的种类
)
中子( 个):决定
的种类
核外电子(带负电荷) 个:决定元素的
2. (上海市高考题)据报道,上海某医院正在研究用放射性同位素碘12553I治疗肿瘤。该同位素原子核内的中子数与核外电子数之差为
A.72 B.19 C.53 D.125
原子结构基础知识
 质子( 个):决定
的种类
质子( 个):决定
的种类
原子核(带正电荷)
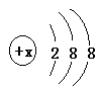
1. 有几种元素的微粒电子层结构如图所示,其中:
(1) 某电中性微粒一般不和其他元素的原子反应,这种微粒符号是______ __。
(2) 某微粒的盐溶液,加入AgNO3溶液时会出现白色浑浊,这种微粒符号是____ ___。
(3)某微粒氧化性甚弱,但得到电子后还原性强,且这种原子有一个单电子,这种微粒符号是_______ _。
(4)某微粒具有还原性,且这种微粒失去2个电子即变为原子,这种微粒的符号是________ ___。
思维方法: 。
展望高考:
4.核外电子排布规律:
(1)每个电子层最多容纳的电子数为 个。
(2)最外层不超过 个(若最外层为K层则不超过 个);次外层不超
过 个(若次外层为L层则不超过 个);倒数第三层不超过 个。
(3)能量最低原理:即核外电子总是尽先排在 、然后才依
次排在 、而原子失去电子时总是先失去 。
(4)核外电子运动特征:自身质量和体积: ;运动范围:
运动速度: ;所以 固定轨道, 能同时测出某时的速
度和位置。描述电子在原子核外运动状态的方法是: ,
此法中的小黑点表示的意义是 。
.[例题解析]
[例1]已知氢元素存在1H、2H、3H三种同位素,氧元素存在16O、17O、18O、
三种同位素,则形成的H2共有 种,形成的H2O共有 种,在形成的水分子中,具有不同相对分子质量的水分子有 种。
解题思路: 。
易错点: 。
[例2]已知X元素能形成相对分子质量分别为a、b、c的三种双原子分子,其分子个数之比为m:n:q,且a>b>c ,则X元素存在 种同位素,其质量数分别为 ;这些同位素原子所占该元素原子总数的百分比依次为 。
 解题思路:
。
解题思路:
。
易错点: 。
[考题再现]
3.核素与同伴素:
(1)核素概念: 。
(2)同位素概念: 。
(3)二者的区别与联系: 。
(4)同位素特征:①核物理性质: 、②物理性质: 、
③化学性质: 、④在自然界中不同形态下的丰度: 。
(5)几种相对原子质量:
①原子的相对质量: 、
②原子的近似相对原子质量: 、
③元素的相对原子质量: 、
④元素的近似相对原子质量: 。
2.原子结构的表示方式:(分别以铝原子和氯离子为例说明)
(1)原子结构示意图: 、 ;
(2)电子式: 、 ;
(3)原子组成表示式(原子符号): 、 。
1. 原子的组成:

据以上关系填空:决定原子种类的因素是 、决定同位素
种类的因素是 、决定原子近似相对原子质量的因素是 、
决定原子所显电性的因素是 。
8. 某1mol链烃A,在一定条件下完全裂解成1mol烷烃B和1mol烯烃C,生成的混合气体对氢气的相对密度为14.5。通过计算回答下列问题:
(1)写出链烃A可能的结构简式和名称。(2)烷烃B和烯烃C可能各是什么?(3)如果要求1molB完全燃烧时需要氧气的物质的量是整数,那么C只能是什么烯烃?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com