
题目列表(包括答案和解析)
7.下列叙述正确的是( )
A.两种元素构成的共价化合物分子中的化学键都是极性键
B.含有非极性键的化合物不一定是共价化合物
C.只要是离子化合物,其熔点就一定比共价化合物的熔点高
D.只要含有金属阳离子,则此物质中必定存在阴离子
6.下列电子式中,正确的是( )


5.已知磷酸分子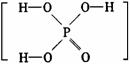 中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是( )
中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是( )

4.下列分子的结构中,原子的最外层不能都满足8电子稳定结构的是( )
A.CO2 B.PCl3 C.CCl4 D.NO2
3.溴化碘(IBr)的化学性质似卤素单质,能跟大多数金属反应生成金属卤化物,能跟某些非金属单质反应生成相应卤化物,能跟水反应,其化学方程为IBr+H2O HBr+HIO,下列有关IBr的叙述中,正确的是( )
HBr+HIO,下列有关IBr的叙述中,正确的是( )
A.固体IBr是分子晶体
B.在很多反应中IBr是强氧化剂
C.IBr跟水反应时,它既是氧化剂又是还原剂
D.跟NaOH溶液反应生成NaBr和NaIO
2.实现下列变化时,需克服相同类型作用力的是( )
A.二氧化硅和干冰的熔化 B.液溴和液汞的气化
C.食盐和冰的熔化 D.纯碱和烧碱的熔化
1.下列物质的化学式中,具有非极性键的离子化合物是( )
A.Na2O B.MgF2 C.NaOH D.Na2O2
4.晶体类型与性质
|
类 型 |
离子晶体 |
原子晶体 |
分子晶体 |
金属晶体 |
|
|
构成晶体微粒 |
|
|
|
|
|
|
微粒间作用力 |
|
|
|
|
|
|
性 质 |
熔沸点 |
|
|
|
|
|
硬 度 |
|
|
|
|
|
|
导电性 |
|
|
|
|
|
|
导热性 |
|
|
|
|
|
|
延展性 |
|
|
|
|
|
|
溶解性 |
|
|
|
|
|
|
典 型
实 例 |
NaCl KBr等 |
金刚石、二氧化硅等 |
H2 O2、冰、干冰等 |
Fe、Cu、Hg、合金等 |
3.思考:非极性键是否只存在于单质分子中?
2.共价键的极性与分子的极性
|
分子组成 |
空 间
构 型 |
常 见
分 子 |
键的极性 |
分子极性 |
|
双 原
子 |
|
N2 O2 Cl2 |
|
|
|
HCl CO NO |
|
|
||
|
三 原
子 |
|
CO2 CS2 |
|
|
|
|
H2O H2S |
|
|
|
|
四 原
子 |
|
BF3 |
|
|
|
|
NH3 |
|
|
|
|
五 原
子 |
|
CH4 CCl4 |
|
|
|
|
CH3Cl CH2Cl2 |
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com