
题目列表(包括答案和解析)
14. (2010年浙江)一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4·H2O是一种重要的染料及农药中间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
(2010年浙江)一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4·H2O是一种重要的染料及农药中间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
相关信息如下:

 w_w w. k#s5_
w_w w. k#s5_
①[Cu(NH3)4]SO4·H2O在溶液中存在以下电离(解离)过程:
[Cu(NH3)4]SO4·H2O=[Cu(NH3)4]2++SO42-+H2O
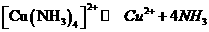
②(NH4)2SO4在水中可溶,在乙醇中难溶。
③[Cu(NH3)4]SO4·H2O在乙醇·水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下:
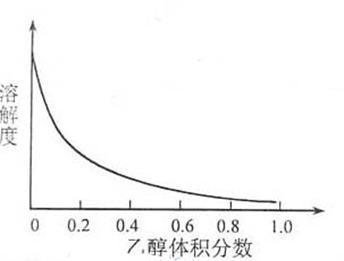
请根据以下信息回答下列问题:

 w_w w. k#s5_
w_w w. k#s5_
(1)方案1的实验步骤为:
a. 加热蒸发 b. 冷却结晶 c. 抽滤 d. 洗涤 e. 干燥
①步骤1的抽滤装置如下图所示,该装置中的错误之处是 ;抽滤完毕或中途停止抽滤时,应先 ,然后 。
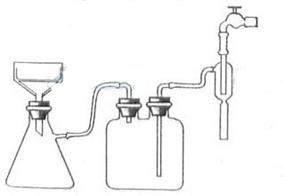
②该方案存在明显缺陷,因为得到的产物晶体中往往含有 杂质,产生该杂质的原因是 。
(2)方案2的实验步骤为:
a. 向溶液C加入适量 ,b. ,c. 洗涤,d. 干燥
①请在上述内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是 。
A. 乙醇 B. 蒸馏水 C. 乙醇和水的混合液 D. 饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是 。
解析:本题主要综合考察了过滤、抽滤实验、沉淀洗涤与干燥及结晶等实验操作原理,同时还结合化学平衡移动原理。抽滤装置的原理是通过气泵(或其他方法)试过滤器下方的压强降低,滤液上下形成压强差,从而加快过滤的速度,所以必需要求布氏漏斗的瓶口斜面朝向抽滤瓶的支管口。
答案:(1)①布氏漏斗的瓶口斜面未朝向抽滤瓶的支管口;断开连接安全瓶与抽气装置间的橡皮管;关闭抽气装置中的水龙头
②]Cu(OH)2或Cu2(OH)2SO4
加热蒸发过程中NH3挥发,使反应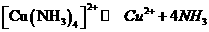 平衡往右移动,且Cu2+发生水解。
平衡往右移动,且Cu2+发生水解。
(2)①乙醇 抽滤(或减压过滤、吸滤)

 w_w w. k#s5_
w_w w. k#s5_
②C
③加热易使[Cu(NH3)4]SO4·H2O 分解(失去水或失去氨气)
13.(2010年天津)纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2·x H2O,经过滤、水洗除去其中的Cl,再烘干、焙烧除去水分得到粉体TiO2 。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:

 w_w w. k#s5_
w_w w. k#s5_
⑴ TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________。
⑵ 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
⑶ 下列可用于测定TiO2粒子大小的方法是_____________________(填字母代号)。
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
⑷ 配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是_________________;使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的_____(填字母代号)。
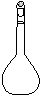



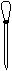

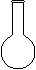

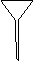

a b c d e
⑸ 滴定终点的现象是___________________________________________________。
⑹ 滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为_________________________。
⑺ 判断下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
① 若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果_________________________。
② 若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果_________。
解析:(1)设TiCl4的系数为1,根据元素守恒,TiO2·xH2O的系数为1,HCl的系数为4;再根据O元素守恒,可知H2O的系数为(2+x),所以方程式为:TiCl4+(2+x) H2O TiO2·xH2O+4HCl。
TiO2·xH2O+4HCl。
(2)检验沉淀是否洗净的方法是,取少量洗涤液,滴加AgNO3溶液,不产生白色沉淀,说明Cl-已除净。

 w_w w. k#s5_
w_w w. k#s5_
(3)核磁共振谱用于测有机物中含有多少种氢原子;红外光谱分析有机物含有何种化学键和官能团;质谱法常用于测有机物相对分子质量;透射电子显微镜可以观察到微粒的大小,所以选项d正确。
(4)NH4Fe(SO4)2中的NH4+和Fe3+易水解,故需加入一定量的稀硫酸抑制水解;配制一定物质的量浓度的溶液,还需要容量瓶和胶头滴管。
(5)因为是用KSCN作指示剂,终点时NH4Fe(SO4)2不再反应,生成血红色的Fe(SCN)3。
(6)根据得失电子守恒,有:1Ti3+-1Fe3+,故n(Fe3+)= n(Ti3+)= n(TiO2)=cV×10-3mol,其质量分数为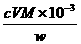 。
。
(7) NH4Fe(SO4)2溶液溅出,其物质的量浓度减小,消耗的体积增大,百分含量偏大;若终点俯视滴定管,读取的体积比实际消耗的体积偏小,质量分数偏小。

 w_w w. k#s5_
w_w w. k#s5_
答案:(1) TiCl4+(2+x) H2O TiO2·xH2O+4HCl
TiO2·xH2O+4HCl
(2)取少量水洗液,滴加AgNO3溶液,不产生白色沉淀,说明Cl-已除净。
(3)d
(4)抑制 NH4Fe(SO4)2水解 a c
(5)溶液变成红色
(6)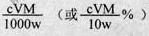
(7)偏高 偏低
12.(2010年江苏)对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。
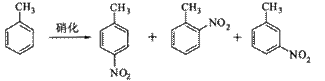
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3溶液水洗至中性,再经分离提纯得到对硝基甲苯。
(l)上述实验中过滤的目的是 。
(2)滤液在分液漏斗中洗涤静置后,有机层处于 层(填“上”或“下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有 。
(3) 下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
|
催化剂 |
n(催化剂) |
硝化产物中各种异构体质量分数(%) |
总产率(%) |
||
|
n(甲苯) |
对硝基甲苯 |
邻硝基甲苯 |
间硝基甲苯 |
||
|
浓H2SO4 |
1.0 |
35.6 |
60.2 |
4.2 |
98.0 |
|
1.2 |
36.5 |
59.5 |
4.0 |
99.8 |
|
|
NaHSO4 |
0.15 |
44.6 |
55.1 |
0.3 |
98.9 |
|
0.25 |
46.3 |
52.8 |
0.9 |
99.9 |
|
|
0.32 |
47.9 |
51.8 |
0.3 |
99.9 |
|
|
0.36 |
45.2 |
54.2 |
0.6 |
99.9 |
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为 。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是 。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有_ 、 。
解析:本题主要考察的是物质的性质和制备,同时考查了数据的处理与分析能力,能够迅速在表中提取到有用信息,利用信息解决有关问题的能力。
(1)因为NaHSO4在该反应中作为催化剂,而NaHSO4不溶于CCl4,所以此反应后过滤的目的是为了回收NaHSO4

 w_w w. k#s5_
w_w w. k#s5_
(2)因为该反应是以CCl4 作为有机溶剂的,CCl4的密度比水大,故有机层在下层;分液漏斗里的液体放不下来,除了分液漏斗堵塞,还有可能是分液漏斗上口活塞未打开,导致内外压强不相等。
(3)①从题给数据分析,当催化剂与甲苯的比例为0.32时,总产率最高且对硝基甲苯的含量最高 ②从题给数据可以看出,无论以何种比例反应,产物中的主要成分主要是对硝基甲苯和邻硝基甲苯; ③从题给数据可以看出,无论以何种比例反应,用NaHSO4 做催化剂的优点是在硝化产物中对硝基甲苯的比例提高、同时催化剂NaHSO4能循环使用。
答案:(1)回收NaHSO4
(2)下 分液漏斗上口塞子未打开
(3)①0.32
②甲苯硝化主要得到对硝基甲苯和邻硝基甲苯
③在硝化产物中对硝基甲苯比例提高 催化剂用量少且能循环使用(凡合理答案均可)
11.(2010年江苏)钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSiO3、BaSO3、Ba(FeO2)2等]。某主要生产BaCl2、BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2,其部分工艺流程如下:
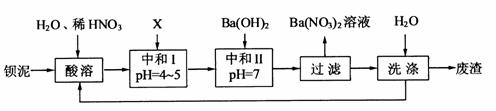
(1)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为 。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,原因是 、 。
(3)该厂结合本厂实际,选用的X为 (填化学式);中和Ⅰ使溶液中______ (填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)。
(4)上述流程中洗涤的目的是 。
解析:本题主要考查的是无机化工流程的分析,此题为化工生产题型,主要考察了化合物性质和制备。(1)HNO3是强酸,与Ba(FeO2)2反应,生成对应的硝酸盐和水,反应的化学方程式为:Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;(2)控制温度,不用浓硝酸的目的是为了控制反应速率,防止反应速率过快;同时浓硝酸容易挥发分解,且浓度越大,越易分解;(3)要除去调节pH且不在引入新的杂质,以及通过产物,结合溶液的酸碱性,选用的X应该为BaCO3;因为在I中含有Fe3+、H+和Ba2+、NO3-等,加入BaCO3后,能使H+浓度降低,进而促进Fe3+水解而降低其浓度;(4)在废渣中存有可溶性钡盐,而钡盐有毒,因此,洗涤的目的是减少可溶性钡盐对环境的污染。

 w_w w. k#s5_
w_w w. k#s5_
答案:(1)Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O
(2)防止反应速度过快 浓HNO3易挥发、分解
(3)BaCO3 Fe3+ H+
(4)减少废渣中可溶性钡盐对环境的污染 (凡合理答案均可)
10.(2010年江苏)高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
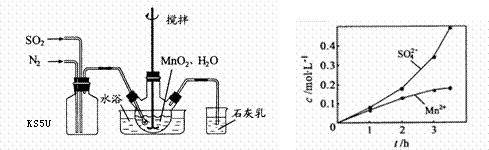
(1)制备MnSO4溶液:在烧瓶中(装置见上图)加入一定量MnO2和水,搅拌,
通入SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO4=MnSO4+H2O)。
①石灰乳参与反应的化学方程式为 。
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有 、 。
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如上图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7。请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
① ;② ;③ ;④ ;⑤低于100℃干燥。

 w_w w. k#s5_
w_w w. k#s5_
解析:本题主要考查的是实验的基本操作、实验仪器的选择、实验误差分析以及外界条件对化学反应速率的影响等。(1)①SO2是酸性氧化物可以与石灰乳发生化学反应,方程式为:Ca(OH)2+SO2=CaSO3+H2O。②根据外界条件对化学反应速率的影响可知,要使SO2尽快转化,在比例不变的情况下,可以通过控制温度或控制气体的流速以确保反应的充分进行。③从图中可以看出,随着时间的推移c(Mn2+)增加的频率减缓,甚至浓度下降,而c(SO42-)一直增加。因为客气中存在大量的氧气,而氧气可以与亚硫酸反应,Mn2+在O2与H2SO3反应中起了催化作用。(2)因为制得的MnSO4溶液显弱酸性,根据题给信息,可以得出制备高纯MnCO3的操作流程:加入NaHCO3或Na2CO3溶解,同时控制溶液的pH<7.7→过滤、洗涤→检验SO42-是否被除去→为了降低MnCO3的损耗,用C2H5OH洗涤→低温干燥。
答案:(1)①Ca(OH)2+SO2=CaSO3+H2O
②控制适当的温度 缓慢通入混合气体
③Mn2+催化O2与H2SO3,反应生成H2S04
(2)①边搅拌边加入NaHCO3(Na2CO3),并控制溶液PH<7.7

 w_w w. k#s5_
w_w w. k#s5_
②过滤,用少量水洗涤2~3次。
③检验SO42-是否被洗涤除去
④用少量C2H5OH洗涤
(凡合理答案均可)
9.(2010年海南)根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么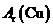 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算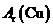 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):

 w_w w. k#s5_
w_w w. k#s5_
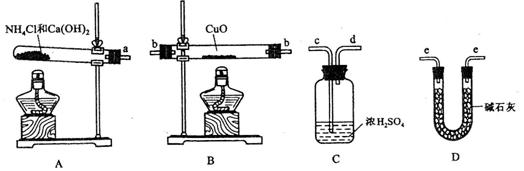
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→________________;
(3)在本实验中,若测得m(CuO)= a g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
①Cu0未完全起反应 ② CuO不干燥
③Cu0中混有不反应的杂质 ④ 碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_____________,或_______________和_______________达到实验目的。
解析:本题主要考察氨气的制备、净化、干燥和利用方程式进行的计算以及有关误差分析。氨气具有弱还原性,在加入条件下可以被氧化铜氧化,反应的化学方程式为:
2NH3+3CuO 3Cu+3H2O+N2↑;因为需要测定反应后生成物水的质量,所以必需保证通入的氨气是纯净干燥的,由于浓硫酸可以与氨气反应,因此只能通过碱石灰进行干燥,所以正确的顺序为a→e→b→e;根据反应方程式可知氧化铜和水的物质的量相等,所以有以下关系式:
3Cu+3H2O+N2↑;因为需要测定反应后生成物水的质量,所以必需保证通入的氨气是纯净干燥的,由于浓硫酸可以与氨气反应,因此只能通过碱石灰进行干燥,所以正确的顺序为a→e→b→e;根据反应方程式可知氧化铜和水的物质的量相等,所以有以下关系式: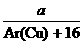 =
=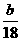 ,解得Ar(Cu)=
,解得Ar(Cu)=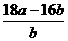 =
=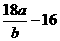 ;若Cu0未完全起反应,说明b偏小,结果偏大;若CuO不干燥,说明a偏小,b偏大,结果偏低;若Cu0中混有不反应的杂质,说明b偏小,结果偏大;若碱石灰不干燥,说明氨气干燥不彻底,b偏大,结果偏低;若NH4C1与Ca(OH)2混合物不干燥,但只要氨气干燥彻底,对结果不影响。所以选项①③正确;根据反应方程式可知也可以通过测定m(CuO)和m(Cu)或m(Cu)和m(H2O)来达到实验目的。
;若Cu0未完全起反应,说明b偏小,结果偏大;若CuO不干燥,说明a偏小,b偏大,结果偏低;若Cu0中混有不反应的杂质,说明b偏小,结果偏大;若碱石灰不干燥,说明氨气干燥不彻底,b偏大,结果偏低;若NH4C1与Ca(OH)2混合物不干燥,但只要氨气干燥彻底,对结果不影响。所以选项①③正确;根据反应方程式可知也可以通过测定m(CuO)和m(Cu)或m(Cu)和m(H2O)来达到实验目的。
答案:(1)2NH3+3CuO 3Cu+3H2O+N2↑
3Cu+3H2O+N2↑

 w_w w. k#s5_
w_w w. k#s5_
(2)a→e→b→e
(3)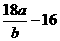
(4)①③
(5)m(CuO)和m(Cu)、m(Cu)和m(H2O)
8.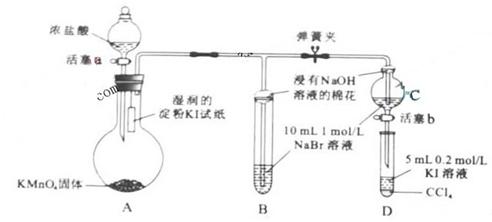 (2010年北京)为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。
(2010年北京)为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。

 w_w w. k#s5_
w_w w. k#s5_
试验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。

 w_w w. k#s5_
w_w w. k#s5_
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a。
Ⅳ………
(1)A中产生黄绿色气体,其电子式是 。
(2)验证氯气的氧化性强于碘的实验现象是 。
(3)B中溶液发生反应的离子方程式是 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 。
(5)过程Ⅲ实验的目的是 。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 ,
得电子能离逐渐减弱。
解析:(1)KMnO4具有强氧化性可以将浓盐酸氧化成黄绿色氯气,氯气为双原子分子,其电子式为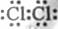 。(2)当碘离子被氧化成碘单质后,可以根据碘单质的性质:碘遇淀粉变蓝来证明。(3)B中的溶液变为黄色,说明有单质溴生成,反应的离子方程式是:
。(2)当碘离子被氧化成碘单质后,可以根据碘单质的性质:碘遇淀粉变蓝来证明。(3)B中的溶液变为黄色,说明有单质溴生成,反应的离子方程式是:
Cl2+2Br-=2Cl-+Br2。(4)由于C中有单质溴生成,因此之需要将C中的溶液滴入KI溶液中即可。(5)由于氯气也可以将KI氧化成碘单质,所以必需排除氯气对下面实验对干扰。(6)考察元素周期律的有关知识。
答案:(1)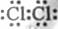


 w_w w. k#s5_
w_w w. k#s5_
(2)淀粉KI试纸变蓝
(3)Cl2+2Br-=2Cl-+Br2
(4)打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静止后CCl4层溶液变为紫红色
(5)确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰
(6)原子半径逐渐增大
7.(2010年四川) 
 w_w w. k#s5_
w_w w. k#s5_
碘被称为“智力元素”,科学合理地补充碘可防止
 碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,
碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,
它的晶体为白色,可溶于水。碘酸钾在酸性介质中
与过氧化氢或碘化物作用均生成单质碘。以碘为原料,
通过电解制备碘酸钾的实验装置如右图所示。
 请回答下列问题:
请回答下列问题:
(1)碘是 (填颜色)固体物质,实验室常用 方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:I2+6KOH=
5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为 ;
阴极上观察到的实验现象是 。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解
液中是否有I-的实验方案,并按要求填写下表。

 w_w w. k#s5_
w_w w. k#s5_
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。

 w_w w. k#s5_
w_w w. k#s5_
|
实验方法 |
实验现象及结论 |
|
|
|
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
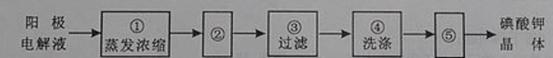
步骤②的操作名称是
,步骤⑤的操作名称是
。步骤④洗涤晶体的目的是
。

 w_w w. k#s5_
w_w w. k#s5_
解析:(1)考查物质的物理性质,较容易。碘是紫黑色固体易升华。(2)阳极发生氧化反应失电子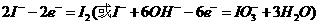 。阴极区加入氢氧化钾溶液,电解氢氧化钾实质是电解水,此时氢离子放电生成氢气,所以会有气泡产生。(3)考查I-的检验。此题可以借助与碘单质遇淀粉变蓝色这一特性,要设法将碘离子转化为碘单质。(4)考查实验的基本操作。要求考生对整个流程分析透彻。
。阴极区加入氢氧化钾溶液,电解氢氧化钾实质是电解水,此时氢离子放电生成氢气,所以会有气泡产生。(3)考查I-的检验。此题可以借助与碘单质遇淀粉变蓝色这一特性,要设法将碘离子转化为碘单质。(4)考查实验的基本操作。要求考生对整个流程分析透彻。
答案:(1)紫黑色 升华w w_w.k*s*5*
(2)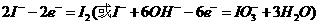 ;有气泡产生(3)
;有气泡产生(3)
|
实验方法 |
实验现象及结论 |
|
取少量阳极区电解液于试管中,加稀硫酸酸化后加入过氧化氢溶液,最后加入几滴淀粉试液,观察是否变蓝。 |
如果不变蓝,说明无I-。(如果变蓝,说明有I-。) |
(4)冷却结晶 干燥 洗去吸附在碘酸钾晶体上的氢氧化钾等杂质
6.(2010年重庆)某兴趣小组用题27图装置探究氨的催化氧化.

 w_w w. k#s5_
w_w w. k#s5_
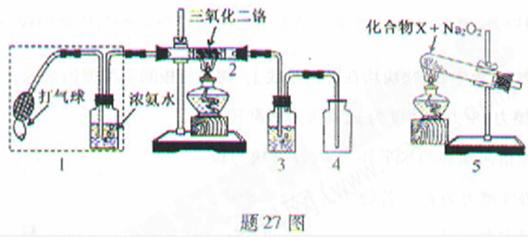
(1)氨催化氧化的化学方程式为___________________.
(2)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质呈红热状态;停止加热后仍能保持红热,该反应是_________反应(填“吸热”或“放热”).
(3)为保证在装置4中观察到红棕色气体,装置3应装入_________;若取消3,在4中仅观察到大量白烟,原因是___________________.
(4)为实现氨催化氧化,也可用装置5替换装置_________(填装置代号);化合物X为_________(只写一种),Na2O2的作用是___________________.
解析:本题考查氨的催化氧化及其相关实验。(1)NH3中N元素化合价为-3价,处于最低价态具有还原性可以被氧气氧化生成NO,反应的方程式为:4NH3+5O2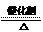 4NO+6H2O。(2)停止加热后仍能保持红热,说明该反应为放热,因此不加热后仍能保持红热状态。(3)产物中有NO和没有反应的NH3,NO会被O2氧化生成NO2,NO2与空气中的水蒸气反应生成HNO3,而HNO3与NH3反应会产生白烟,因此必需除去未反应的NH3,可以用浓硫酸吸收NH3。(4)装置5与1均产生可以产生NH3。NH4Cl加热分解可得NH3和HCl,而HCl与Na2O2可生成O2。
4NO+6H2O。(2)停止加热后仍能保持红热,说明该反应为放热,因此不加热后仍能保持红热状态。(3)产物中有NO和没有反应的NH3,NO会被O2氧化生成NO2,NO2与空气中的水蒸气反应生成HNO3,而HNO3与NH3反应会产生白烟,因此必需除去未反应的NH3,可以用浓硫酸吸收NH3。(4)装置5与1均产生可以产生NH3。NH4Cl加热分解可得NH3和HCl,而HCl与Na2O2可生成O2。
答案:

 w_w w. k#s5_
w_w w. k#s5_
(1)4NH3+5O2 4NO+6H2O (2)放热
4NO+6H2O (2)放热
(3)浓H2SO4;生成的NO与O2反应生成NO2,NO2与水反应生成HNO3,NH3与HNO3反应生成了NH4NO3而冒白烟。
(4)I;Na2O2与HCl反应生成氧气(合理答案均给分)
5.(2010年安徽) 某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
[实验]制作银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
⑴下列有关制备银镜过程的说法正确的是 。
a. 边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水,至最初的沉淀恰好溶解为止
b.将几滴银氨溶液滴入2ml乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配置过程中,溶液的pH增大
[提出假设]
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO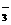 能氧化Ag。
能氧化Ag。
[设计实验方案,验证假设]
(2)甲同学从上述实验的生成物中检验出Fe2+,验证了假设1的成立。请写出Fe3+氧化Ag的离子方程式: 。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示:NO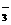 在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
|
实验步骤(不要求写具体操作过程) |
预期现象和结论 |
   w_w w. k#s5_ w_w w. k#s5_① ② 。。。。。。 |
若银镜消失,假设②成立。 若银镜不消失,假设②不成立。 |
[思考与交流]
⑷甲同学验证了假设1成立,若乙同学验证了假设2成立,则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO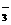 都氧化了Ag。
都氧化了Ag。
你是否同意丙同学的结论,并简述理由:________________________________。
解析:(1)发生银镜反应时银氨溶液应该是过量的,b错误;银镜反应需要水浴加热,c错误。因此ade正确;(2)依据反应的现象可以写出反应的化学方程式:Fe3+ + Ag = Fe2+ + Ag+;(3)NO3-只有在酸性条件下才具有氧化性,因此首先要测定溶液的pH,然后在配制相同pH的硝酸溶液进行反应;(4)见答案。
答案:(1)a、d、e (2)Fe3+ + Ag = Fe2+ + Ag+
(3)
|
实验步骤(不要求写具体操作过程) |
预期现象和结论 |
|
①测定上述实验用的Fe(NO3)3溶液的pH ②配制相同pH的硝酸溶液,将此溶液加入有银镜的试管内 |
若银镜消失,假设②成立。 若银镜不消失,假设②不成立。 |
(4)不同意。甲同学检验出了Fe2+,可确定Fe3+ 一定氧化了Ag;乙同学虽然验证了此条件下NO3-能氧化Ag,但在硝酸铁溶液氧化Ag时,由于没有检验NO3-的还原产物,因此不能确定NO3-氧化了Ag。[(3)(4)其他合理答案均可]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com