
题目列表(包括答案和解析)
20.水蒸气中常含有部分(H2O)2,要确定(H2O)2的存在,可采用的方法是
A.1 L水蒸气冷凝后与足量金属钠反应,测产生氢气的体积
B.1 L水蒸气通过浓硫酸后,测浓硫酸增重的质量
C.该水蒸气冷凝后,测水的pH D.该水蒸气冷凝后,测氢氧原子比
19.以下各种尾气吸收装置中,适合于吸收易溶性气体,而且能防止倒吸的是
A. B.
B.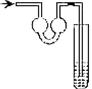 C.
C.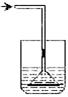 D.
D.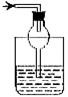
18.下列离子中,电子数大于质子数且质子数大于中子数的是
A.D3O+ B.Li+ C.OD- D.OH-
17.某500 mL溶液中含0.1 mol Fe2+、0.2 mol Fe3+,加入0.2 mol铁粉,待Fe3+完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变)
A.0.4 mol/L B.0.6 mol/L C.0.8 mol/L D.1.0 mol/L
16.欲使0.1 mol/L的NaHCO3溶液中c(H+)、c(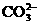 )、c(
)、c(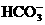 )都减少,其方法是
)都减少,其方法是
A.通入二氧化碳气体 B.加入氢氧化钠固体
C.通入氯化氢气体 D.加入饱和石灰水溶液
15.对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有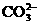
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
14.叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是
A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(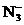 )>c(OH-)
)>c(OH-)
B.HN3与NH3作用生成的叠氮酸铵是共价化合物
C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(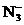 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
D.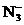 与CO2含相等电子数
与CO2含相等电子数
13.下列离子方程式正确的是
A.碳酸氢钠溶液中加入盐酸: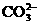 +2H+¾®CO2+H2O
+2H+¾®CO2+H2O
B.硫化亚铁与盐酸反应:S2-+2H+¾®H2S
C.苯酚钠溶于醋酸溶液:C6H5O-+CH3COOH¾®C6H5OH+CH3COO-
D.氯化亚铁溶液中通入少量氯气:Fe2++Cl2¾®Fe3++2Cl-
11.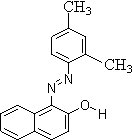 苏丹红是很多国家禁止用于食品生产的合成色素。结构简式如右图。关于苏丹红说法错误的是
苏丹红是很多国家禁止用于食品生产的合成色素。结构简式如右图。关于苏丹红说法错误的是
A.分子中含一个苯环和一个萘环 B.属于芳香烃
C.能被酸性高锰酸钾溶液氧化 D.能溶于苯
12.下列说法错误的是
A.原子晶体中只存在非极性共价键 B.分子晶体的状态变化,只需克服分子间作用力
C.离子晶体在熔化状态下能导电 D.金属晶体通常具有导电、导热和良好的延展性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com