
题目列表(包括答案和解析)
5. 下列叙述正确的是
A. 两种元素构成的共价化合物分子中的化学键都是极性键
B. 两种非金属元素原子之间形成的化学键都是极性键
C. 含有极性键的化合物分子中一定不含非极性键
D. 只要是离子化合物,其熔点就比共价化合物的熔点高
4. 在一定条件下有如下反应:R2On2-+aH++3Y2- =2R3++3Y+bH2O,则R2On2-中的n值为
A.4 B. 5 C.6 D. 7
3. 实验室用4mol SO2和2mol O2进行下列反应:
2SO2 (g)+O2(g)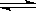 2SO3(g)
2SO3(g)
△H=–196.64kJ/mol,当放出314.62 kJ热量时,SO2的转化率为
A.40% B. 50% C.80% D. 90%
2. FeCl3溶液、Fe(OH)3 胶体共同具备的性质是
A.加入饱和的MgSO4溶液都发生聚沉
B.分散质的粒子都不能通过半透膜
C.都比较稳定,密封保存一段时间也都不会产生沉淀
D.加入硫酸先产生沉淀,后沉淀溶解
1. 下列物质不能用作饮用水的消毒剂的是
A.
Cl2
B.
 -OH
-OH
C. O3 D. ClO2
16.(11分)(探究创新题)某混合金属粉末,除Mg外还含有Al、Zn中的一种或两种,含量都在10%以上。某研究小组设计实验探究该混合金属粉末中加NaOH溶液、锌元素的存在。
所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O
该小组探究过程如下:
●查阅资料:
 ①镁、加NaOH溶液、锌都是白色金属;
①镁、加NaOH溶液、锌都是白色金属;
②锌(Zn)可以与NaOH溶液反应生成H2;
③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3·H2O;
④Zn2+易形成络合物[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH。
●提出假设:
(1)假设1:该混合金属粉末中除镁外还含有__________;
(2)假设2:该混合金属粉末中除镁外还含有__________;
(3)假设3:该混合金属粉末中除镁外还含有加NaOH溶液、锌。
●实验探究:
基于假设3,甲同学设计了如图1所示的实验方案,乙同学设计了如图2所示的实验方 案:
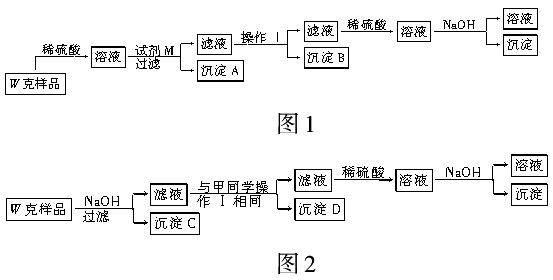

(1)试剂M是__________。
(2)写出操作Ⅰ的过程:
________________________________________________________________________
________________________________________________________________________。
(3)丙同学认为乙同学的方案比甲同学的好,理由是
________________________________________________________________________
________________________________________________________________________。
(4)丁同学研究了甲、乙两同学的方案后,用最简便的方法测定了W g样品中金属镁(Mg)的质量分数,他的方法是
________________________________________________________________________。
答案 提出假设:(1)加NaOH溶液(或Al)
(2)锌(或Zn)(以上两空可颠倒)
实验探究:(1)NaOH溶液
(2)在滤液中加入稀硫酸,直至生成的沉淀刚好溶解,再加入足量的稀氨水
(3)步骤简单,节约试剂
(4)将沉淀C小心洗涤,干燥后称量、计算即可
15.(10分)(2010·滨州质检)实验室可用加NaOH溶液屑、氨水、氢氧化钠溶液、稀硫酸 等来制备氢氧化加NaOH溶液,某同学设计了三种实验方案,
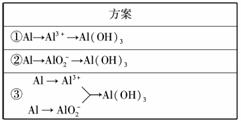

(1)用方案①制备Al(OH)3时使用的药品最好是加NaOH溶液屑、稀硫酸和氨水,不用 氢 氧化钠代替氨水的原因是
________________________________________________________________________
________________________________________________________________________;
写出该方案中有关的离子方程式
________________________________________________________________________。
(2)用方案②来制备Al(OH)3时,必须注意__________的用量,以防止生成的Al(OH)3溶解。
(3)三种方案中,你认为最好的是__________(填序号),原因是
________________________________________________________________________
________________________________________________________________________。
解析 分析本题应从Al(OH)3的两性着手,过量的强酸、强碱均能降低Al(OH)3的产率,而Al3+与AlO反应制取氢氧化加NaOH溶液,则不存在该问题,故③方案最好。
答案 (1)若用NaOH溶液沉淀Al3+,终点不易控制,因为Al(OH)3会溶于过量的NaOH溶液,从而影响Al(OH)3的生成量
2Al+6H+===2Al3++3H2↑,
Al3++3NH3·H2O===Al(OH)3↓+3NH
(2)稀硫酸 (3)③ 药品用量减少,操作最为简单
14.(9分)(2008·重庆理综,27)某学习小组用如图所示装置测定加NaOH溶液镁合金中加NaOH溶液的质量分数和加NaOH溶液的相对原子质量。
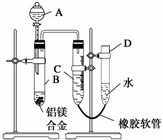
(1)A中试剂为________________。
(2)实验前,先将加NaOH溶液镁合金在稀酸中浸泡片刻,其目的是
________________________________________________________________________。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂;⑤检查气密性。上述操作的顺序是__________(填序号);记录C的液面位置时,除视线平视外,还应________________________________________________________________________。
(4)B中发生反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
(5)若实验用加NaOH溶液镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为c g,则加NaOH溶液的相对原子质量为____________________。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得加NaOH溶液的质量分数将__________(填“偏大”、“偏小”或“不受影响”)。
解析 (1)观察实验装置图可知是用量气法完成实验目的,故A中应盛NaOH溶液,在B中发生2Al+2NaOH+2H2O===2NaAlO2+3H2↑的反应。
(2)目的是除去加NaOH溶液镁合金表面的氧化膜。
(3)正确顺序应为⑤①④③②;为使C中气体的压强与外界大气压相等,还应使D与C的液面相平。
(5)据2Al - 3H2
2 3
得M(Al)=
(6)据w(Al)=×100%的计算公式可知未洗涤不溶物会造成加NaOH溶液的质量分数偏小。
答案 (1)NaOH溶液 (2)除去加NaOH溶液镁合金表面的氧化膜
(3)⑤①④③② 使D和C的液面相平
(4)2Al+2NaOH+2H2O===2NaAlO2+3H2↑
(5) (6)偏小
13.(10分)(2009·广东,24)超细氧化加NaOH溶液是一种重要的功能陶瓷原料。
(1)实验室常以NH4Al(SO4)2和NH4HCO3为原料,在一定条件下先反应生成沉淀NH4AlO(OH)HCO3,该沉淀高温分解即得超细Al2O3。NH4AlO(OH)HCO3热分解的化学反应方程式为
________________________________________________________________________
________________________________________________________________________。
(2)NH4Al(SO4)2·12H2O的相对分子质量为453。欲配制100 mL pH为2、浓度约为0.1 mol/L的NH4Al(SO4)2溶液,配制过程为:
①用托盘天平称量NH4Al(SO4)2·12H2O固体
________________________________________________________________________g;
②将上述固体置于烧杯中,
________________________________________________________________________。
(3)在0.1 mol/L NH4Al(SO4)2溶液中,加NaOH溶液各形态的浓度(以Al3+计)的对数(lgc)随溶液pH变化的关系见下图:
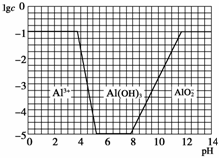
①用NaOH溶液调节(2)中溶液pH至7,该过程中发生反应的离子方程式有________________________________________________________________________
________________________________________________________________________。
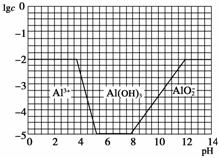
②请画出0.01 mol/L NH4Al(SO4)2溶液中加NaOH溶液各形态的浓度的对数lgc随溶液pH变化的关系图,并进行必要的标注。
解析 (1)根据题中信息及元素守恒NH4AlO(OH)HCO3热分解的产物除Al2O3外还应有NH3、H2O和CO2:2NH4AlO(OH)HCO3Al2O3+2NH3↑+3H2O+2CO2↑。
(2)①n[NH4Al(SO4)2]=0.1 L×0.1 mol/L=0.01 mol
m[NH4Al(SO4)2·12H2O]=0.01 mol×453 g/mol=4.53 g≈4.5 g
称量→称量→溶解→移液→洗涤→定容。
(3)①从图中可看出pH=7时,Al元素全部以Al(OH)3形式存在。
②依据题中给出的0.1 mol/L NH4Al(SO4)2的图象,可画出0.01 mol/L的图象,同时标明加NaOH溶液元素的存在形态Al3+、Al(OH)3、AlO即可。
答案 (1)2NH4AlO(OH)HCO3Al2O3+2NH3↑+3H2O+2CO2↑
移液→移液→洗涤→定容
(3)①Al3++3OH-===Al(OH)3↓,
H++OH-===H2O,
NH+OH-===NH3·H2O
②
12.(2009·盐城调研)将一定质量的Mg和Al混合物

投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。则下列说法正确的是 ( )
A.Mg和Al的总质量为8 g
B.硫酸的物质的量浓度为5 mol/L
C.生成的H2在标准状况下的体积为11.2 L
D.NaOH溶液的物质的量浓度为5 mol/L
解析 由图可知,固体中含有0.15 mol的Mg和0.2 mol的Al,所以总质量为9 g;与硫酸反应生成的氢气的体积应为(0.15 mol+0.3 mol)×22.4 L/mol=10.08 L;在加入240 mL NaOH溶液时,Al(OH)3恰好全部转化为NaAlO2,所以氢氧化钠溶液的浓度为=5 mol/L。
答案 D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com