
题目列表(包括答案和解析)
7.(2009年无锡模拟)用稀H2SO4、NaOH溶液和金属铝为原料制取Al(OH)3。甲、乙、丙三个学生的制备途径分别是:
甲:Al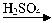 Al2(SO4)3
Al2(SO4)3
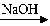 Al(OH)3
Al(OH)3
乙:Al 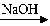 NaAlO2
NaAlO2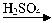 Al(OH)3
Al(OH)3
丙:
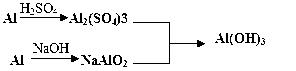
若要得到等量的Al(OH)3,则( )
A.三者消耗的原料相同
B.甲消耗的原料的总物质的量最多
C.乙消耗的原料的总物质的量最少
D.丙消耗的原料的总物质的量最少
6.(2009年北京卷)由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如下图转化关系(部分生成物和反应条件略去)。下列推断不正确的是( )
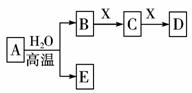 A.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
A.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
B.若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,则E一定能还原Fe2O3
C.若D为CO,C能和E反应,则A一定为Na2O2
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
5.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2yCO3,关于该物质的说法正确的是( )
A.该物质属于两性氢氧化物
B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2yCO3最多可消耗3 mol H+
D.该药剂不适合于胃溃疡患者服用
4.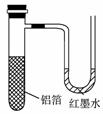 (2009年福州模拟)用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断,下列说法错误的是( )
(2009年福州模拟)用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断,下列说法错误的是( )
A.实验中发生的反应都是氧化还原反应
B.铝是一种较活泼的金属
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝和氧化汞的混合物
3.若1.8 g某金属跟足量盐酸充分反应,放出2.24 L(标准状况)氢气,则该金属是( )
A.Al
B.Mg
C.Fe
D.Zn
2.只用胶头滴管和试管,不用其他试剂就可以区别的溶液(浓度均为0.1 mol·-1L)是( )
①CaCl2和Na2CO3 ②Ba(OH)2和NaHCO3 ③稀H2SO4和Na2CO3 ④NaAlO2和盐酸 ⑤AlCl3和NaOH
A.①②③
B.③④⑤
C.①②
D.全部
1.常温下,把钠、镁和铝各一小块分别投入到1 mol/L NaOH溶液中,化学反应速率(v)由快到慢的顺序是( )
A.v钠>v镁>v铝
B.v铝>v钠>v镁
C.v钠>v铝>v镁
D.v铝>v镁>v钠
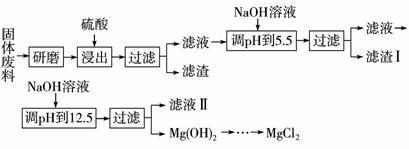
12.(2009年广东卷)某厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:
|
沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
pH |
3.2 |
5.2 |
12.4 |
部分阳离子以氢氧化物形式完全沉淀时溶液的pH见上表,请回答下列问题:
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有_______________(要求写出两条)
(2)滤渣Ⅰ的主要成分有____________。
(3)从滤液Ⅱ中可回收利用的主要物质有____________。
(4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
 MgCl2+2NaClO3=Mg(ClO3)2+2NaCl
MgCl2+2NaClO3=Mg(ClO3)2+2NaCl
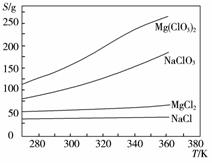
已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2。简述可制备Mg(ClO3)2的原因:_________________。
②按①中条件进行制备实验。在冷却降温析出Mg
(ClO3)2过程中,常伴有NaCl析出,原因是:
_______________。除去产品中该杂质的方法是:____________。
11.(2009年湛江模拟)某化学兴趣小组测定某Fe2(SO4)3样品(只含少量FeCl2杂质)中铁元素的质量分数,按以下实验步骤进行操作:
①称取a g样品,置于烧杯中;
②加入50 mL 1.0 mol/L稀硫酸和一定量的蒸馏水,使样品溶解,然后准确配制成250.00 mL溶液;
③量取25.00 mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;
④加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤,洗涤沉淀;
⑥将沉淀转移到某容器内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;
⑦……
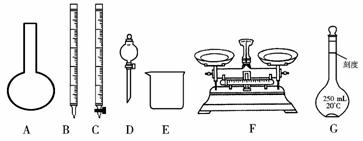
请根据上面叙述,回答:
(1)上图所示仪器中,本实验步骤①②③中必须用到的仪器有E和____________(填字母)。
(2)步骤②中:配制50 mL,1.0 mol/L稀H2SO4需要98%(密度1.84 g/cm3)的浓H2SO4体积为____________ mL,量取该体积的浓H2SO4用到量筒规格是____________。
(3)样品中的杂质Fe2+有较强的还原性,完成并配平下列反应的离子方程式
□Fe2++□ClO2□□=□Fe3++□Cl-+□H2O
从理论上分析,上述实验中若将氯水改为ClO2时,对实验结果造成____________(填“偏大”“偏小”或“不影响”),等物质的量的ClO2与Cl2的氧化效率之比为____________。
(4)第⑥步的操作中,将沉淀物转移到____________(填仪器名称)中加热,冷却至室温,称量其质量为m1 g,再次加热并冷却至室温称量其质量为m2 g,若m1与m2差值较大,接下来的操作应当是____________。
(5)若步骤⑥不在干燥器中冷却,则测定的铁元素的质量分数会____________(填“偏大”“偏小”或“不影响”);若容器质量是W1 g,最终容器和固体的总质量是W2 g,则样品中铁元素的质量分数为____________(列出算式,不需化简)。
10.(2009年上海模拟)某一反应体系中有反应物和生成物共6种:HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe2(SO4)3,在反应后的溶液中滴加KSCN溶液不显红色。
(1)该反应中,被氧化的元素是____________,氧化剂是____________。
(2)在该反应中,发生氧化反应的过程是____________→____________。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目:____________ 。
(4)FeSO4可用于制墨水、颜料、补血剂等,它易被氧化。FeSO4遇H2SO4(浓)、HNO3时反应的产物是N2O3、H2O、Fe2(SO4)3,则该反应中还原剂与氧化剂的物质的量之比为____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com