
题目列表(包括答案和解析)
8.常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为O2的是( )

7.在一定温度和压强下,1 L X气体和1 L Y气体完全反应后生成1 L水蒸气和1 L氮气。X、Y两种气体是高·考¥资%源~网 ( )
A.H2、N2O4 B.H2、N2O3 C.H2、N2O D.H2、NO2
6.在三个密闭容器中分别充入Ne、H2、O2三种气体,在以下各种情况下排序正确的是 ( )
A.当它们的体积和温度、压强均相同时,三种气体的密度ρ(H2)>ρ(Ne)>ρ(O2)
B.当它们的温度和密度都相同时,三种气体的压强p(H2)>p(Ne)>p(O2)
C.当它们的质量和温度、压强均相同时,三种气体的体积V(O2)>V(Ne)>V(H2)
D.当它们的压强和体积、温度均相同时,三种气体的质量m(H2)>m(Ne)>m(O2)
5.在同温同压下,相同体积的甲、乙两种气体的质量比是17∶14。若乙气体是CO,则甲气体可能是( )
A.H2S B.HCl C.NH3 D.Cl2
4.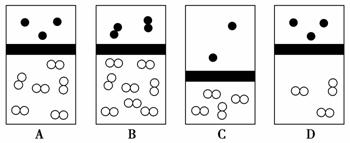 下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是 ( )
下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是 ( )
3.由阿伏加德罗常数(NA)和一个水分子的质量(m水)、一个水分子的体积(V水),不能确定的物理量有 ( )
A.1摩尔水的质量 B.1摩尔水蒸气的质量
C.1摩尔水的体积 D.1摩尔水蒸气的体积
2.下列叙述正确的是(用NA代表阿伏加德罗常数的值) ( )
A. 2.4 g金属镁变为镁离子时失去的电子数为0.1NA
B.1 mol HCl气体中的粒子数与0.5 mol/L盐酸中溶质的粒子数相等
C.在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10 NA
D.CO和N2为等电子体,22.4 L的CO气体与1 mol N2所含的电子数相等
1.下列说法正确的是 ( )
A.NaOH的摩尔质量为40 g
B. 1 mol O2的质量与它的相对分子质量相等
C.1 mol OH-的质量为17 g·mol-1
D.氦气的摩尔质量(单位g·mol-1)在数值上等于它的相对原子质量
21. (2010·临沂模拟)由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH、Mg2+、CO、Ba2+、SO.将该混合物溶于水后得澄清溶液,现取3份100 mL该溶液分别进行如下实验:
|
实验 序号 |
实验内容 |
实验结果 |
|
1 |
加AgNO3溶液 |
有白色沉淀生成 |
|
2 |
加足量NaOH溶液并加热 |
收集到气体1.12 L(已折算成标准状况下的体积) |
|
3 |
加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6.27 g,第二次称量读数为2.33 g |
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是____________(填“一定存在”“一定不存在”或“不能确定”);根据实验1-3判断混合物中一定不存在的离子是________.
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
|
阴离子符号 |
物质的量浓度(mol/L) |
|
|
|
|
|
|
|
|
|
(3)试确定K+是否存在?________,判断的理由是________________________________
______________________________________________________________.
20.常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,得到密度为1.17 g/cm3的混合溶液.
(1)该混合溶液中NaCl的质量分数为 .
(2)该混合溶液中NaCl的物质的量浓度 mol/L.
(3)在1000 g水中需加入 mol氯化钠,才能使其浓度恰好与上述混合溶液浓度相等(保留1位小数).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com