
题目列表(包括答案和解析)
9.(2009年合肥质检)某化学兴趣小组选用下列实验装置测定工业原料气(含SO2、N2、O2)中SO2的含量。
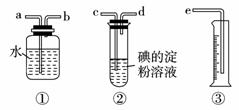
(1)若原料气从左向右流向时,上述装置组装连接的顺序是:原料气→____________(填a、b、c、d、e)。
(2)装置②中发生反应的离子方程式为____________ ;当装置②中出现____________(填现象)时,立即停止通气。
(3)你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是____________。(填编号)
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
(4)若碘溶液的浓度为0.05 mol/L,体积为20 mL,收集到的N2与O2的体积为297.6 mL(已折算为标准状况下的体积),SO2的体积分数为____________。
8.标准状况下,某同学向100 mL H2S饱和溶液中通入SO2,所得溶液pH变化如下图所示。下列分析中,正确的是( )
A.ab段反应是:SO2+2H2S=3S↓+2H2O
B.亚硫酸是比氢硫酸更弱的酸
C.原H2S溶液的物质的量浓度为0.10 mol·-1L
D.b点对应的溶液导电性最强
7.下列过程中,最终的白色沉淀不一定是BaSO4的是( )
A.无色溶液
 白色沉淀
白色沉淀
B.Ba(NO3)2溶液
 白色沉淀
白色沉淀
C.Fe(NO3)2溶液
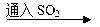
 白色沉淀
白色沉淀
D.无色溶液 白色沉淀
白色沉淀 白色沉淀
白色沉淀
6.(2010年枣庄检测)有一瓶无色气体,可能含有H2S、CO2、HBr、HCl、SO2中的一种或几种。向其中加入过量氯水,得到透明溶液,把溶液分成两份。向其中一份中加入盐酸酸化的BaCl2溶液,出现白色沉淀;向另一份中加入硝酸酸化的AgNO3溶液,也有白色沉淀。则下列结论正确的是( )
A.原气体中肯定有SO2
B.原气体中肯定有H2S和HBr
C.原气体中肯定有SO2和HCl
D.原气体中肯定没有CO2
5.(2010年哈师大附中模拟)硫黄在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,溴水褪色,乙变成丙。在丙里加入Na2S生成气体丁,把丁通入乙得到沉淀戊。甲、乙、丙、丁、戊均含有硫元素,则它们正确的顺序是( )
A.SO3 H2SO4 H2SO3 H2S S
B.SO2 H2SO3 H2SO4 SO2 SO3
C.SO3 H2SO4 H2SO3 SO2 Na2S2O3
D.SO2 H2SO3 H2SO4 H2S S
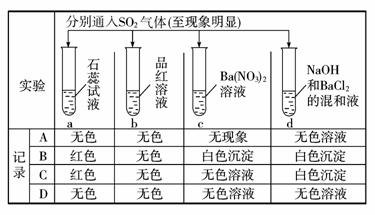
4.下列实验报告记录的实验现象正确的是( )
3.能与SO2气体反应,但无沉淀产生的是( )
①溴水 ②Ba(OH)2溶液 ③石灰水 ④Na2CO3溶液
⑤稀H2SO4 ⑥H2S溶液 ⑦Na2SO3溶液
A.只有①
B.①④⑤
C.④⑥⑦
D.①④⑦
①CuS ②FeS ③SO23 ④H2S ⑤FeCl2
A.①③⑤
B.①②③⑤
C.①②④⑤
D.全部
2.(2009年山东卷)下列推断合理的是( )
A.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂
B.金刚石是自然界中硬度最大的物质,不可能与氧气发生反应
C.浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应
D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色
12. (2009年北京卷)某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。可选药品:浓硝酸、3 mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳已知:氢氧化钠溶液不与NO反应,能与NO2反应。2NO2+2NaOH=NaNO3+NaNO2+H2O
(2009年北京卷)某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。可选药品:浓硝酸、3 mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳已知:氢氧化钠溶液不与NO反应,能与NO2反应。2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中。装置③、④、⑥中盛放的药品依次是______________。
(2)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹后______________。
(3)装置①中发生反应的化学方程式是- 。
(4)装置②的作用是-________________,发生反应的化学方程式是________________。
(5)该小组得出的结论所依据的实验现象是_________________。
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确。
这些方案中可行的是(选填序号字母)____________。
a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气
11.某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时,设计如下方案:
|
|
操作 |
结论 |
|
① |
火柴梗 |
变黑者为浓硫酸 |
|
② |
加入金属铝片 |
产生刺激性气味者为浓硫酸 |
|
③ |
分别加入到盛水的试管中 |
放热者为浓硫酸 |
|
④ |
用玻璃棒蘸浓氨水靠近酸的瓶口 |
冒白烟者为浓硫酸 |
|
⑤ |
加到CuSO4·5H2O晶体中 |
变白者为浓硫酸 |
(1)其中可行的是____________(填序号)。
(2)其中一个稍作改进就能成为可行的是____________,改进方法是_________________。
(3)完全错误的是____________,因为____________ 。
(4)请给出另外两种鉴别方法;
|
|
操作 |
根据现象得出结论 |
|
A |
|
|
|
B |
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com