
题目列表(包括答案和解析)
284. 在黑色火药发生爆炸的反应中,+2N3+3=2+N 2↑+32↑被还原的元素是()
2↑+32↑被还原的元素是()
A. 只有N B. 只有
. 只有 D. N和
271. 根据下列事实:①X+Y2+=X2++Y,②Z+2H2=Z(H)2+H2↑,③Z2+氧化性比X2+弱,④Y+2+=+Y2+,可推知X、Y、Z 、的还原性由强到弱的顺序是()
、的还原性由强到弱的顺序是()
A. X>Y>Z>
B. Y>X>>Z
. Z>X>Y>
D. Z>Y>X>
翰林汇272. 根据下列实验事实,判断微粒氧化性大小顺序正确的是()
①Fel3溶液中滴入I溶液,加l4振荡,l4层呈紫色
②Fel2溶液中滴加氯水,再加N溶液,呈红色
③M n4溶液中滴加盐酸,Mn4溶液褪色
n4溶液中滴加盐酸,Mn4溶液褪色
A. I2<l2<Fe3+<Mn4-
B. Mn4->l2>Fe 3+>I2
3+>I2
. l2>I2>Fe3+>Mn4-
 D. Fe3+>Mn4->l2>I2
D. Fe3+>Mn4->l2>I2
翰林汇273. 有下列氧化还原反应
(1)Fe+4=+Fe4
(2)+2Fel3=l2+2Fel2
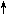 (3)2Mn4+16Hl=2l+2Mnl2+l2+8H2
(3)2Mn4+16Hl=2l+2Mnl2+l2+8H2
(4)2Fe l
l 2+l2=
2+l2= 2Fel3
2Fel3
根据上述反应判断各微粒的氧化性由弱到强的顺序是()
A. 2+、Fe2+、l2、Fe3+、Mn
B. Fe2+、2+、Mn 、Fe3+、l2
、Fe3+、l2
. F e2+、2+、Fe3+、l2、Mn
e2+、2+、Fe3+、l2、Mn
D. 2+、Fe2+、l2、Mn 、Fe3+
、Fe3+
翰林汇274. 常温下,下列三个反应都能自发的 向右进行:
向右进行:
2D-+A2=2A-+D22B-+D2=2D-+B22A-+2=2-+A2[来源:]
由此得出正确结论是()
A. A-、B-、-、D-中-还原性最强
B. A2、B2、2、D2中2的氧化性最弱
. 2-+B2=2B-+2不能自发向右进行
D. 还原性A->B-
翰林汇27. A2、B2、23种单质和它们离子间能发生下列反应
2A-+2=2-+A22-+B2=2B-+2
若X-能与2发生反应2X-+2=2-+X2有关说法中不正确的是()
A. 氧化性B2>2>A2
B. 还原性X->->B-
. X2与B-能发生反应
D. X2与B-不能发生反应
翰林汇276. 已知下列反应
(1)2Fel3+2I=2Fel2+2l+I2
(2)6Fel2+3Br2=4Fel3+2FeBr3
下列离子的还原性由强至弱的顺序是()
A. I->Br->Fe2+
 B. Fe2+>I->Br-[来源:]
B. Fe2+>I->Br-[来源:]
. I->Fe2+>Br-
D. Br->Fe2+>I-
翰林汇277. 下列各组离子因氧化还原反应而不能大量共存的是()
A. H+、Na+、l-、232-
B. Fe3+、Fe2+、N3-、42-
. Na+、H-、l-、H2P4-
D. Na+、2+、2-、l-
翰林汇278. 下列变化需要加入氧化剂的是()
A. 2- H-
H-
B. H3- 2↑
2↑
. 2I- I2
I2
D. 2+
翰279. 已知浓H24和Fe3+都可以将氧化成2+,浓H24可将Br-氧化成Br2,Fe与Br2反应生成FeBr3,据此确定物质氧化性由强到弱的顺序是()
A. 浓H24、2+、Fe3+、Br2
B. 浓H24、Br2、Fe3+、2+
. Br2、浓H24、2+、Fe3+
D. 2+、Fe3+、Br2、浓H24
翰林汇280. 关于3l2+6H=l3+l+3H2的反应,以下说法正确的是()
A. l2是氧化剂,H是还原剂
B. 被氧化的氯元素的质量为被还原的 氯元素质量的倍
氯元素质量的倍
. 上述反应是氧化-还原反应
D. H既不是氧化剂,又不是还原剂
翰林汇281. 在3l2+8NH3===6NH4l+N2的反应中,表现还原性的物质是(),还原产物是().
A. l2 B. NH3 . NH4l D. N2
翰林汇282. 选出相应的化学方程式使其与1~4中的叙述相适应
A. Zn+H24(稀)===Zn4+H2↑
B. 6Hl+l3===l+3l2↑+3H2
. 2Mn4 2Mn4+Mn2+2↑
2Mn4+Mn2+2↑
D. l2+2NaI===2Nal+I2
(1)一种单质使一种化合物中的一种元素被氧化()
(2)一种单质使一种化合物中的一种元素被还 原()
原()
(3)同种物质中一种元素氧化另一种元素()
(4)在不同物质中,同种元素之间发生氧化还原反应()
翰林汇283. 下列化学反应中,发生氧化反应的是()
A. Ag++e===Ag B. r272-+6e+14H+===2r3++7H2
. H2===+2H++2e D. Mn42-+8H++e===Mn2++4H2
330. 市场销售的某种食用精制盐包装袋上有如下说明(部分):
|
产品标准 |
 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
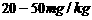 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处): 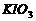 +
+
 +
+ 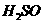 4
=
4
= 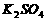 +
+
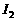 +
+ 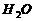
(2)上述反应生成的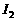 可用四氯化碳检验。向碘的四氯化碳溶液中加入
可用四氯化碳检验。向碘的四氯化碳溶液中加入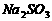 稀溶液,将
稀溶液,将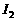 还原,以回收四氯化碳。
还原,以回收四氯化碳。
①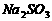 稀溶液与
稀溶液与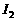 反应的离子方程式是
反应的离子方程式是

②某学生设计回收四氯化碳的操作步骤为:
a、将碘的四氯化碳溶液置于分液漏斗中; b、加入适量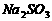 稀溶液;
稀溶液;
、分离出下层液体。
以上设计中遗漏的操作及在上述操作中的位置是
(3)已知: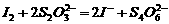
某学生测定食用精制盐的碘含量,其步骤为:
a、准确称取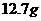 食盐,加适量蒸馏水使其完全溶解;
食盐,加适量蒸馏水使其完全溶解;
b、用稀硫酸酸化所得溶液,加入足量 溶液,使食用盐中
溶液,使食用盐中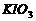 与
与 反应完全;
反应完全;
、以淀粉溶液为指示剂,逐滴加入物质的量浓度为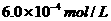 的
的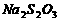 溶液
溶液 ,恰好反应完全。
,恰好反应完全。
①判断中反应恰好完全依据的现象是
②根据以上实验和包装说明,所测精盐的碘含量是 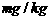
贵州省贵阳一中2011届高三化学一轮复习专题题库:
329.(1)请将种物质:N2、Fe4、Fe(N3)3、HN3和Fe2(4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_________+__________→__________+__________+__________+H2
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 ml氧化剂_______(填“得到”或“失去”)___________ ml电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中,并用单线桥表示:
__________+ __________→
328. “绿色试剂”双氧水可作为矿业废液消毒剂,如要消除采矿业废液中的氰化物(如N),化学方程式为:N+H22+H2=A+NH3↑
(1)生成物A的化学式为
 。
。
(2)在标准状况下有0.448L氨气生成,则转移的电子数为 。
(3)反应中被氧化的元素为 。
(4)H22被称为绿色氧化剂的理由是
 。
。
327. l3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为





 l3+ Hl(浓)= l+ l2↑+
l2↑+ H2
l3+ Hl(浓)= l+ l2↑+
l2↑+ H2
(1)请配平上述化学方程式(计量数填入框内)
(2)浓盐酸在反应中显示出来的性质 是___________(填编号)
是___________(填编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1ml l2,则转移的电子的物质的量为________ml。
326. 已知下述三个实验均能发生化学反应
|
① |
② |
③ |
|
将铁钉放入硫酸铜溶液中 |
向硫酸亚铁溶液中滴入几滴浓硝酸 |
将铜丝放入氯化铁溶液中 |
下列判断正确的是( )
A.上述实验证明氧化性:Fe3+>Fe2+>2+
B.实验②中Fe2+既显氧化性又显还原性
.实验③中发生是置换反应
D.实验①中铁钉只做还原剂
32. 下列说法中不正确的是( )
A.判断氧化还原反应的方法是:是否有氧元素的参与
B.氧化还原反应的实质是电子的得失或偏移
.置换反应一定是氧化还原反应
D.复分解反应一定不是氧化还原反应
323. 在一定条件下,R3n¯与氟气可发生如下反应:R3n-+ F2 +2H- =R4-+ 2F-+H2(已配平),从而可知在R3n- 中,R元素的化合价是( )
A.+4 B.+ .+6 D.+7
 .........m
.........m
324关于3l2 + 6H = l3 + l + 3H2的反应,以下说法正确的是( )
A.l2是氧化剂,H是还原剂
B.被氧化的氯元素的质量为被还原的氯元素质量的倍
.3ml氯气参加反应转移ml电子
D.H既不是氧化剂,又不是还原剂
322. 白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。
(1)白磷是__________________晶体,31g白磷与足量的氧气完全燃烧释放出74.J的热量,请写出白磷燃烧的热化学反应方程式:
____________________________________________________
(2)已知白磷和氯酸溶液可发生如下反应:
□P4 +□Hl3 +□ --□Hl +□H3P4
配平并完成上述反应方程式,该反应的氧化剂是______________。
(3)白磷有毒,有实验室可采用4溶液进行处理,其反应为:
11P4 + 604 + 96H2 = 203P + 24 H3P4 + 60 H24
该反应的氧化产物是___________,若有11ml P4反应,则有________ml电子转移。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com