
题目列表(包括答案和解析)
20.(12分)从煤中可以得到苯及苯的同系物,苯及苯的同系物是重要的有机化工原料。
(1)从煤中得到煤焦油的方法为________;
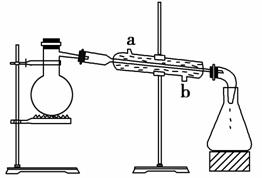
(2)用下面装置从煤焦油中分离出苯及苯的同系物,还需要的仪器为________,冷凝管进水口为________(填“a”或“b”);
(3)用甲苯可以制造一种烈性炸药TNT,反应如下:

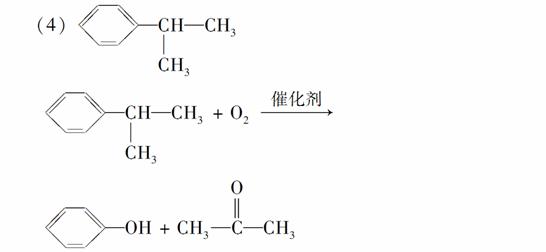
(4)用苯和丙烯可以生产两种重要的有机化工原料:苯酚和丙酮。生产流程如下:
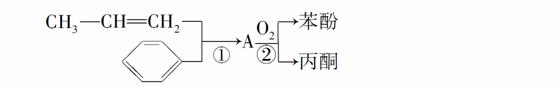
已知反应①是加成反应,A的一氯代物有5种,则A结构简式为________;反应②的化学方程式为_____________________________。
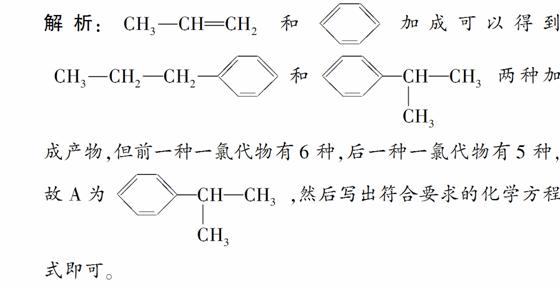
答案:(1)干馏
(2)酒精灯、温度计 b
(3)取代反应
19.(12分)在已经提取氯化钠、溴化镁等化学物质的富碘卤水中,采用下图所示的工艺流程来生产单质碘。
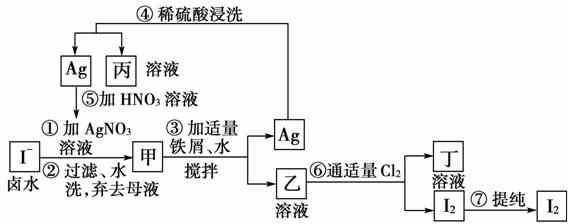
回答下列问题:
(1)写出乙、丁中溶质的化学式:乙_________,丁_________。
(2)第④步操作中用稀H2SO4浸洗的目的是_________ (填写字母编号)。
A.除去未反应的NO3- B.除去未反应的I-
C.除去未反应的铁屑 D.除去碱性物质
(3)第⑦步操作可供提纯I2的一种方法是____________________。
(不要求写出具体步骤)
(4)实验室检验I2的方法是________________________________。
(5)甲物质见光易变黑,原因是(用化学方程式表示): _______________________________________________________。
解析:富碘卤水中的I-与Ag+反应生成AgI(甲),AgI、铁屑在水中经不断搅拌,会缓慢发生反应生成Ag和FeI2(乙),在第④步加入稀H2SO4是溶解多余的铁屑而提纯银,再把银溶于硝酸,制取AgNO3,重新与I-反应。而乙溶液中通入适量Cl2,可生成FeCl3溶液(丁)和I2单质,用萃取的方法提纯碘。
答案:(1)FeI2 FeCl3 (2)C (3)萃取 (4)将I2加到淀粉溶液中,溶液显蓝色 (5)2AgI2Ag+I2
18.(12分)某化学研究性学习小组在实验室中模拟海水提取溴的过程,其实验流程如下:
海水除去悬浮杂质 氧化剂氧化 Br2(g)
Na2CO3溶液吸收[NaBrNaBrO3]Br2
(1)取24 L除去悬浮杂质后的海水,浓缩至2 L;
(2)向其中通入足量Cl2,反应的离子方程式:________________,通入热空气的目的:________________________________;
(3)将吹出的Br2用纯碱溶液吸收,反应得到NaBr、NaBrO3和CO2,反应的化学方程式:________________________,产生的CO2通入足量澄清石灰水中,得到1 g白色沉淀;
(4)将吸收Br2的溶液用足量硫酸处理得到Br2,反应的化学方程式为________________________________,理论上可以得到Br2的质量为________________________;
(5)请计算海水中溴的浓度为________g/L。
解析:通过反应Cl2+2Br-===Br2+2Cl-置换出溴单质后,一般用热空气或水蒸气将Br2吹出;根据各步反应,可确定如下关系:Br2-CO2-CaCO3,根据CaCO3的质量可求出原24 L海水中Br2的质量为=1.6 g,则海水中溴的浓度为=0.067 g/L。
答案:(2)Cl2+2Br-===Br2+2Cl- 将Br2吹出
(3)3Br2+3Na2CO3===5NaBr+NaBrO3+3CO2↑
(4)5NaBr+NaBrO3+3H2SO4===3Br2+3Na2SO4+3H2O 1.6 g
(5)0.067
17.(8分)金属热还原法广泛用于冶金过程中。用金属A(或其合金)作还原剂在高温下将另一种金属B的化合物还原以制取金属B(或其合金)的方法,通常是按还原剂来命名。
(1)用铝作为还原剂生产金属铬,称为铝热法,化学方程式为
_______________________________________________________。
(2)用硅作为还原剂还原V2O3冶炼钒,称为硅热法,化学方程式为________________________________________________________。
硅(特别是硅铁)的价格比铝低,所以硅热还原法在铁合金及某些金属的生产中占有重要地位。但硅的还原能力不如铝,为使硅热还原过程更易进行,常加入CaO。试分析加入CaO的作用: ________。
(3)试写出克劳尔(w.J.Kroll)法即镁热法还原TiCl4生产海绵钛的方程式:____________________________________________________。
解析:由题意可知,本题所涉及的化学反应大都为置换反应,化学方程式可直接根据题设条件和反应物、生成物进行书写。因为Si与V2O3反应生成的SiO2熔点高,不利于反应的继续进行,常加入CaO,与SiO2反应生成CaSiO3,以利于反应的顺利进行(题干中已知)。
答案:(1)2Al+Cr2O32Cr+Al2O3
(2)2V2O3+3Si3SiO2+4V 加入的CaO与生成的SiO2反应:CaO+SiO2CaSiO3,使上述硅热反应更易进行
(3)TiCl4+2MgTi+2MgCl2
16.金属材料在日常生活以及生产中有着广泛的应用。下列关于金属的一些说法不正确的是( )
A.合金的性质与其成分金属的性质不完全相同
B.工业上金属Mg、Al都是用电解熔融的氯化物制得的
C.金属冶炼的本质是金属阳离子得到电子变成金属原子
D.越活泼的金属越难冶炼
解析:选B。工业上制取Mg是电解MgCl2,制取Al是电解氧化铝:MgCl2(熔融)Mg+Cl2↑;2Al2O3(熔融)电解冰晶石4Al+3O2↑。
15.用石油和煤可以得到有机化工生产中需要的众多原料,例如由石油得到的乙烯和由煤得到的苯制聚苯乙烯。
生产过程如下:

下列说法不正确的是( )
A.通过裂解可以从石油中获得更多的乙烯
B.把煤干馏不能直接得到苯
C.制聚苯乙烯的反应①为加成反应,②为消去反应
D.反应①②③的原子利用率都达到了100%
解析:选D。裂解是为了得到更多的有机化工原料如乙烯等;煤干馏只能得到苯和苯的同系物的混合物,还要进行分馏才能得到苯;根据反应特点可知①为加成反应,②为消去反应;反应①③的原子利用率都达到了100%,而反应②中除生成目标产物外,还生成了其他产物,原子利用率小于100%。
14.2008年北京奥运会“祥云”火炬的设计突出体现了“绿色奥运、科技奥运、人文奥运”的理念。下列说法明显错误的是( )
A.“祥云”火炬使用的燃料为丙烷,这是一种价格低廉的常用燃料而且燃烧充分,对环境不造成污染
B.“祥云”火炬的外形材料为轻薄高品质铝合金和中空塑件,均为可回收的环保材料
C.“祥云”火炬的手柄用高触感橡胶漆喷涂,防滑,手感舒适
D.“祥云”火炬的外壳采用了铝材的氧化着色技术,但会缩短火炬的使用寿命
解析:选D。铝材氧化着色会形成保护层,可延长火炬的寿命。
13.若将海水淡化作饮用水使用,下列方法在原理上完全不可行的是( )
A.加明矾使海水中的盐分沉淀而淡化
B.利用太阳能使海水蒸馏淡化
C.将海水慢慢凝固以获取淡化的饮用水
D.将海水通过离子交换树脂,以除去所含离子
解析:选A。明矾净水只是除去水中的悬浮粒子,不能除去海水的Ca2+、Mg2+、Cl-等离子而使其淡化。蒸馏、凝固、离子交换树脂法都能除去海水中的离子使其淡化。
12.节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务。下列举措不符合这一要求的是( )
A.将煤液化、气化,提高燃料的燃烧效率
B.为保证饮食卫生大力提倡使用一次性筷子
C.进一步推广使用乙醇汽油作为汽车的燃料
D.洗涤衣物时合理使用无磷洗衣粉等洗涤剂
解析:选B。使用一次性筷子需要大量的木材。
11.下列说法中,不正确的是( )
A.石油化学工业是以石油为原料,既生产石油产品又生产化学品的石油加工业
B.石油的催化裂化既能提高汽油产量,又能提高汽油的质量
C.石油的裂解和裂化都是化学变化,但二者的目的不一样
D.烷烃在裂解过程中既可发生断链裂解又可发生脱氢裂解
解析:选A。此题意在考查学生对石油炼制及石油化工基本工艺的原料、原理的了解。石油化学工业的原料是石油和天然气,因此A不正确。石油催化裂化既能提高汽油产量又能提高汽油质量;裂解是深度裂化,以获取化工原料--乙烯、丙烯、丁烯为生产目的,故B、C均正确。烷烃裂解方式主要有两种,即断链和脱氢,可表示为Cm+nH2(m+n)+2CnH2n+CmH2m+2,CnH2n+2CnH2n+H2,故D正确。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com