
题目列表(包括答案和解析)
168.今有下列三个氧化还原反应:①2Fel3+2I 2l+2Fel2+I2 ②2Fe+3l2
2l+2Fel2+I2 ②2Fe+3l2 2Fel3
2Fel3
③2Mn4+16Hl 2l+2Mnl2+l2↑+8H2若某溶液中有Fe2+、I-和l-共存,要氧化除去I-而不影响Fe2+和l-,可加入的试剂是( )
2l+2Mnl2+l2↑+8H2若某溶液中有Fe2+、I-和l-共存,要氧化除去I-而不影响Fe2+和l-,可加入的试剂是( )
A.l2 B.Mn4 .Fel3 D.Hl
167.R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应;X2++Z=X+Z2+;Y+Z2+=Y2++Z。这四种离子被还原成0价时表现的氧化性大小符合 ( )
A R2+>X2+>Z2+>Y2+ B X2+>R2+>Y2+>Z2+
Y2+ >Z2+>R2+>X2+ D Z2+>X2+>R2+>Y2+
>Z2+>R2+>X2+ D Z2+>X2+>R2+>Y2+
166.G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的化学式,但知道它们在一定条件下具有 如下的转换关系(未配平):
如下的转换关系(未配平):
① G → Q + Nal
② Q + H2 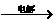 X +
H2
X +
H2
③ Y + NaH → G+ Q+H2 ④ Z + NaH → Q + X + H2
这五种化合物中,氯的化合价由低到高的顺序为 ( )
A.G、Y、Z、Q、X B.Z、X、G、Y、Q
.Q、G、Z、Y、X D.G、Y、Q、Z、X
16.下图为实验室研究炼铁的化学原理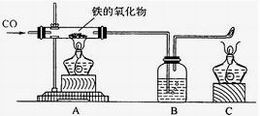 的装置,请回答和该实验有关的问题。
的装置,请回答和该实验有关的问题。
⑴A处玻璃管中发生反应的化学方程式为___________
⑵B处的实验现象_____
⑶处酒精灯的作用______
⑷现有含杂质的氧化铁样 品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
|
|
反应前 |
氧化铁完全反应后 |
|
甲组 |
洗气瓶和石灰水的质量为190g |
洗气瓶和石灰水的质量为196g |
|
乙组 |
玻璃管和氧化铁样品的质量为7.9g |
玻璃管和氧化铁样品的质量为.2g |
你认为应选择___组的数据来计算样品中氧化铁的质量分数,其结果为__ _。
164.将 和
和 的混合物在酸性溶液中用
的混合物在酸性溶液中用 0.07
0.07 溶液处理,发生反应如下:
溶液处理,发生反应如下:
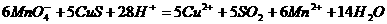
反应后煮沸溶液,赶尽 ,剩余的
,剩余的 恰好与
恰好与
 溶液完全反应。
溶液完全反应。
(1)配平 与
与 反应的离子方程式:
反应的离子方程式:
□ □
□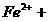 □
□ □
□ □
□ □
□
(2) 溶液与混合物反应后,剩余
溶液与混合物反应后,剩余 的物质的量为
ml。
的物质的量为
ml。
(3)欲配制 溶液,需称取
溶液,需称取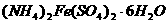
( )的质量为
g。
)的质量为
g。
(4)混合物中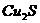 的质量分数为
。
的质量分数为
。
163. (1)请将种物质:N2、Fe4、Fe(N3)3、HN3和Fe2(4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
(1)_________+__________→__________+ __________+__________+H2
__________+__________+H2
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 ml氧化剂_______(填“得到”或“失去”)___________ ml电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
__________+
__________ →
→
162.(1)在淀粉碘化钾的酸性溶液中,滴加少量次氯酸钠溶液,立即会看到溶液变成蓝色,这是因为(用离子方程式表示) 。
(2)在淀粉和碘形成的蓝色溶液中,滴加Na23溶液,又发现蓝色消失,这是因为 (用离子方程式表示) 。
(3)对比以上两组试验所得结果,将I2、l-、42-按氧化性由强到弱顺序排列为:
 。
。
161.某一反应体系有反应物和生成物共五种物质:
2、H2r4、r(H)3、H2、H22。已知该反应中H22只发生如下过程:H22→2
(1) 该反应中的还原剂是 。
(2) 该反应中,发生还原反应的过程是 → 。
(3) 写出该反应的化学方程式,并标出电子转移的方向和数目________________________。
(4) 如反应转移了0.3ml电子, 则产生的气体在标准状况下体积为________。
则产生的气体在标准状况下体积为________。
160.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:N3-+4H++3e→N+2H2 ,现有Mn4、Na23、2、Fe2(4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生0.2ml气体,则转移电子的物质的量是 ml。
(4)若1ml甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: 。
19.针对以下四个涉及H22的反应(未配平),填写空白:
A.Na22+Hl H22+Nal B.Ag2+H22
H22+Nal B.Ag2+H22 Ag+2+H2
Ag+2+H2
.H22 H2+2
D.H22+r2(4)3+H
H2+2
D.H22+r2(4)3+H 2r4+24+H2
2r4+24+H2
(1)H22仅体现氧化性的反应是________,该反应配平的化学方程式为_____________;
(2)H22既体现氧化性又体现还原性的反应是______________________。
(3)H22体现还原性的反应是________________。A体现了H22的 性。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com