
题目列表(包括答案和解析)
31.将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是( )
A.表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠
B.“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液
C.最后变成碳酸钠粉末
D.该过程的所有化学反应均为氧化还原反应
30.甲、乙、丙、丁四个烧杯内分别放人 0.1mol的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入 100mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁的质量分数大小的顺序是 ( )
A.甲<乙<丙<丁 B.丁<甲<乙<丙 C.甲=丁<乙=丙 D.丁<甲<乙=丙
29.现有A、B、C三种白色固体及一种无色气体D。A、B、C均可溶于水,其中C的溶液为碱溶液,焰色反应均呈黄色,且四种物质中间存在如下反应关系:
①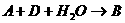 ②
②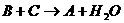
③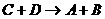 +H2O
④
+H2O
④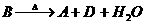
试推断:A是 B是 C是 D是 。 (写化学式)
写出③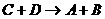 的化学方程式:
的化学方程式:
28.现有NaHCO3和Na2CO3·xH2O的混合物,为了测定x值,革同学采用如下装置进行实验:
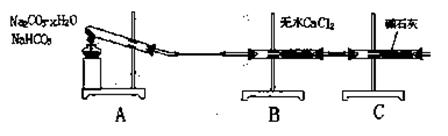
⑴ A的装置的作用是___________________________________。
⑵ B的装置的作用是 _____________________________。
⑶ C的装置的作用是 _____________________________。
⑷若在试管A中装入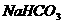 和
和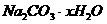 的混合物3.7g,用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22g,通过计算求x值。
的混合物3.7g,用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22g,通过计算求x值。
27.将a mol的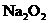 和
和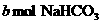 固体混合后,在密闭容器中加热到250℃,让其充分反应,假设
固体混合后,在密闭容器中加热到250℃,让其充分反应,假设 分解产生的
分解产生的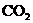 与
与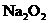
反应完后,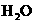 再与
再与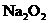 反应.
反应.
(1)当剩余固体为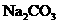 ,排出气体为
,排出气体为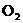 ,
,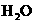 时,
时,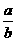 的值为________.
的值为________.
(2)当剩余固体为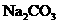 ,NaOH,排出气体为
,NaOH,排出气体为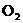 ,
,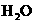 时,
时,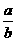 的值为________.
的值为________.
(3)当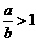 时,剩余固体为________,排出气体为________.
时,剩余固体为________,排出气体为________.
(4)当排出的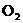 和
和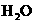 为等物质的量时,则
为等物质的量时,则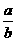 的值为________.
的值为________.
26.一小块钠置于氧气流中加热一段时间后得一固体混合物A。然后将A置于盛满水并倒置于水中的容器中,反应结束后测得产生气体质量为0.5g。用电火花引爆气体,冷却后剩余氧气质量为0.32g,生成的溶液用含HCl 3.65g稀盐酸恰好中和,求:①原来金属钠的质量。②固体A中各组分的质量。
25. Na2CO3和NaHCO3混合物9.5g加入稀盐酸,到不再产生气体为止,恰好用去50g稀盐酸,将生成的气体通入过量的石灰水中,得到沉淀10g,求:①混合物中Na2CO3与NaHCO3各多少g?②所用稀盐酸的溶质质量分数。③所得溶液溶质质量分数。
24.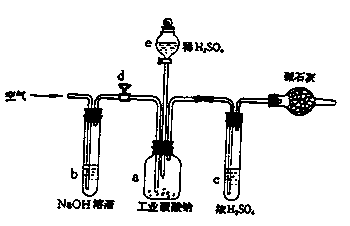 工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如下图的装置:
工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如下图的装置:
操作程序是:1.准确称取盛有碱石灰的干燥管的质量(m1g),再准确称取一定质量纯碱mg并全部放入a中;2.组装全部反应装置并检查气密性,关闭d;由e逐滴加入稀硫酸至不再产生气泡为止;3.打开d,慢慢鼓入空气10min;4.再称干燥管的总质量为m2g。
①(2分)必须鼓入空气的理由是______________________________。
②(2分)不设置装置C将使测定结果______(填“偏大”、“偏小”或“不变”),原因是____________________________。
③(2分)不设置b 将使测定结果______(填“偏大”、“偏小”或“不变”),原因是_____________________________。
④(4分)Na2CO3质量分数的计算式为__________________________。
23.图中,A是单质,B的焰色反应呈黄色。判断A、B、C、D的化学式:
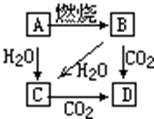 A________ B________ C________ D________
A________ B________ C________ D________
写出下列转化的化学方程式为:
⑴.A→ B________________________________
⑵.B→ D________________________________
⑶.A→ C________________________________
22.一瓶经常使用的NaOH 溶液里常含有的杂质是 ,若要除去杂质而不带入新的杂质所需加入的试剂是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com