
题目列表(包括答案和解析)
10.(2009年浙江绍兴一中高三期末)20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中正确的是 ( )
A.25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1
B.此溶液中KCl的质量分数为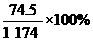
C.20℃时,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174 g·cm-3
9.已知(1)某饱和溶液的体积;(2)密度;(3)溶质和溶剂的质量比;(4)溶质的摩尔质量。要根据溶质的溶解度计算其饱和溶液的物质的量浓度时,在上述条件中,必不可少的是 ( )
A.(1)(2)(3)(4) B.(1)(4)
C.(2)(4) D.(1)(2)(4)
8.有A、B两种硫酸溶液,A溶液硫酸的质量分数为5a %,B溶液硫酸的质量分数为a %,将A、B两溶液等体积混合后,所得硫酸溶液中硫酸的质量分数是 ( )
A.小于3a % B.等于3a %
C.大于3a % D.无法确定
7.有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的c(Na+)(mol/L)为 ( )
A.(y-2x)/a B.(y-x)/a
C.(2y-2x)/a D.(2y-4x)/a
6.某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的溶质质量分数是 ( )
A.30% B.26.5+3.5100+6.5×100%
C.26.5% D.26.5+3.5100+6.5+3.5×100%
5.某溶液中大量存在以下五种离子:NO-3、SO2-4、Fe3+、H+、M,其物质的量之比为n(NO-3)∶n(SO2-4)∶n(Fe3+)∶n(H+)∶n(M)=2∶3∶1∶3∶1,则M可能为 ( )
A.Fe2+ B.Mg2+
C.CO2-3 D.Ba2+
4.设NA为阿伏加德罗常数,下列对于0.3 mol/L硫酸钾溶液的说法不正确的是 ( )
A.1 L溶液中含有0.6 NA个钾离子
B.1 L溶液中含有钾离子和硫酸根离子总数为0.9 NA
C.2 L溶液中钾离子浓度为1.2 mol/L
D.2 L溶液中含有硫酸根离子0.6 NA个
3.(2010年保定模拟)实验室用下列溶质配制一种混合溶液,已知溶液中 则其溶质可能是 ( )
则其溶质可能是 ( )
A.KCl Na2SO4
B.KCl Na2SO4 NaCl
C.NaCl Na2SO4 K2SO4
D.KCl K2SO4 Na2SO4
2.V L Fe2(SO4)3溶液中含Fe3+m g,溶液中SO2-4的物质的量浓度是 ( )

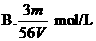


1.下列溶液中的c(Cl-)与50 mL 1 mol/L氯化铝溶液中的c(Cl-)相等的是 ( )
A. 150 mL 1 mol/L氯化钠溶液
B.75 mL 2 mol/L氯化铵溶液
C.150 mL 1 mol/L氯化钾溶液
D.75 mL 1 mol/L氯化铝溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com