
题目列表(包括答案和解析)
29. 有机物A是一种广谱高效食品防腐剂,右图是A 分子
有机物A是一种广谱高效食品防腐剂,右图是A 分子
的球棍模型。回答问题:
(1)写出A的分子式: ;
(2)A能够发生反应的类型有(填写序号): ;
① 氧化反应 ② 加成反应 ③ 取代反应 ④ 消去反应
(3)写出A与烧碱溶液反应的化学方程式:
;
(4)下列是一些中草药中所含的有机物:
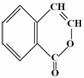

① ②
桂皮酸 异香豆素
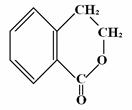

③ ④
二氢异香豆素 香豆素
其中互为同分异构体的是(填写序号): ;
能与Br2水反应的是(填写序号): ;
(5)A的一种同分异构体B在一定条件下可转化为二氢异香豆素,写出B发生消去反应的化学方程式:
;
(6)A的另一种同分异构体C遇FeCl3溶液显紫色;1molC可与1mol NaOH反应生成有机物D;D被Ag(NH3)2OH溶液氧化后经酸化得有机物E,E经酯化、消去两步反应可得香豆素。写出符合上述要求的一种C的结构简式:
。
化学知识点考察检测(5)
DCCA DDDD
27. 已知A 是一种常见的盐,B 、C 、K 为常见金属,K 的氧化物是耐火材料,且能溶于碱溶液。G 为淡黄色固体,H 、F 为无色气体,F 在空气中会变成红棕色。它们的转化关系如下图所示(个别产物略去)。

请回答下列问题:
( 1 ) A 的化学式为______________________
( 2 )在反应① ② ③ ④ 中属于置换反应的是___________________________
( 3 )反应② 的离子方程式为__________________________________________
( 4 )反应⑤ 的总反应化学方程式为__________________________________(填序号)。
*28. 已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。

主要实验步骤如下:
① 按图组装仪器,并检查装置的气密性
② 用托盘天平称取6.0 g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③ 称量盛有碱石灰的U型管的质量得到32.6 g
④ 从分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体时为止
⑤ 从导管A处缓缓鼓入一定量的空气
⑥ 再次称量盛有碱石灰的U型管的质量,得到34.8 g
⑦ 重复步骤⑤和⑥的操作,直到U型管的质量基本不变。
请填空和回答问题:
(1)简述用托盘天平称取6.0g样品的操作步骤(天平已调平)
。
(2)在③步骤中称量质量时涉及到多步添加,撤去法码的操作,请用“↓”表示在托盘上加上砝码,“↑”表示从托盘上取下砝码的称量过程。(法码有50g、20g、10g、5g、2g、1g等多种规格,1g以下移动游码)注:表格可不填满
|
砝码质量/g |
50 |
20 |
|
|
|
|
|
|
|
|
|
|
称量过程 |
↓↑ |
|
|
|
|
|
|
|
|
|
|
(3)装置中干燥管B的作用是
(4)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果 (填偏高、偏低或不变)
(5)步骤⑤的目的是_____________________________、A中NaOH溶液的作用是________________________________________________________________。
(6)步骤⑦的目的是
(7)该试样中纯碱的质量分数为(精确到0.1) .
26. X、Y、Z、W四种短周期元素,其中W元素+1价阳离子是一个质子。X、Y、Z之间的形成化合物有XY2、Z2Y、XY3、Z2Y2、Z2X等。已知Ym-与Zn+两种离子具有相同的电子层结构;Xm-离子比Ym-离子多一层电子。试回答: ⑴ X原子的原子结构示意图是______ ___,它处于周期表中位置________________。 ⑵ Z2Y2的电子式为__ __,W2Y2的结构式 ,该化合物含有化学键类型 。 ⑶ 用电子式表示Z2Y的形成过程__________ __。 ⑷ 又知XY3的水化物与Z2Y2反应可生成一种具有漂白性物质,推测反应时的化学方程式为__________ _______。 ⑸ Z的最高价氧化物对应水化物和X的最高价氧化物对应水化物在溶液中反应的离子方程式是__________ ________。 ⑹ 由X、Y、Z和W四种元素所组成的两种化合物溶液反应产生气体的离子方程式_____________________ ______。
12. 下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸 还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。

下列说法中不正确的是( )
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应 D.当X是强酸时,C在常温下是气态单质
*13. 氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:
aHClO3===bO2↑+cCl2↑+dHClO4+eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法不正确的是 ( ) A变蓝的淀粉碘化钾试纸褪色是因为可能发生了5C12+I2+6 H2O==12H++10C1-+2IO3- B.若氯酸分解所得混合气体,1 mol混合气体经干燥后质量为47.6 g,则反应方程式可表为8HClO3===3O2↑+2Cl2↑+4HClO4+2H2O C.若化学计量数a=8,b=3,则该反应转移电子数为20e- D.由反应可确定氧化性HClO4>HClO3
11.
 *由草木灰提取钾盐并检验钾元素存在的下列实验操作中,错误的是
*由草木灰提取钾盐并检验钾元素存在的下列实验操作中,错误的是
A.溶解 B.过滤 C.蒸发 D.焰色反应
10. 下列说法正确的是 A.在Cu与浓硫酸反应中,欲观察生成的CuSO4溶液的颜色,应采取操作是反应完毕,冷却后,向试管中慢慢加入少量的水,边加边振荡试管。 B.氯气和SO2均可作漂白剂,若同时使用它们去漂白某一润湿的有色物质,其漂白效果会明显加强 C.硫粉在过量的纯氧气中燃烧可以生成三氧化硫 D.二氧化硫能够杀灭霉菌和细菌,可以作为食物和干果的防腐剂
9. *运用元素周期律分析下面的推断,其中错误的是: ①铍(Be)的氧化物的水化物可能具有两性,②铊(Tl)既能与盐酸作用产生氢气,又有跟NaOH溶液反应放出氢气,Tl(NO3)3溶液的酸性很强,③砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸,④锂(Li)在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱,⑤硫酸锶(SrSO4)是难溶于水的白色固体,⑥硒化氢(H2Se)是无色,有毒,比H2S稳定的气体 A.②④⑥ B.①②③④ C.①③⑤ D.②④⑤
8. 对相同状况下的12C18O和14N2两种气体,下列说法正确的是 A.若质量相等,则质子数相等 B.若原子数相等,则中子数相等 C.若分子数相等,则体积相等 D.若体积相等,则密度相等
7. 下列叙述正确的是 A.在CCl4、NH3、PCl5中各原子最外层均能达到8电子的稳定结构 B.13C与C60互为同素异形体 C.M层电子为奇数的所有主族元素所在的族序数与该元素的原子的M层电子数相等 D.
|
6. 用NA表示阿伏加德罗常数,下列说法正确的是: ①18g D2O含有的电子数为10NA ②同温、同压下,相同体积的氟气和氩气所含的原子数相等 ③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA ④在标准状况下,22.4LSO3的物质的量为1mol ⑤2.9g熟石膏(2CaSO4·H2O)中含有的结晶水分子数为0.01NA ⑥3.2gCu与10.0g98%的浓硫酸反应可得0.05 NA个SO2分子 ⑦1mol Na2O2与水完全反应时转移电子数为2NA ⑧2.8g晶体硅中含有的Si-Si键的数目为4NA A.③⑤⑥⑦⑧ B.③④⑤⑥ C.①②④⑦ D.③⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com