
题目列表(包括答案和解析)
1.按核电荷数的增大,氧族元素的下列性质按递增顺序排列的是( )
①单质的熔点 ②元素的非金属性 ③氢化物的还原性 ④与H2反应的能力 ⑤+6价氧化物对应水化物的酸性 ⑥阴离子的半径
A.①②③ B.④⑤⑥ C.③④⑤ D.①③⑥
解析:氧族元素中随核电荷数的增加,其性质呈规律性变化,单质的熔沸点、原子半径、阴离子半径及阴离子的还原性等均递增,而元素的非金属性、单质氧化性、与H2化合的能力、最高价氧化物对应水化物的酸性及其气态氢化物的稳定性等均递减。
答案:D
11.某科研小组,用含有少量的CaO和Fe2O3的高岭土(主要成分: Al2O3·2SiO2·2H2O)来研制新型净水剂,其实验方案如下:将土样和纯碱混合均匀,加热熔融,冷却后用水浸取熔块,过滤弃去残渣,滤液用盐酸酸化,经过滤,分别得到沉淀和溶液,溶液即是净水剂。
(1)溶解时,主要成分与纯碱反应的化学方程式为(提示:①Al2O3与纯碱的反应和SiO2与纯碱的反应相似,②NaAlO2溶于水):
①____________________________________________________________________________。
②____________________________________________________________________________。
(2)最后得到的沉淀物是____________,生成沉淀的离子方程式为______________________。
(3)实验室中常备的坩埚有瓷坩埚、氧化铝坩埚和铁坩埚,本实验熔融土样时应选用_____________坩埚。
解析:这是一道信息给予题,根据题示情境,其实验步骤可整理表示为:

(1)高岭土熔化时,其成分中的SiO2和Al2O3与Na2CO3反应生成Na2SiO3和NaAlO2。
(2)熔块加水使Na2SiO3和NaAlO2溶解与其他杂质分离,在过滤后的滤液中加入盐酸则使Na2SiO3、NaAlO2分别与过量的盐酸反应,生成H4SiO4沉淀和AlCl3溶液,过滤得滤液即为净水剂。
(3)因为瓷坩埚中含有SiO2,氧化铝坩埚主要成分是Al2O3,它们都能与Na2CO3在高温下发生反应,故熔融样品时只能用铁坩埚。
答案:(1)①SiO2+Na2CO3 Na2SiO3+CO2↑
Na2SiO3+CO2↑
②Al2O3+Na2CO3 2NaAlO2+CO2↑
2NaAlO2+CO2↑
(2)H4SiO4
2H++ +H2O====H4SiO4↓
+H2O====H4SiO4↓
(3)铁
10.(2010全国高考理综Ⅱ,26)A、B、C、D、E代表单质或化合物,它们之间的相互转换关系如下所示。A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似。
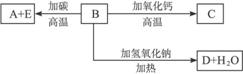
请填空:
(1)形成单质A的原子的结构示意图为_____________,它的最高化合价为_____________。
(2)B的化学式(分子式)为_____________,B的晶体类型为_____________,B和碳反应生成A和E的化学方程式是__________________________________。
(3)C的化学式(分子式)为_____________,D的化学式(分子式)为_____________。
解析:由“A为地壳中含量仅次于氧的非金属单质,晶体结构与金刚石相似”推知A为Si,根据B A+E,B
A+E,B C,B
C,B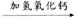 D+H2O,不难推知B为SiO2,C为CaSiO3,D为Na2SiO3。
D+H2O,不难推知B为SiO2,C为CaSiO3,D为Na2SiO3。
答案:
(1)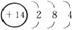 +4
+4
(2)SiO2 原子晶体 SiO2+2C Si+2CO↑
Si+2CO↑
(3)CaSiO3 Na2SiO3
9.石棉是一种具有压伸强度大、柔韧性强、耐热、耐火焰、耐酸和碱的腐蚀,而且价格低廉的硅酸盐。石棉有毒,能使人患肺癌。
(1)有一种石棉叫做矿青石棉,其化学式为Na2Fe5Si8H2O24。写成氧化物形式的化学式为________________________________________。
(2)许多含氧酸及其盐类均可以类似地改写为氧化物的形式,请继续改写以下物质:
HNO3____________________,HCOOH___________________,KAl(SO4)2·12H2O________________。
通过以上改写可知,HNO3的酸酐为__________,HCOOH与H2SO4反应可制_________气体。
(3)已知在一定条件下,Fe在Cl2中燃烧可以生成Fe3Cl8,它可以看作是FeCl2·2FeCl3。类似地,碘与Fe在一定条件下可得到Fe3I8,则它可以看作是__________________________。
解析:将硅酸盐改写成氧化物时,要注意金属氧化物在前,非金属氧化物在后;低价在前,高价在后;H2O一般写在最后。另外书写时应注意金属在化合物中化合价的不同。
答案:(1)Na2O·3FeO·Fe2O3·8SiO2·H2O
(2)N2O5·H2O CO·H2O
K2O·Al2O3·4SO3·24H2O N2O5 CO
(3)3FeI2·I2
8.(2010江苏南通检测)下列有关新材料的说法正确的是( )
A.新材料包括新型无机非金属材料和功能有机高分子材料
B.制作光导纤维的材料是单晶硅
C.美国国家实验室制备的类似于二氧化硅结构的二氧化碳原子晶体与干冰属于同分异构体
D.有机高分子材料全部是通过加聚反应或缩聚反应合成
解析:选项A中新材料包括了新型无机非金属材料和功能有机高分子材料,是正确的;选项B中制作光导纤维的材料应是二氧化硅, 不是单晶硅,故B不正确;C选项中二氧化碳原子晶体与二氧化碳分子晶体类型不同,不互为同分异构体;D选项中有机高分子材料分为天然有机高分子材料和合成有机高分子材料,所以说全部是通过加聚反应或缩聚反应合成是不正确的,故本题只有选项A正确。
答案:A
7.从下面所给的四个词中选出一个与陶瓷、玻璃、水泥同类的( )
A.光导纤维 B.有机玻璃 C.人造纤维 D.砖瓦
解析:从题干所给的信息:陶瓷属于硅酸盐,也属于新型无机非金属材料,玻璃和水泥属于硅酸盐,很明显,另一物质,必须属于硅酸盐才能使其归纳在一起,由此不难得出选项D是正确的。A的主要成分为SiO2,不属于硅酸盐;有机玻璃和人造纤维都属于有机物,不符合题意;砖瓦是陶瓷器中的土器,属于硅酸盐。
答案:D
6.钢化玻璃的用途之一是制造汽车车窗。合成钢化玻璃的主要原料是( )
A.石灰石、纯碱、黏土、硼砂 B.纯碱、石灰石、石英
C.碳酸钾、石灰石、石英 D.水玻璃、石灰石、石英、氧化铅
解析:钢化玻璃的成分与普通玻璃的成分相同,只是后期处理不同。生产普通玻璃的主要原料是纯碱、石灰石、石英,由此可知答案应选B。
答案:B
5.高岭土的组成可表示为Al2Si2Ox(OH)y其中x、y的数值分别是( )
A.7、2 B.5、4 C.6、3 D.3、6
解析:本题涉及两个未知数x、y,但由化合价规则只能列出一个方程,因而要用不定方程的知识求解。
根据化合价规则,Al为+3价,Si为+4价,O为-2价,则有
2×(+3)+2×(+4)+x×(-2)+y×(-1)=0,化简得2x+y=14,将A、B、C、D中的x、y值代入,只有B项符合方程。
答案:B
4.(2010山东名校联考)高温下发生反应:SiO2+3C SiC+2CO↑,其中氧化剂和还原剂的质量比为( )
SiC+2CO↑,其中氧化剂和还原剂的质量比为( )
A.1∶3 B.5∶3 C.1∶2 D.2∶1
解析:此反应中氧化剂为C,还原剂也为C。参加反应的C是3 mol时,有2 mol失电子转化成CO,被氧化,1 mol得电子转化成SiC,被还原,所以氧化剂和还原剂的质量比为1∶2。
答案:C
3.下列说法正确的是( )
A.二氧化硅溶于水显酸性,所以二氧化硅属于酸性氧化物
B.二氧化硅是酸性氧化物,它不溶于任何酸
C.二氧化碳通入水玻璃可以得到原硅酸
D.因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强
解析:二氧化硅不溶于水,能溶于氢氟酸:SiO2+4HF====SiF4↑+2H2O,碳酸钠与二氧化硅在高温下能反应是因为产生的CO2气体不断逸出,使化学平衡不断向生成物的方向移动,故A、B、D不正确。
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com