
题目列表(包括答案和解析)
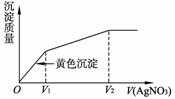
3. (2007年高考上海卷)往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如下图所示。则原溶液中c(I-)/c(Cl-)的比值为( )
A.(V2-V1)/V1B.V1/V2
C.V1/(V2-V1)D.V2/V1
2. 对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间的关系类似于c(H+)·c(OH-)=Kw,存在等式c(M+)·c(X-)=Ksp。一定温度下,将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是 ( )
①20 mL 0.01 mol·L-1KCl溶液
②30 mL 0.02 mol·L-1CaCl2溶液
③40 mL 0.03 mol·L-1 HCl溶液
④10 mL蒸馏水
⑤50 mL 0.05 mol·L-1AgNO3溶液
A.①>②>③>④>⑤
B.④>①>③>②>⑤
C.⑤>④>②>①>③
D.④>③>⑤>②>①
1. 向5 mL NaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶解度关系为( )
A.AgCl=AgI=Ag2S
B.AgCl<AgI<Ag2S
C.AgCl>AgI>Ag2S
D.AgI>AgCl>Ag2S
18. 已知某溶液中只存在OH-、H+、NH+4、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是 ,
上述四种离子浓度的大小顺序为 (填序号)。
(2)若上述关系中:③是正确的,则溶液中的溶质是 ;④是正确的,则溶液中的溶质为 。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,
则混合前c(HCl) c(NH3·H2O)
(填“大于”、“小于”或“等于”,下同),混合前,酸中c(H+)和
碱中c(OH-)的关系c(H+) c(OH-)。
第四节 难溶电解质的溶解平衡
17. 现有常温下的0.1 mol·L-1纯碱溶液。
(1)你认为该溶液呈碱性的主要原因是(用离子方程式表示): 。
为证明你的上述观点,请设计一个简单的实验,简述实验过程: 。
(2)同学甲认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32-离子不超过其总量的10%。请你设计实验证明该同学的观点是否正确。
(3)同学乙就该溶液中粒子之间的关系写出了下列四个关系式,你认为其中正确的是 。
a+)=2c(CO32-)
B.c(CO32-)>c(OH-)>c(HCO3-)>c(H2CO3)
C.c(CO32-)+c(HCO3-)=0.1 mol·L-1
D.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
(4)水解反应是典型的可逆反应。水解反应的化学平衡常数称为水解常数(用Kh表示),请写出Na2CO3第一步水解反应的水解常数的表示式: 。
16. 物质的量浓度相同的①氨水;②氯化铵;③碳酸氢铵;④硫酸氢铵;⑤硫酸铵5种溶液中c(NH+4)的大小顺序是 ,溶液pH的大小顺序是 。
15. 将0.1 mol·L-1的醋酸钠溶液20 mL与0.1 mol·L-1盐酸10 mL混合后,溶液显酸性,则溶液中有关粒子的浓度关系正确的是( )
A. c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH)
B. c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C. c(CH3COO-)=c(Cl-)>c(H+)>c(CH3COOH)
a+)+c(H+)=c(CH3COO-)+c(OH-)
14. (2008年高考重庆卷·理综)向三份0.1 mol·L-1 CH3COONa溶液中分别加入少量NH4NO3、Na2SO3、FeCl3固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
A.减小、增大、减小 B.增大、减小、减小
C.减小、增大、增大 D.增大、减小、增大
13. 下列各溶液中,微粒的物质的量浓度关系正确的是( )
A.0.1 mol·L-1Na2CO3溶液:c(OH-)=c(HCO-3)+c(H+)+c(H2CO3)
B.0.1 mol·L-1NH4Cl溶液:c(NH+4)=c(Cl-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-)
12. (2007年高考海南卷)下列溶液能与镁反应生成氢气的是( )
A.氯化铵溶液 B.氢氧化钠溶液
C.碳酸钾溶液 D.饱和石灰水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com