
题目列表(包括答案和解析)
13. (2009年浙江金华十校联考)下表是五种银盐的溶度积常数
|
化学式 |
AgCl |
Ag2SO4 |
Ag2S |
AgBr |
AgI |
|
溶度积 |
1.8×10-10 |
1.4×10-5 |
6.3×10-50 |
7.7×10-13 |
8.51×10-16 |
下列说法错误的是( )
A.五种物质在常温下溶解度最大的是Ag2SO4
B.将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀
C.对于氯化银、溴化银和碘化银三种物质在常温下的溶解度随着氯、溴、碘的顺序增大
D.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
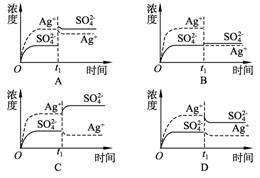
12. (2008年高考广东卷)已知Ag2SO4的Kw为2.0×10-3,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO42-浓度随时间变化关系如图[饱和Ag2SO4溶液中
c(Ag+)=0.034 mol·L-1]。若t1时刻在上述体系中加入100 mL 0.020 mol·L-1 Na2SO4溶
液,下列示意图中,能正确表示t1时刻后Ag+和SO2-4浓度随时间变化关系的是( )
11. 有100 mL MgCl2和AlCl3的混合溶液,其中c(Mg2+)=0.2 mol·L-1,c(Cl-)=1.3 mol·L-1。要使Mg2+完全转化为Mg(OH)2且与Al3+恰好分开,至少需要2 mol·L-1的NaOH溶液的体积为( )
A.80 mL B.100 mL
C.120 mL D.140 mL
10. 向少量Mg(OH)2悬浊液中加入适量的饱和NH4Cl溶液,结果固体完全溶解。对此甲、乙两同学各自作了自己的解释:
甲:Mg(OH)2(s)  Mg2++2OH-①
Mg2++2OH-①
NH4++H2O NH3·H2O+H+②
NH3·H2O+H+②
H++OH-=H2O③
由于③反应的发生,使平衡①右移,Mg(OH)2溶解。
乙:Mg(OH)2(s)  Mg2++2OH-①
Mg2++2OH-①
NH4++OH-=NH3·H2O②
由于②反应的发生,使平衡①右移,沉淀溶解,丙同学用下面的一种试剂重做了该实验,证明甲、乙的解释只有一种正确。他用的试剂是( )
A.NH4NO3 B.CH3COONH4
C.(NH4)2SO4 D.氨水
9. 许多马路两旁的树干都均匀地涂抹了石灰水。下列有关说法不正确的是( )
A.饱和石灰水加入生石灰,若温度不变,则Ca2+的物质的量不变
B.饱和石灰水加入生石灰,若温度不变,则pH不变
C.升高饱和石灰水的温度时,Ca(OH)2的溶度积常数Ksp减小
D.石灰水显碱性,能使蛋白质变性,所以有防治树木害虫病的作用
8. 下列离子方程式中错误的是( )
A.碳酸氢镁与足量NaOH溶液的反应:
Mg2++HCO3-+OH-=MgCO3↓+H2O
B.碳酸氢钙溶液跟盐酸反应:
HCO3-+H+=H2O+CO2↑
C.醋酸跟氢氧化钾溶液反应:
CH3COOH+OH-=CH3COO-+H2O
D.碳酸镁跟稀硫酸溶液反应:
MgCO3+2H+=Mg2++H2O+CO2↑
7. 某无色溶液中,可大量共存的离子组是( )
A.Na+、HCO3-、SO42-、Br-
B.Cu2+、NO3-、Cl-、SO42-
C.Al3+、Cl-、Na+、CO32-
D.K+、Mg2+、SO42-、OH-
6. 在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:Ca(OH)2(s) Ca(OH)2(aq)
Ca(OH)2(aq)
 Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是( )
Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是( )
A.n(Ca2+)增大 B.c(Ca2+)减少
C.n(OH-)增大 D.c(OH-)不变
5. 在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(x)与溶液中沉淀的物质的量(y)的关系示意图正确的是( )

4. 在100 mL 0.10 mol/L的AgNO3溶液中加入100 mL溶有2.08 g BaCl2的溶液,再加入100 mL溶有0.010 mol CuSO4·5H2O的溶液,充分反应。下列说法中正确的是( )
A.最终得到白色沉淀和无色溶液
B.最终得到的白色沉淀是等物质的量的两种化合物的混合物
C.最终得到的溶液中,Cl-的物质的量为0.02 mol
D.在最终得到的溶液中,Cu2+的物质的量浓度为0.01 mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com