
题目列表(包括答案和解析)
8. 根据金属活动性顺序表,Cu不能发生:Cu+2H2O=Cu(OH)2↓+H2↑的反应。但选择恰当电极材料和电解液进行电解,这个反应就能变为现实。下列四组电极和电解液中,能实现该反应最为恰当的是( )
|
|
A |
B |
C |
D |
|
阳极 |
石墨棒 |
Cu |
Cu |
Cu |
|
阴极 |
石墨棒 |
石墨棒 |
Fe |
Pt |
|
电解液 |
CuSO4溶液 |
Na2SO4溶液 |
H2SO4溶液 |
H2O |
7. 下列说法中,正确的是( )
①镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀
②钢铁表面常易锈蚀生成Fe2O3·nH2O
③锌和铁构成原电池时,铁作负极
④铅蓄电池中铅作负极,PbO2作正极,两极浸到稀H2SO4中
A.只有②④
B.只有①③
C.①②③
D.①②③④
6. 如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。下列叙述正确的是 ( )

A.a中铁钉附近呈现红色
B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应
D.b中铝条附近有气泡产生
5. 三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:
用 NaOH调NiCl2溶液pH至7.5,加入适量硫酸钠后进行电解。电解过程中产生的Cl2
在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法正确的是( )
A.可用铁作阳极材料
B.电解过程中阳极附近溶液的pH升高
C.阴极反应方程式为:2Cl--2e-=Cl2↑
D.1 mol二价镍全部转化为三价镍时,外电路中通过了1 mol电子
4. 用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况),从而可知M的相对原子质量为( )
A.22.4ax/b B.11.2ax/b C.5.6ax/b D.2.5ax/b
3. 质量均为100 g的铜为电极电解硝酸银溶液,电解一段时间后,两电极质量相差28 g,此时阳极质量为( )
A.121.6 g B.88.2 g C.89.6 g D.93.6 g
2. 下列有关用惰性电极电解AgNO3溶液一段时间后的说法正确的是( )
A.电解过程中阴极质量不断减少
B.电解过程中溶液的pH不断升高
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解后两极产生的气体体积比为2∶1
1. 下列关于铜电极的叙述正确的是( )
A.铜锌原电池中,铜作负极
B.用电解法精炼粗铜时,粗铜作阴极
C.在镀件上电镀铜时,可用金属铜作阳极
D.电解稀H2SO4制H2、O2时,铜作阳极
17. 有甲、乙两位学生均想利用原电池反应验证金属的活动性顺序,并探究产物的有关性质,分别设计了如下图所示的原电池,请回答:
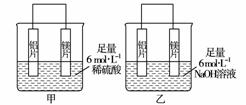
(1)甲池中正极上的实验现象是 。
(2)乙池的总反应的离子方程式为 。
(3)上述实验证明了“利用金属活动性顺序表直接判断原电池正负极”,这种作法 (“可靠”或“不可靠”),如不可靠请你提出另一种判断原电池正负极的可行的方案 。(若你认为可靠,此空可不做答)
(4)一段时间后,乙学生将乙池两极取出,然后取少许乙池溶液逐滴滴加6 mol·L-1H2SO4直至过量,可能观察到的现象是 ,各阶段对应的离子方程式分别是 。
第二节电解池金属的电化学腐蚀与防护
16. (1)今有2H2+O2 2H2O反应,构成燃料电池,则负极通的应是
,正极通的应是
,电极反应式为
、 。
2H2O反应,构成燃料电池,则负极通的应是
,正极通的应是
,电极反应式为
、 。
(2)如把KOH改为稀H2SO4作电解质溶液,则电极反应式为 、 。
(1)和(2)的电解液不同,反应进行后,其溶液的pH各有何变化? 。
(3)如把H2改为甲烷、KOH作导电物质,则电极反应式为: 、 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com