
题目列表(包括答案和解析)
6.向100mLFeBr2溶液中通入标准状况下的C123.36L,C12全部被还原,测得溶液中c(Br-)=c(C1-),则原FeBr2溶液的物质的量浓度是 ( )
A.0.75mol/L B.1.5mol/L C.2 mol/ L D.3 mol/ L
5.下列说法或表示正确的是
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由单质 A转化为单质 B 是一个吸热过程,由于可知单质 B 比单质 A稳定
C. 稀溶液中: H + (aq)+OH - (aq) H2O(l); △H=-57.3kJ/mol, 若将含 0.5molH2SO4 的浓硫酸与含 l mol NaOH 的溶液混合,放出的热量大于 57.3kJ
D.在 101kPa 时,H2 燃烧热化学方程式为 2H2(g)+O2(g) = 2H2O(l);
△H=-571.6kJ/ mol, 则 H2 在 101kPa 时的燃烧热为 571.6kJ/mol
4.在一定条件下,RO3 n- 与 R 2- 发生如下反应: RO3 n- +2R 2- +6H + =3R+3H2O,下列 关于元素 R 的叙述中正确的是 ( )
A.R 原子的最外层上有 4 个电子 B.RO3 n- 中的 R 只能被还原
C.R 的单质既有氧化性又具有还原性 D. HnRO3 一定是强酸
3.为确定某溶液的离子组成,分别进行如下实验:
①测定溶液的 pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性, 产生无刺激性、 能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加 Ba(NO3)2 溶液,产生白色沉淀。
④取上层清液继续滴加 Ba(NO3)2 溶液至无沉淀时, 再滴加 Ag NO3 溶液, 产生白色沉淀。
根据实验以下推测正确的是 ( )
A.一定有 SO3 2- 离子 B.一定有 CO3 2- 离子
C.一定有 C1- 离子存在 D.不能确定 HCO3 - 离子是否存在
2. 一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钆(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对燃料电池说法正确的是( )
A.在熔融电解质中,O2-由负极移向正极
点燃
B.电池的总反应是:2C4H10+13O2 8CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+4e-=2O2-
D.通入丁烷的一极是正极,电极反应为:2C4H10+26e-+13O2-=4CO2+5H2O
1.下列排列顺序正确的是 ( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HC1O4 ④结合质子能力:OH->CH3COO->C1-
A.①③ B.②④ C.①④ D.②③
1.设NA表示阿佛加德罗常数,下列说法正确的是( )
A.1mol CaC2中有3NA个离子
B.1mol SiO2中含有2NA个共价键
C.1L 1mol/L CH3COONa溶液中含NA个CH3COO-离子
D.42g C2H4和C3H6的混合物中一定含有6NA个氢原子
命题意图:高考对NA的考查重现率很高,并且出题很灵活,涉及的知识点也较多,这
一考点是学生必须掌握的。
思路点拨:A选项,C22-为一个离子;B选项,SiO2晶体中一个Si原子与4个O原子成键,1mol SiO2中含有4NA个共价键;C选项,CH3COO-离子部分水解了。
11.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
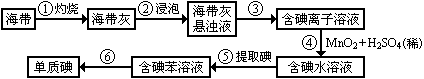
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_________(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是_________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_________。
(3)步骤④反应的离子方程式是____________________________________。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是____________________________。
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:__________。
10. (Ⅰ)针对齐齐哈尔第二制药有限公司(以下简称齐二药)生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭一事,药品安全问题引起人们的关注。“亮菌甲素”结构简式如右图,是黄色或橙黄色结晶粉末,几乎不溶于水,辅料丙二醇(C3H8O2)溶成针剂用于临床。该药为利胆解痉药,适用于急性胆囊炎、慢性胆囊炎急性发作及慢性浅表性胃炎等。
(Ⅰ)针对齐齐哈尔第二制药有限公司(以下简称齐二药)生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭一事,药品安全问题引起人们的关注。“亮菌甲素”结构简式如右图,是黄色或橙黄色结晶粉末,几乎不溶于水,辅料丙二醇(C3H8O2)溶成针剂用于临床。该药为利胆解痉药,适用于急性胆囊炎、慢性胆囊炎急性发作及慢性浅表性胃炎等。
(1)写出“亮菌甲素”的分子式_________________。
(2)1mol 亮菌甲素最多能和_______mol H2发生反应,该反应类型是_______反应。
(3)写出“亮菌甲素”和足量NaOH溶液完全反应的化学反应方程式:_________________。
(Ⅱ)含碳、氢、氧元素的下列有机物分子式通式:
A.Cn(H2O)m B.(C2H3)n(H2O)m C.(C2H)n(H2O)m
D.(CH)n(H2O)m E.(C2O)n(H2O)m F.(CO)n(H2O)m
(1)若充分燃烧某类有机物,消耗氧气的体积与生成二氧化碳的体积之比为5∶4(相同条件下),则该类有机物分子式通式是上述各式中的_________(填代号)。
(2)若某有机物分子式符合上述C的通式,其相对分子质量为136,写出该有机物的分子式_________;若该有机物属于酯类且分子中含有苯环,则其可能的同分异构体有_________种,写出其中不能发生银镜反应的同分异构体的结构简式_________。
9.有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知:A和C、B和D分别位于同主族,且B、D质子数之和是A、C质子数之和的2倍;E在同周期元素中原子半径最小。
(1)A2B和A2D的沸点较高者是_________(填化学式),其原因是_________________;
(2)由A、B、C、D四种元素形成的能发生反应的两种化合物相互反应的离子方程式为_________________;
(3)A、B、C三种元素所形成的化合物的电子式为_________________;
(4)用多孔的石墨电极电解滴有酚酞的C和E形成的化合物的饱和溶液。接通电源一段时间后,_______极(填电极名称)附近出现红色;另一极的电极反应式为__________,可用__________检验该极所得的产物。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com